含铁化合物是重要的基础材料。
请问答:
(1)已知: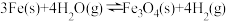
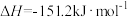 ,
,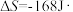
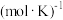 。
。 。当
。当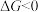 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为___________ K。
(2)高炉炼铁中发生的基本反应之一为:

①在1100℃时,K=0.263,若此时测得高炉中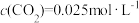 ,
,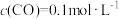 ,判断反应速率
,判断反应速率 (正)
(正)___________  (逆),理由是
(逆),理由是___________ 。
②下列说法不正确的是___________ 。
A.须采用高温高压的反应条件使FeO还原为
B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
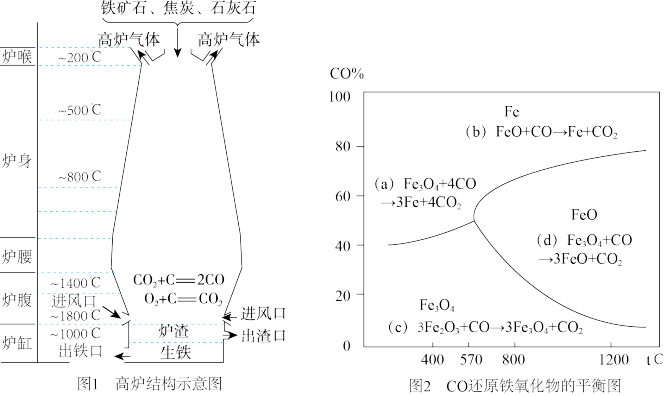
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是___________ (选填:a、b、c、d)。
④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是___________ 。
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是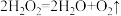 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①___________ ;②___________ 。
请问答:
(1)已知:
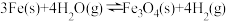
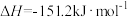 ,
,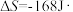
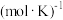 。
。 。当
。当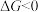 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为(2)高炉炼铁中发生的基本反应之一为:


①在1100℃时,K=0.263,若此时测得高炉中
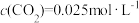 ,
,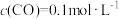 ,判断反应速率
,判断反应速率 (正)
(正) (逆),理由是
(逆),理由是②下列说法不正确的是
A.须采用高温高压的反应条件使FeO还原为

B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是

④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到
 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:| 还原剂 | 600℃ | 700℃ | 800℃ | 900℃ | 1000℃ | 1100℃ | 1200℃ |
| H2 | 4.18 | 3.34 | 2.94 | 2.60 | 2.32 | 2.30 | 2.25 |
| CO | 1.66 | 2.50 | 2.90 | 3.24 | 3.52 | 3.54 | 3.59 |
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是
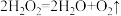 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①
2021·浙江绍兴·模拟预测 查看更多[3]
(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)第七单元 化学反应速率与化学平衡(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省绍兴市2021-2022学年高三上学期11月选考科目诊断性考试化学试题
更新时间:2021-11-12 15:56:28
|
相似题推荐
【推荐1】铁能形成多种化合物,如Fe(SCN)3,[Fe(CO)5](羰基铁),它们在生活生产中有广泛应用。
(1)实验室常用KSCN溶液、K4[Fe(CN)6]溶液、苯酚溶液检验Fe3+。
①K4[Fe(CN)6]溶液可用于检验_______ (填离子符号),现象为_______
②基态K原子核外有_______ 种空间运动状态不同的电子;用钾盐作紫色烟花原料,是因为电子_______ (填标号),产生紫色光。
a.从基态跃迁到激发态释放能量 b.从激发态跃迁到基态释放能量
(2)汽车安全气囊气体发生剂一种组合主要有叠氮化钠(NaN3)、三氧化二铁(Fe2O3)、硝酸铵(NH4NO3)。叠氮化钠收到撞击后产生气体并放出热量,硝酸铵吸收热量分解,金属钠与铁的氧化物反应。叠氮酸根N 的空间构型为
的空间构型为_______ (V形、直线形、平面三角形);NH4NO3为_______ (共价化合物、离子化合物)
(3)实验室常用邻二氮菲检验Fe2+,生成橙红色的邻二氮菲亚铁络离子,选择pH范围为2~9的原因是_______ 。

(4)羰基铁[Fe(CO)5]为分子构成的物质,可用作催化剂。
①1mol[Fe(CO)5]分子中含σ键数目为_______ 。
②据文献报道:Fe(CO)5催化某反应的一种反应机理如下图所示。下列叙述错误的是_______ 。
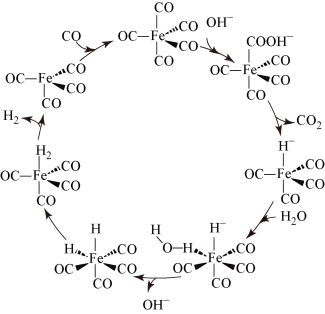
A.OH-参与了该催化循环
B.该反应可产生清洁燃料H2
C.该反应可消耗温室气体CO2
D.该催化循环中Fe的成键数目发生变化
(1)实验室常用KSCN溶液、K4[Fe(CN)6]溶液、苯酚溶液检验Fe3+。
①K4[Fe(CN)6]溶液可用于检验
②基态K原子核外有
a.从基态跃迁到激发态释放能量 b.从激发态跃迁到基态释放能量
(2)汽车安全气囊气体发生剂一种组合主要有叠氮化钠(NaN3)、三氧化二铁(Fe2O3)、硝酸铵(NH4NO3)。叠氮化钠收到撞击后产生气体并放出热量,硝酸铵吸收热量分解,金属钠与铁的氧化物反应。叠氮酸根N
 的空间构型为
的空间构型为(3)实验室常用邻二氮菲检验Fe2+,生成橙红色的邻二氮菲亚铁络离子,选择pH范围为2~9的原因是

(4)羰基铁[Fe(CO)5]为分子构成的物质,可用作催化剂。
①1mol[Fe(CO)5]分子中含σ键数目为
②据文献报道:Fe(CO)5催化某反应的一种反应机理如下图所示。下列叙述错误的是

A.OH-参与了该催化循环
B.该反应可产生清洁燃料H2
C.该反应可消耗温室气体CO2
D.该催化循环中Fe的成键数目发生变化
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】配位化学的应用十分广泛,在经济、生产、生活等方面都有重要作用。
(1)在配合物中部分分子或离子与中心离子较紧密地结合在一起,组成在溶液中能够稳定存在的整体,称为“内界”{书写时用“[ ]”与外界分离}。与中心离子结合不够紧密的离子则处于“外界”。内界和外界不同,物质的性质也不同,如CoCl3与NH3形成的三种配合物A、B、C,Co3+的配位数均为6,但它们的颜色各异,如果各取1molA、B、C溶于水,加入足量硝酸银溶液,分别产生1mol、2mol、3mol白色沉淀。则它们的化学式分别为A:_______ ;B:_______ ,C:_______ ,它们的配体分别是A:_______ ;B:_______ ;C:_______ 。
(2)甲醇和CO合成乙酸时,使用铑羰基化合物[Rh(CO)2I2]-作为催化剂,使得原本需要高压下才能进行的反应在低压下也能进行。其催化机理如图:

①根据Rh的化合价可将I、II、III、IV、V分为:
1)化合价_______ 价,包含_______ ;
2)化合价_______ 价,包含_______ ;(有几种化合价填几类,可不填满,也可增加)
②上述机理中包括_______ 步反应,其中一步为氧化加成,该步反应的方程式为_______ 。
(1)在配合物中部分分子或离子与中心离子较紧密地结合在一起,组成在溶液中能够稳定存在的整体,称为“内界”{书写时用“[ ]”与外界分离}。与中心离子结合不够紧密的离子则处于“外界”。内界和外界不同,物质的性质也不同,如CoCl3与NH3形成的三种配合物A、B、C,Co3+的配位数均为6,但它们的颜色各异,如果各取1molA、B、C溶于水,加入足量硝酸银溶液,分别产生1mol、2mol、3mol白色沉淀。则它们的化学式分别为A:
(2)甲醇和CO合成乙酸时,使用铑羰基化合物[Rh(CO)2I2]-作为催化剂,使得原本需要高压下才能进行的反应在低压下也能进行。其催化机理如图:

①根据Rh的化合价可将I、II、III、IV、V分为:
1)化合价
2)化合价
②上述机理中包括
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在密闭容器中进行可逆反应:CO (g)+NO2(g)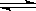 CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
(1)增大容器的体积,平衡____________ ,反应混合物的颜色____________ ;
(2)通入CO2气体,平衡____________ ,反应混合物颜色_______________ ;
(3)升高温度,平衡_______________ ,反应混合物的颜色____________ ;
(4)加入一定量的N2,平衡____________ ,反应混合物的颜色___________ ;
(5)加入催化剂,平衡________________ 。
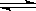 CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)(1)增大容器的体积,平衡
(2)通入CO2气体,平衡
(3)升高温度,平衡
(4)加入一定量的N2,平衡
(5)加入催化剂,平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)一定条件下1 L的密闭容器中,反应mA(g)+nB(g)  pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为
pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为______ mol/(L∙min)。
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,m+n______ p+q(选填“>”、“<”或“=”),v逆______ (选填“增大”、“减小”或“不变”)。
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是________ 。(选填编号,下同)
a.增大A的浓度 b. 缩小容器体积
c. 加入催化剂 d.升高温度
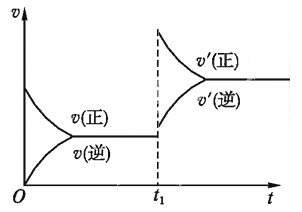
(4)若nV正(A)=mV逆(B),则该反应________ 。
a.向正反应方向进行 b. 向逆反应方向进行 c.处于平衡状态 d.无法判断
 pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为
pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,m+n
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是
a.增大A的浓度 b. 缩小容器体积
c. 加入催化剂 d.升高温度

(4)若nV正(A)=mV逆(B),则该反应
a.向正反应方向进行 b. 向逆反应方向进行 c.处于平衡状态 d.无法判断
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知
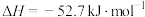 ,常温下N2O4为无色气体。
,常温下N2O4为无色气体。
(1)某课外活动小组为了探究压强对化学平衡的影响,设计了相关实验,请根据所学知识预测实验结果:在容积为30cm3针筒中抽入10cm3的NO2气体,将针筒前端封闭,静置一段时间至气体颜色不变。将针筒活塞拉至20cm3处,此时气体的颜色___________ (填“变深”、“变浅”或“不变”),一段时间后气体颜色___________ (填“变深”、“变浅”或“不变”),但仍比拉动活塞之前针筒内气体的颜色___________ (填“深”或“浅”)。在此过程中,该反应的化学平衡常数___________ (填“增大”、“减小”或“不变”),混合气体中NO2的百分含量___________ (填“增大”、“减小”或“不变”)。
(2)利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

①有关该过程说法正确的是___________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
②反应至B点时NO2的转化率为___________ 。
③图像中C、E两点气体平均摩尔质量较大的点为___________ (填代号)。
(3)某温度下,在体积恒为1 L的密闭容器内,起始时只加入1 mol NO2,达到平衡时其转化率为75%,则该温度下反应 的平衡常数
的平衡常数
___________ L⋅mol-1。

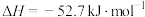 ,常温下N2O4为无色气体。
,常温下N2O4为无色气体。(1)某课外活动小组为了探究压强对化学平衡的影响,设计了相关实验,请根据所学知识预测实验结果:在容积为30cm3针筒中抽入10cm3的NO2气体,将针筒前端封闭,静置一段时间至气体颜色不变。将针筒活塞拉至20cm3处,此时气体的颜色
(2)利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

①有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
②反应至B点时NO2的转化率为
③图像中C、E两点气体平均摩尔质量较大的点为
(3)某温度下,在体积恒为1 L的密闭容器内,起始时只加入1 mol NO2,达到平衡时其转化率为75%,则该温度下反应
 的平衡常数
的平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】汽车尾气中含有CO、NOx等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)已知 4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH=-1200 kJ·mol−1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol−1
①该反应在________________ (填“高温、低温或任何温度”)下能自发进行。
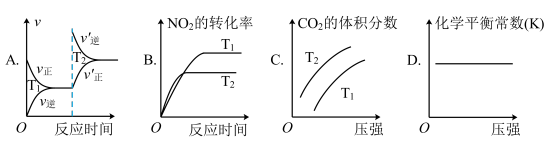
②对于该反应,改变某一反应条件(温度T1>T2),下列图像正确的是_______ (填序号)。
③某实验小组模拟上述净化过程,一定温度下,在2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为__________ ;两种方式达平衡时,N2的体积分数:甲______ 乙( 填“>、=、<或不确定”,下同),NO2的浓度:甲______ 乙。
(2)柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
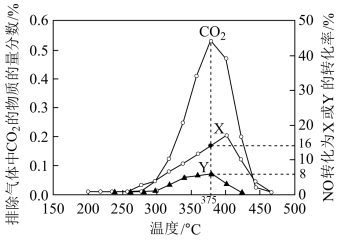
①375℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为________ 。
②实验过程中采用NO模拟NOx,而不采用NO2的原因是__________________ 。
(1)已知 4CO(g)+2NO2(g)
 4CO2(g)+N2(g) ΔH=-1200 kJ·mol−1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol−1①该反应在
②对于该反应,改变某一反应条件(温度T1>T2),下列图像正确的是

③某实验小组模拟上述净化过程,一定温度下,在2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为
| 甲 | 乙 |
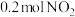 | 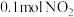 |
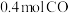 | 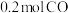 |

| 模拟尾气 | 气体(10mol) | 碳烟 | ||
| NO | O2 | He | ||
| 物质的(mol) | 0.025 | 0.5 | 9.475 | a |
②实验过程中采用NO模拟NOx,而不采用NO2的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
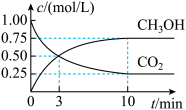
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____ mol/(L·min)。
②该反应的平衡常数表达式为K=_________ 。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________ 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案_______ (填“是”、“否”)可行,理由是:_______ 。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②该反应的平衡常数表达式为K=
③下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量SO2:Cu(s)+2H2SO4(l)=CuSO4(s)+SO2(g)+2H2O(l) ΔH=−11.9kJ·mol-1。判断该反应的自发性并说明理由___________ 。
(2)已知2SO2(g)+O2 2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
①反应开始到第10分钟,SO3反应速率为________ 。
②该温度下反应的平衡常数为________ 。
③平衡时SO2的转化率为________ 。
(3)工业上主要采用接触法用含硫矿石制备硫酸。其主要工艺是焙烧、炉气精制、用钒做催化剂将SO2氧化成SO3、吸收等。结合本大题的信息,完成下题。
①下列说法正确的是______ 。
a.须采用高温高压的反应条件使SO2氧化为SO3
b.通入过量的空气可以提高含硫矿石和SO2的转化率
c.进入接触室之前的气流无需净化处理
②在焙烧前要将硫铁矿粉碎,这样做的目的是______ 。
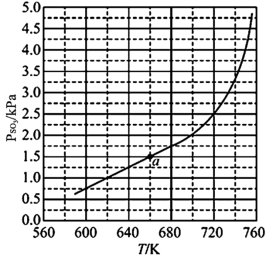
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s) Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)_____ kPa,Kp(Ⅰ)随反应温度升高而_____ (填“增大”“减小”或“不变”)。
(1)实验室可用铜与浓硫酸反应制备少量SO2:Cu(s)+2H2SO4(l)=CuSO4(s)+SO2(g)+2H2O(l) ΔH=−11.9kJ·mol-1。判断该反应的自发性并说明理由
(2)已知2SO2(g)+O2
 2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。①反应开始到第10分钟,SO3反应速率为
②该温度下反应的平衡常数为
③平衡时SO2的转化率为
(3)工业上主要采用接触法用含硫矿石制备硫酸。其主要工艺是焙烧、炉气精制、用钒做催化剂将SO2氧化成SO3、吸收等。结合本大题的信息,完成下题。
①下列说法正确的是
a.须采用高温高压的反应条件使SO2氧化为SO3
b.通入过量的空气可以提高含硫矿石和SO2的转化率
c.进入接触室之前的气流无需净化处理
②在焙烧前要将硫铁矿粉碎,这样做的目的是
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s)
 Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
您最近一年使用:0次




