V、W、X、Y、Z为五种短周期主族元素,它们的原子序数依次增大,其中只有X元素为金属元素。V和X元素原子的最外层电子数相等,Y的最高正价与最低负价的代数和为4,X、Y元素的质子数之和是V、W元素原质子数之和的3倍,Z元素的单质是黄绿色气体,其水溶液能使有色布条褪色。请回答下列问题:
(1)请写出元素符号:V为___________ ,X为___________ W为___________ ,Y为___________ ,Z为___________ 。
(2)Y元素形成的简单离子的结构示意图为___________ 。
(3)V、W、X三种元素形成的简单离子的半径从大到小的顺序为___________ (用离子符号表示)。
(4)由V、W、X三种元素组成的物质为___________ (填化学式),其与 反应的化学方程式为
反应的化学方程式为___________ 。
(5)非金属性:Y___________ Z(填“>”或“<”),请举出一个能说明这一事实的依据:___________ 。
(1)请写出元素符号:V为
(2)Y元素形成的简单离子的结构示意图为
(3)V、W、X三种元素形成的简单离子的半径从大到小的顺序为
(4)由V、W、X三种元素组成的物质为
 反应的化学方程式为
反应的化学方程式为(5)非金属性:Y
更新时间:2024-04-07 14:12:54
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】SiO2属于酸性氧化物,实验室里盛放碱液的玻璃试剂瓶不能用玻璃塞,而常用橡皮塞是因为(用离子方程式表示)_____ ;实验室常用NaOH溶液吸收有毒的氯气尾气,防止污染空气。用离子方程式表示此反应:_____ ;赤热的铁与水蒸气反应的化学方程式为______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】硅与铝同周期。SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O·CaO·6SiO2。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式为____________________________________________ 。长石是铝硅酸盐,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为___________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)保存NaOH溶液的试剂瓶不能用玻璃磨口塞,用离子方程式表示其原因___________ ,工艺师常用___________ (填物质名称)来雕刻玻璃。
(2)绿柱石(绿宝石矿藏的主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO•Al2O3•6SiO2,其n值为___________ 。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作___________ 。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___________ (填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(1)保存NaOH溶液的试剂瓶不能用玻璃磨口塞,用离子方程式表示其原因
(2)绿柱石(绿宝石矿藏的主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO•Al2O3•6SiO2,其n值为
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有以下物质:①氨气② ③
③ ④
④ 胶体⑤
胶体⑤ 溶液⑥S⑦亚硫酸氢钠⑧蔗糖
溶液⑥S⑦亚硫酸氢钠⑧蔗糖
(1)属于非电解质的是_______ (填序号,下同),属于强电解质的是_______
(2)向④中逐滴滴加⑤,可观察到产生红褐色沉淀,后沉淀溶解得到黄色溶液,试写出沉淀溶解的离子方程式:_______ 。
(3)写出⑦在水溶液的电离方程式:_______ 。
(4)②与⑥所对应的元素,非金属性强的是_______ (填元素符号),结合原子结构的知识解释以上结论_______ 。
 ③
③ ④
④ 胶体⑤
胶体⑤ 溶液⑥S⑦亚硫酸氢钠⑧蔗糖
溶液⑥S⑦亚硫酸氢钠⑧蔗糖(1)属于非电解质的是
(2)向④中逐滴滴加⑤,可观察到产生红褐色沉淀,后沉淀溶解得到黄色溶液,试写出沉淀溶解的离子方程式:
(3)写出⑦在水溶液的电离方程式:
(4)②与⑥所对应的元素,非金属性强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请回答下列问题
(1)元素周期律是指______ 随着______ 的递增而呈现______ 变化的规律,该规律背后的根本原因是______ 。
A.原子核外电子排布呈周期性变化 B.元素的相对原子质量逐渐增大
C.原子半径呈现从大到小的周期性变化 D.元素化合价呈周期性变化
(2)如图为元素周期表的一部分。请按要求填空。
①以上元素中,原子半径最小的是______ (写元素符号);最高价氧化物对应水化物中酸性最强的是______ (写化学式),其电离方程式为_____________
②S在元素周期表中的位置是______ ; 电子式为
电子式为____________ , 属于
属于______ 电解质或非电解质)
③下列说法正确的是______
A.可以通过Na和 溶液的置换反应来说明Na和Mg的金属性强弱
溶液的置换反应来说明Na和Mg的金属性强弱
B.离子半径: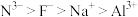
C.氧化性: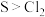
D.F、N、C最高正价依次递减
④C和N中,非金属性较强的是______ (写元素符号),请用一个化学反应方程式说明______ 。
(1)元素周期律是指
A.原子核外电子排布呈周期性变化 B.元素的相对原子质量逐渐增大
C.原子半径呈现从大到小的周期性变化 D.元素化合价呈周期性变化
(2)如图为元素周期表的一部分。请按要求填空。
C | N | F | |||||
Na | Al | S | Cl |
②S在元素周期表中的位置是
 电子式为
电子式为 属于
属于③下列说法正确的是
A.可以通过Na和
 溶液的置换反应来说明Na和Mg的金属性强弱
溶液的置换反应来说明Na和Mg的金属性强弱B.离子半径:
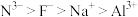
C.氧化性:
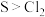
D.F、N、C最高正价依次递减
④C和N中,非金属性较强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】2019年为元素周期表发现150周年,故将2019年定为“国际化学元素周期表年”,新版周期表包含118种元素,表中代表元素周期表前四周期。回答下列问题:
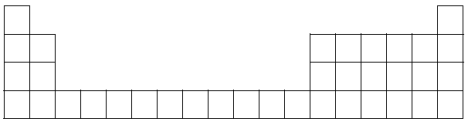
(1)将铁的元素符号填写在上述元素周期表相应的空格中____ 。
(2)短周期元素M、N的原子序数依次增大,原子M、N的最外层电子数均为最内层电子数的2倍。写出工业生产上用M制备N的化学方程式____ 。
(3)下列有关性质的比较正确且能用元素周期律解释的是___ (填标号)。
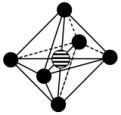
(4)SCl6分子的空间结构为正八面体形(如图所示)。1molSCl6中含有___ molS-Cl键。
(5)写出短周期主族元素中原子半径最大的元素与第二周期第VIA族元素形成的既有离子键又有共价键的物质的电子式____ ,该物质与水反应时,还原剂为____ 。

(1)将铁的元素符号填写在上述元素周期表相应的空格中
(2)短周期元素M、N的原子序数依次增大,原子M、N的最外层电子数均为最内层电子数的2倍。写出工业生产上用M制备N的化学方程式
(3)下列有关性质的比较正确且能用元素周期律解释的是
| A.酸性:HCl>HClO | B.非金属性:N>P |
| C.碱性:NaOH>Al(OH)3 | D.沸点:HF>HCl |

(5)写出短周期主族元素中原子半径最大的元素与第二周期第VIA族元素形成的既有离子键又有共价键的物质的电子式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,请回答下列有关问题
(1)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为_______ 。
(2)由元素①和④形成的四核分子的结构式为_______ 。
(3)由上述元素构成的淡黄色固体化合物的电子式为_______ ,该化合物所含的化学键类型为_______ (填“离子键”、“极性键”或“非极性键”),若将少量该固体投入到含有 、
、 、
、 、
、 的溶液中,反应完全后,上述离子数目增大的有
的溶液中,反应完全后,上述离子数目增大的有_______ (用离子符号表示)。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是_______ (用离子符号表示),元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)元素的非金属性⑧_______ ⑩(填“>”或“<”);下列事实不能证明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素①和④形成的四核分子的结构式为
(3)由上述元素构成的淡黄色固体化合物的电子式为
 、
、 、
、 、
、 的溶液中,反应完全后,上述离子数目增大的有
的溶液中,反应完全后,上述离子数目增大的有(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素的非金属性⑧
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】联合国大会将2019年定为“国际化学元素周期表年” ,显示了元素周期律的重要性。下表列出了7种元素在周期表中的位置:
回答下列问题: 。
(1)⑦的元素符号是___________ ,③的原子结构示意图为___________ 。
(2)上述7种元素中,金属性最强的是___________ ( 填元素符号) ,最高价氧化物对应水化物具有两性的物质是___________ ( 填化学式)。
(3)用“>”、“<”、“=”填空。
(4)③的单质与②的简单氢化物反应的离子方程式为___________ ,
④的单质与③的最高价氧化物对应水化物反应的离子方程式___________ 。
(5)用电子式表示③和⑤形成化合物的过程___________ 。
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | |||||
| 4 | ⑥ | ⑦ | ||||||
(1)⑦的元素符号是
(2)上述7种元素中,金属性最强的是
(3)用“>”、“<”、“=”填空。
| 类别 | 比较 |
| 简单氢化物稳定性 | ① |
| 简单离子半径 | ③ |
| 元素的非金属性 | ⑤ |
④的单质与③的最高价氧化物对应水化物反应的离子方程式
(5)用电子式表示③和⑤形成化合物的过程
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1) Al元素在元素周期表中的位置为_______ ,K2O的电子式为_______ 。
(2)上述元素中(Si除外),形成的简单离子的半径由大到小的顺序为_______ (填离子符号)。
(3)简单氢化物的稳定性:H2O_______ SiH4(填“>”、“<”或“=”)
(4)白云石所含的两种金属元素中,金属性较强的元素是_______ ,写出一个能说明这一事实的化学方程式_______ 。
(5)已知硅酸(H2SiO3)为白色胶状沉淀。若要利用下图装置证明非金属性:
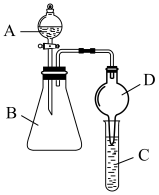
C>Si,则A中加_______ ,B中加Na2CO3,C中加_______ 。(可供选择的药品:稀硫酸、盐酸、稀硝酸、硅酸钠溶液、饱和碳酸氢钠溶液。)
(1) Al元素在元素周期表中的位置为
(2)上述元素中(Si除外),形成的简单离子的半径由大到小的顺序为
(3)简单氢化物的稳定性:H2O
(4)白云石所含的两种金属元素中,金属性较强的元素是
(5)已知硅酸(H2SiO3)为白色胶状沉淀。若要利用下图装置证明非金属性:

C>Si,则A中加
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】有A、B、C、D四种元素,已知A元素原子的K层和M层电子数相同;B元素原子的L层比K层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的最外层电子数是次外层电子数的3倍。
(1)写出元素符号:A________ ,D________ 。
(2)A的原子结构示意图_______________ ,B的离子结构示意图______________ ,C的离子结构示意图______________________ 。
(3)D原子的电子式________________ 。
(4)A和B元素组成的物质的化学式为________ ,它是由________ (选填“原子”、“离子”或“分子”)构成的物质。
(5)由C和D可组成CD2-离子,一个CD2-离子所带电子数为________ 。
(1)写出元素符号:A
(2)A的原子结构示意图
(3)D原子的电子式
(4)A和B元素组成的物质的化学式为
(5)由C和D可组成CD2-离子,一个CD2-离子所带电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的―1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题。
(1)B元素在元素周期表中的位置是第______ 周期______ 族。
(2)画出D元素的原子结构示意图____________ 。
(3)与E的氢化物分子所含电子总数相等的分子是____________ (举一例、填化学式,下同)、离子是____________ 。
(4)A与C形成的化合物中含有化学键的类型是____________ 。
(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为________________________ 。
(1)B元素在元素周期表中的位置是第
(2)画出D元素的原子结构示意图
(3)与E的氢化物分子所含电子总数相等的分子是
(4)A与C形成的化合物中含有化学键的类型是
(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】联合国将2019年定为“国际化学元素周期表年”,新版周期表包含118种元素,下表代表元素周期表前四周期,回答下列问题:

(1)表中的实线是元素周期表的部分边界,请在图中用实线画出金属元素与非金属元素的分界线,将硼、磷的元素符号填写在上述周期表相应的空格中_____ 。
(2)某元素的原子次外层电子数比最外层电子数多1个,单质常温下为黄绿色气体,该元素的最高价氧化物对应水化物的电离方程式为_____ 。
(3)下列有关性质的比较正确,且能用元素周期律解释的是___________ 。
a.非金属性:O>S b.热稳定性:HF<HCl
c.酸性:HCl>H2SO3 d.碱性:NaOH>Mg(OH)2
(4)某金属单质既可以和强酸反应也可以和强碱溶液反应,写出对应的离子方程式___________ ;___________ 。
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为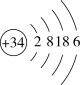 。
。
①Se在元素周期表中的位置是___________ 。
②Se的简单气态氢化物的化学式为___________ 。
③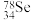 和
和 互称为
互称为___________ 。

(1)表中的实线是元素周期表的部分边界,请在图中用实线画出金属元素与非金属元素的分界线,将硼、磷的元素符号填写在上述周期表相应的空格中
(2)某元素的原子次外层电子数比最外层电子数多1个,单质常温下为黄绿色气体,该元素的最高价氧化物对应水化物的电离方程式为
(3)下列有关性质的比较正确,且能用元素周期律解释的是
a.非金属性:O>S b.热稳定性:HF<HCl
c.酸性:HCl>H2SO3 d.碱性:NaOH>Mg(OH)2
(4)某金属单质既可以和强酸反应也可以和强碱溶液反应,写出对应的离子方程式
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为
 。
。①Se在元素周期表中的位置是
②Se的简单气态氢化物的化学式为
③
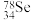 和
和 互称为
互称为
您最近一年使用:0次



