某小组同学欲研究 的性质。
的性质。
(1)将相关的含硫物质分为如下表所示 组,第
组,第 组中物质
组中物质 的化学式是
的化学式是___________ 。
(2)利用下图所示的装置研究 的性质:
的性质:

①在 中检验
中检验 的氧化性,则
的氧化性,则 中发生的化学反应方程式:
中发生的化学反应方程式:___________ 。
②在C中装 溶液,目的是检验
溶液,目的是检验 的还原性,溶液逐渐褪色,生成
的还原性,溶液逐渐褪色,生成 ,同时
,同时 降低,则C中反应的离子方程式为
降低,则C中反应的离子方程式为___________ 。
③在 中有
中有 溶液,反应后增重
溶液,反应后增重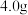 ,则装置
,则装置 中发生反应的总化学方程式是
中发生反应的总化学方程式是___________ 。
 的性质。
的性质。(1)将相关的含硫物质分为如下表所示
 组,第
组,第 组中物质
组中物质 的化学式是
的化学式是| 第1组 | 第2组 | 第3组 |
| S(单质) |  、 、 、 、 、 、 |  、 、 、 、 、 、 |
(2)利用下图所示的装置研究
 的性质:
的性质: 
①在
 中检验
中检验 的氧化性,则
的氧化性,则 中发生的化学反应方程式:
中发生的化学反应方程式:②在C中装
 溶液,目的是检验
溶液,目的是检验 的还原性,溶液逐渐褪色,生成
的还原性,溶液逐渐褪色,生成 ,同时
,同时 降低,则C中反应的离子方程式为
降低,则C中反应的离子方程式为③在
 中有
中有 溶液,反应后增重
溶液,反应后增重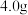 ,则装置
,则装置 中发生反应的总化学方程式是
中发生反应的总化学方程式是
更新时间:2024-04-08 11:24:51
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】黄铁矿(主要成分为FeS2)曾是我国大多数硫酸厂制取硫酸的主要原料。某化学学习小组对黄铁矿石进行如下实验探究。
[实验一]测定硫元素的含量。
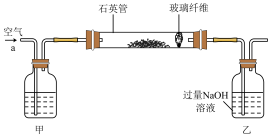
I.将m1g该黄铁矿样品放入如图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
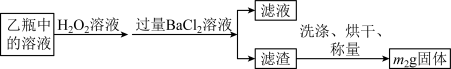
Ⅱ.反应结束后,将乙瓶中的溶液进行如下图所示处理。
[实验二]测定铁元素的含量。
Ⅲ.测定铁元素的含量的实验步骤如下图所示。
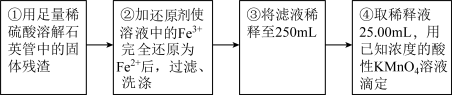
问题讨论:
(1)上述装置中,甲瓶内所盛试剂是____________ 溶液。
(2)向乙瓶溶液中滴加H2O2溶液时,发生氧化还原反应的离子方程式为_______ 。
Ⅱ中除了可以用H2O2溶液作为氧化剂,还可以加入____________ (填序号)。
①氯水 ②浓H2SO4 ③HNO3 ④Fe2(SO4)3
(3)该黄铁矿中硫元素的质量分数为___________________ 。
(4)Ⅲ的步骤②中,若选用铁粉作还原剂,你认为合理吗?并说明理由。(如合理,则此空不填)___________ (填“合理“或”不合理“)、_____ (如合理,则此空不填)。
(5)若要测定铁元素的含量,则步骤Ⅲ中还需要测定的数据有______________ 。
[实验一]测定硫元素的含量。
I.将m1g该黄铁矿样品放入如图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2
 2Fe2O3+8SO2
2Fe2O3+8SO2
Ⅱ.反应结束后,将乙瓶中的溶液进行如下图所示处理。

[实验二]测定铁元素的含量。
Ⅲ.测定铁元素的含量的实验步骤如下图所示。

问题讨论:
(1)上述装置中,甲瓶内所盛试剂是
(2)向乙瓶溶液中滴加H2O2溶液时,发生氧化还原反应的离子方程式为
Ⅱ中除了可以用H2O2溶液作为氧化剂,还可以加入
①氯水 ②浓H2SO4 ③HNO3 ④Fe2(SO4)3
(3)该黄铁矿中硫元素的质量分数为
(4)Ⅲ的步骤②中,若选用铁粉作还原剂,你认为合理吗?并说明理由。(如合理,则此空不填)
(5)若要测定铁元素的含量,则步骤Ⅲ中还需要测定的数据有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫代硫酸钠(Na2S2O3)可看成是一个S原子取代了Na2SO4中的一个O原子而形成。某校化学研究性学习小组运用类比学习的思想,通过实验探究Na2S2O3的化学性质。
【提出问题】Na2S2O3是否与Na2SO4相似具备下列性质呢?
猜想①:_______________________________________________________ ;
猜想②:溶液呈中性,且不与酸反应;
猜想③:无还原性,不能被氧化剂氧化。
【实验探究】基于上述猜想②③,设计实验方案。
【实验结论】Na2S2O3能与酸反应,具有还原性,与Na2SO4的化学性质不相似。
【问题讨论】
(1)甲同学向探究“猜想③”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由__________________________ 。
(2)请重新设计一个实验方案,证明Na2S2O3被氯水氧化。该实验方案是_______________________ 。
【提出问题】Na2S2O3是否与Na2SO4相似具备下列性质呢?
猜想①:
猜想②:溶液呈中性,且不与酸反应;
猜想③:无还原性,不能被氧化剂氧化。
【实验探究】基于上述猜想②③,设计实验方案。
| 实验操作 | 实验现象或预期实验现象 | 现象解释(用离子方程式表示) | |
| 猜想② | 溶液pH=8 | ||
| 向pH=2的硫酸中滴加Na2S2O3溶液 | S2O32—+2H+=S↓+SO2↑+H2O | ||
| 猜想③ | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 |
【问题讨论】
(1)甲同学向探究“猜想③”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由
(2)请重新设计一个实验方案,证明Na2S2O3被氯水氧化。该实验方案是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】在一定条件下,金属单质X和非金属单质Y能够反应,生成化合物Z,Z能与水发生水解反应生成气体G和白色沉淀P(如下框图所示),已知气体G与空气之密度比约为1.17。请填空:

(1)组成单质X和Y的元素分别属第____________ 族和第___________ 族;
(2)Z与水发生水解反应方程式_____________________ ;
(3)每生成1mol的化合物Z,反应中转移_________________ mol的电子。

(1)组成单质X和Y的元素分别属第
(2)Z与水发生水解反应方程式
(3)每生成1mol的化合物Z,反应中转移
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末,常用作有机反应的催化剂。实验室制备CuBr的实验步骤和装置如图。

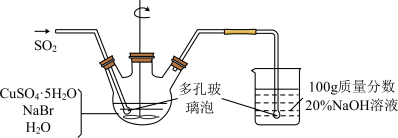
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去蒸馏水中的_______ (写化学式); 三颈烧瓶中反应生成CuBr的离子方程式为_______ ;控制反应在60℃进行,实验中可采取的措施是 _______ ;说明反应已完成的现象是 _______ 。
(2)步骤②抽滤需要避光的原因是_______ ,步骤③依次用溶有少量SO2的水、溶有少量SO2的乙醇、极易挥发的乙醚洗涤,洗涤剂需“溶有SO2”的原因是_______ ;最后用乙醚的目的可能是_______ 。
(3)将产品在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6g。本实验产品的产率是_______ (保留小数点后1位)。
(4)欲利用上述装置烧杯中的吸收液(经检测主要含有Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。完善下列步骤:①在烧杯中继续通入SO2至恰好反应完全;②向烧杯中加入_______ g 20% NaOH;③加入少量维生素C溶液作抗氧化剂;④通过蒸发浓缩、_______ 、过滤、用乙醇洗涤2~3次;⑤置于真空干燥箱中干燥。


(1)实验所用蒸馏水需经煮沸,煮沸目的是除去蒸馏水中的
(2)步骤②抽滤需要避光的原因是
(3)将产品在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6g。本实验产品的产率是
(4)欲利用上述装置烧杯中的吸收液(经检测主要含有Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。完善下列步骤:①在烧杯中继续通入SO2至恰好反应完全;②向烧杯中加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全。确定分解产物的成分。
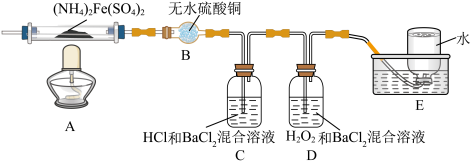
(1)B装置的作用是_________ 。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中一定有_______ 气体产生,写出D中发生反应的离子方程式________ 。
(3)A中固体分解后产生NH3,写出其两种用途_________ 。
(4)用实验的方法验证C溶液含有NH4+:_________ 。

(1)B装置的作用是
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中一定有
(3)A中固体分解后产生NH3,写出其两种用途
(4)用实验的方法验证C溶液含有NH4+:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为测定某地空气中SO2和可吸入颗粒的含量,某同学设计了如下图所示的实验装置:
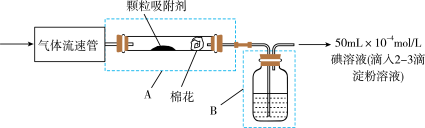
注:①气体流速管是用来测量单位时间内通过气体体积的装置
②颗粒吸附剂用于吸附可吸入颗粒
(1)上述实验测定SO2的原理为___________ (用化学方程式表示)。
(2)应用上述装置测定空气中SO2和可吸入颗粒的含量,除需测定气体流速(单位:mL·s-1)外,还需要测定碘溶液蓝色褪去所需的时间和___________ 。
(3)已知:碘单质微溶于水,KI可以增大碘在水中溶解度。为精确配制100mL5.0×10-4mol·L-1的碘溶液,先要配制1000mL1.0×10-2mol·L-1碘溶液,再取5.00mL溶液稀释成为5.0×10-4mol·L-1碘溶液。
①第一步:用托盘天平称取___________ g碘单质加入烧杯中,同时加入少量碘化钾固体,加适量水搅拌使之完全溶解。
②第二步:___________ ,洗涤、定容、摇匀。
(4)空气中SO2含量的测定:
①已知空气中二氧化硫的最大允许排放浓度不得超过0.02mg·L-1,在指定的地点取样,以200mL·s-1气体流速通过气体流速管通入到上图实验装置中,观察记录碘溶液褪色所需时间为500s,则该地空气中的SO2含量是___________ mg·L-1,___________ (填“符合”、“不符合”)排放标准。
②如果甲同学用该方法测量空气中SO2的含量时,所测得的数值比实际含量低,其原因可能是___________ (假设溶液配制、称量或量取及各种读数均无错误。写出一种可能原因即可)

注:①气体流速管是用来测量单位时间内通过气体体积的装置
②颗粒吸附剂用于吸附可吸入颗粒
(1)上述实验测定SO2的原理为
(2)应用上述装置测定空气中SO2和可吸入颗粒的含量,除需测定气体流速(单位:mL·s-1)外,还需要测定碘溶液蓝色褪去所需的时间和
(3)已知:碘单质微溶于水,KI可以增大碘在水中溶解度。为精确配制100mL5.0×10-4mol·L-1的碘溶液,先要配制1000mL1.0×10-2mol·L-1碘溶液,再取5.00mL溶液稀释成为5.0×10-4mol·L-1碘溶液。
①第一步:用托盘天平称取
②第二步:
(4)空气中SO2含量的测定:
①已知空气中二氧化硫的最大允许排放浓度不得超过0.02mg·L-1,在指定的地点取样,以200mL·s-1气体流速通过气体流速管通入到上图实验装置中,观察记录碘溶液褪色所需时间为500s,则该地空气中的SO2含量是
②如果甲同学用该方法测量空气中SO2的含量时,所测得的数值比实际含量低,其原因可能是
您最近一年使用:0次



