无论是在环境保护领域还是工农业生产领域,氮及其化合物一直是人们的研究重点:
I.某实验小组利用以下装置制取氨气并探究氨气的部分性质:
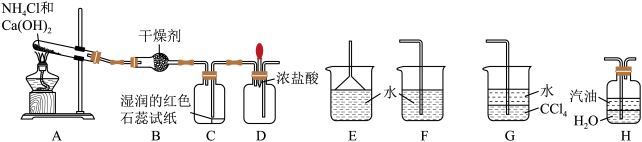
(1)装置A中发生反应的化学方程式为_______ 。
(2)装置B中的干燥剂是_______ (填名称)。
(3)装置C中可观察到的现象是_______ 。
(4)实验进行一段时间后,挤压D中的胶头滴管,向其中滴入1~2滴浓盐酸,可观察到的现象是_______ 。
(5)为防止过量氨气外逸,需要上述装置的末端增加一个尾气吸收装置,上述可选用的装置有_______ (填“E”、“F”、“G”或“H”)。
Ⅱ.工业制硝酸时尾气中含有NO、 ,可选择碱液吸收。用不同浓度的NaOH溶液吸收
,可选择碱液吸收。用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如下图:(
含量不同的尾气,关系如下图:( )
)
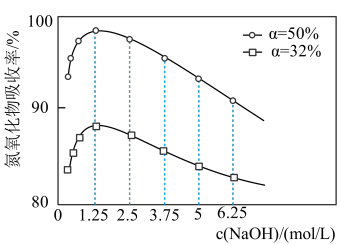
(6)据图得知_______ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
(7)当 小于50%时,加入
小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是_______ 。
I.某实验小组利用以下装置制取氨气并探究氨气的部分性质:

(1)装置A中发生反应的化学方程式为
(2)装置B中的干燥剂是
(3)装置C中可观察到的现象是
(4)实验进行一段时间后,挤压D中的胶头滴管,向其中滴入1~2滴浓盐酸,可观察到的现象是
(5)为防止过量氨气外逸,需要上述装置的末端增加一个尾气吸收装置,上述可选用的装置有
Ⅱ.工业制硝酸时尾气中含有NO、
 ,可选择碱液吸收。用不同浓度的NaOH溶液吸收
,可选择碱液吸收。用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如下图:(
含量不同的尾气,关系如下图:( )
)
(6)据图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大(7)当
 小于50%时,加入
小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是
更新时间:2024-04-08 13:22:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】碱式氯化镁[ ]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。
]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。

请回答下列问题:
(1)装 溶液的仪器名称是
溶液的仪器名称是_______ 。装置B的作用是_______ 。
(2)上述实验装置中存在的一处明显错误是_______ 。
(3)写出装置A中发生反应的离子方程式:_______ 。
(4)装置C中发生反应的化学方程式为_______ 。
(5)装置F中倒置漏斗的作用是_______ 。
(6)在空气中加热 也可制备
也可制备 ,若将
,若将 和
和 混合共热可制备无水
混合共热可制备无水 ,
, 的作用是
的作用是_______ 。
 ]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。
]和氨气都是重要的化工产品和原料。某小组拟用氢氧化镁和氯化铵反应制备碱式氯化镁和氨气(实验室用亚硝酸钠溶液和氯化铵溶液共热制备氮气)。
请回答下列问题:
(1)装
 溶液的仪器名称是
溶液的仪器名称是(2)上述实验装置中存在的一处明显错误是
(3)写出装置A中发生反应的离子方程式:
(4)装置C中发生反应的化学方程式为
(5)装置F中倒置漏斗的作用是
(6)在空气中加热
 也可制备
也可制备 ,若将
,若将 和
和 混合共热可制备无水
混合共热可制备无水 ,
, 的作用是
的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的循环涉及多种化学物质(下图中的W、M、X、Y、Z均是化学物质)
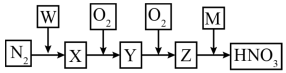
(1)由N2→X是工业合成氨的反应,每消耗7gN2放出23.4kJ的能量,写出该反应的热化学方程式_______ 。
(2)实验室中有一种物质常用作氧化剂,可以使Y直接转化为硝酸且绿色环保,写出该物质与Y反应的化学方程式:_______ 。
(3)某化学兴趣小组设计了如图所示的浓 与
与 反应的微型实验,下列说法中错误的是
反应的微型实验,下列说法中错误的是_______ (填标号)。

A.挤压塑料瓶使浓 进入干燥管就可引发反应
进入干燥管就可引发反应
B.将装置口向上提起就可停止反应
C.蘸碱液的棉花可用蘸水的棉花替代
D.该装置适用于木炭与浓硝酸或浓硫酸的反应实验
(4)某同学利用如图装置让氨气与氧化铜反应,验证氨气的性质并验证部分产物(部分装置未画出)。发现反应确实能发生,且反应后得到三种物质,其中有两种单质。

请回答下列问题:
①实验室制取氨气的化学方程式是_______ 。
②从氨中N元素的化合价角度看,该同学想证明的是氨的_______ ,实验中观察到_______ ,则能够证明氨具有这个性质。
③B装置的作用是_______ 。
④A中反应的化学方程式是_______ 。

(1)由N2→X是工业合成氨的反应,每消耗7gN2放出23.4kJ的能量,写出该反应的热化学方程式
(2)实验室中有一种物质常用作氧化剂,可以使Y直接转化为硝酸且绿色环保,写出该物质与Y反应的化学方程式:
(3)某化学兴趣小组设计了如图所示的浓
 与
与 反应的微型实验,下列说法中错误的是
反应的微型实验,下列说法中错误的是
A.挤压塑料瓶使浓
 进入干燥管就可引发反应
进入干燥管就可引发反应B.将装置口向上提起就可停止反应
C.蘸碱液的棉花可用蘸水的棉花替代
D.该装置适用于木炭与浓硝酸或浓硫酸的反应实验
(4)某同学利用如图装置让氨气与氧化铜反应,验证氨气的性质并验证部分产物(部分装置未画出)。发现反应确实能发生,且反应后得到三种物质,其中有两种单质。

请回答下列问题:
①实验室制取氨气的化学方程式是
②从氨中N元素的化合价角度看,该同学想证明的是氨的
③B装置的作用是
④A中反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氨基甲酸铵( )是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
)是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
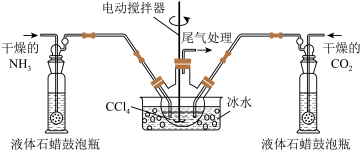
已知:①制取氨基甲酸铵反应为: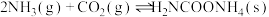
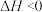 。
。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
③四氯化碳与液体石蜡均为惰性介质。
回答下列问题:
(1)若用如图所示装置制取氨气,你所选择的试剂是_______ 。
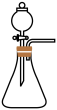
(2)液体石蜡鼓泡瓶的作用是_______ ,尾气处理装置中的试剂是_______ 。
(3)三颈烧瓶需用冰水浴冷却,其目的是_______ 。
(4) 液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是
液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是_______ 。
(5)将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到平衡: 。可以判断该反应已经达到平衡的是_______。
。可以判断该反应已经达到平衡的是_______。
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是_______ 。(计算结果保留四位有效数字)[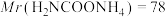 、
、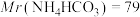 ]
]
 )是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
)是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
已知:①制取氨基甲酸铵反应为:
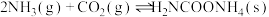
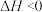 。
。②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
③四氯化碳与液体石蜡均为惰性介质。
回答下列问题:
(1)若用如图所示装置制取氨气,你所选择的试剂是

(2)液体石蜡鼓泡瓶的作用是
(3)三颈烧瓶需用冰水浴冷却,其目的是
(4)
 液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是
液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是(5)将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到平衡:
 。可以判断该反应已经达到平衡的是_______。
。可以判断该反应已经达到平衡的是_______。A. |
| B.容器中总压强不变 |
| C.容器中混合气体的平均相对分子质量不变 |
| D.容器中氨气的体积分数不变 |
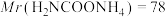 、
、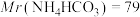 ]
]
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】I.利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:

(1)一定条件下,NO与NO2存在下列反应:NO(g) + NO2(g) N2O3(g),其平衡常数表达式为K =
N2O3(g),其平衡常数表达式为K = ____ 。
(2)吸收时,尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋,好处是____ 。
(3)为提高Ca(NO2)2的产率及纯度,则n(NO)∶n(NO2)应控制为____ 。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为___ 。
II.铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原—氯化法可实现由铝土矿制备金属铝,相关的热化学方程式如下:
Al2O3(s) + AlCl3(g) + 3C(s) =3AlCl(g) + 3CO(g) △H = a kJ·mol—1
3AlCl (g)=2Al(l) + AlCl3(g) △H = bkJ·mol—1
则Al2O3(s) + 3C(s) =2Al(l) + 3CO(g) △H =__ kJ·mol—1(用含a、b的代数式表示)。
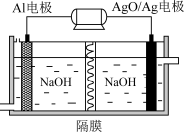
(2)铝电池性能优越,Al—AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为____ 。

(1)一定条件下,NO与NO2存在下列反应:NO(g) + NO2(g)
 N2O3(g),其平衡常数表达式为K =
N2O3(g),其平衡常数表达式为K = (2)吸收时,尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋,好处是
(3)为提高Ca(NO2)2的产率及纯度,则n(NO)∶n(NO2)应控制为
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为
II.铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原—氯化法可实现由铝土矿制备金属铝,相关的热化学方程式如下:
Al2O3(s) + AlCl3(g) + 3C(s) =3AlCl(g) + 3CO(g) △H = a kJ·mol—1
3AlCl (g)=2Al(l) + AlCl3(g) △H = bkJ·mol—1
则Al2O3(s) + 3C(s) =2Al(l) + 3CO(g) △H =
(2)铝电池性能优越,Al—AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组对碳与浓硝酸的反应进行探究,已知:2NaOH+2NO2=NaNO3+NaNO2+H2O,2NaOH+NO2+NO=2NaNO2+H2O。请回答下列可题:
I.甲同学设计 如图所示装置制备并收集NO

(1)碳与浓硝酸反应的化学方程式为__________________ 。
(2)C的作用为_______________ 。
(3)乙同学认为用装置F代替B更合理,理由为_______________ 。
(4)乙同学用改进后的装置进行实验。
①将浓HNO3滴入圆底烧瓶中的操作为__________________ 。
②点燃A处酒精灯开始反应后,圆底烧瓶中的现象为________________ 。
II.探究NO与Na2O2反应

已知NaNO2既有氧化性,又有还原性;J 处硬质玻璃管中制得的NaNO2中含有少量NaNO3。
(5)检验上图装置气密性的方法为____________________ 。
(6)实验结束后,设计实验证明J 处硬质玻璃管中有NaNO2生成________________ 。
供选试剂:蒸馏水KI-淀粉溶液,KMnO4溶液、NaOH溶液.BaCl2溶液、稀硫酸
I.甲同学设计 如图所示装置制备并收集NO

(1)碳与浓硝酸反应的化学方程式为
(2)C的作用为
(3)乙同学认为用装置F代替B更合理,理由为
(4)乙同学用改进后的装置进行实验。
①将浓HNO3滴入圆底烧瓶中的操作为
②点燃A处酒精灯开始反应后,圆底烧瓶中的现象为
II.探究NO与Na2O2反应

已知NaNO2既有氧化性,又有还原性;J 处硬质玻璃管中制得的NaNO2中含有少量NaNO3。
(5)检验上图装置气密性的方法为
(6)实验结束后,设计实验证明J 处硬质玻璃管中有NaNO2生成
供选试剂:蒸馏水KI-淀粉溶液,KMnO4溶液、NaOH溶液.BaCl2溶液、稀硫酸
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①NO+NO2+2OH- = 2NO +H2O;
+H2O;
②气体液化的温度:NO2为21℃,NO为 -152℃。
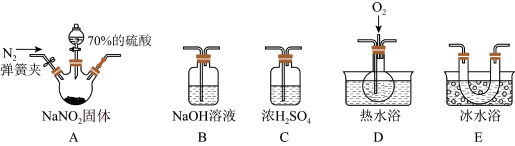
(1)为检验A中生成气体产物,仪器的连接顺序(左→右)为A、___________、___________、___________、B;___________
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是___________ ;
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。确认A中产生的气体含有NO,依据的现象是___________ ;
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为___________ ;
(5)通过上述实验探究过程,可得出装置A中反应的离子方程式是___________ 。
已知:①NO+NO2+2OH- = 2NO
 +H2O;
+H2O;②气体液化的温度:NO2为21℃,NO为 -152℃。

(1)为检验A中生成气体产物,仪器的连接顺序(左→右)为A、___________、___________、___________、B;
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。确认A中产生的气体含有NO,依据的现象是
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为
(5)通过上述实验探究过程,可得出装置A中反应的离子方程式是
您最近一年使用:0次



