Ⅰ.以下是物质的组成I分类以及符号表征,请按要求回答以下问题
(1)相同质量的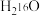 与超重水
与超重水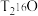 所含中子数之比为
所含中子数之比为___________ 与足量金属钠反应产生的气体在相同状况下的质量比为___________ 。
Ⅱ.下列变化:① 溶于水;②酒精溶于水;③KOH溶于水;④
溶于水;②酒精溶于水;③KOH溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥碘升华;⑦
溶于水;⑥碘升华;⑦ 受热分解;⑧氨气液化;⑨
受热分解;⑧氨气液化;⑨ 熔化;⑩
熔化;⑩ 熔化
熔化
(2)以上变化过程所涉及到的物质中,只含有共价键的是___________ (填相对应的序号,下同),属于共价化合物的是___________ 。
(3)以上变化没有化学键被破坏的是___________ ,只有离子键被破坏的是___________ (填序号)。
(4)⑦中物质的电子式为___________ ,用电子式表示⑧中物质的形成过程___________ 。
(1)相同质量的
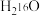 与超重水
与超重水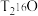 所含中子数之比为
所含中子数之比为Ⅱ.下列变化:①
 溶于水;②酒精溶于水;③KOH溶于水;④
溶于水;②酒精溶于水;③KOH溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥碘升华;⑦
溶于水;⑥碘升华;⑦ 受热分解;⑧氨气液化;⑨
受热分解;⑧氨气液化;⑨ 熔化;⑩
熔化;⑩ 熔化
熔化(2)以上变化过程所涉及到的物质中,只含有共价键的是
(3)以上变化没有化学键被破坏的是
(4)⑦中物质的电子式为
更新时间:2024-04-08 13:44:50
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)1.5mol CH4约含有___________ 个CH4分子,质量为___________ g,标准状况下体积为___________ 升。49 gH2SO4溶于水得到0.5升溶液其物质的量浓度为___________ mol/L。
(2)碳酸钙是___________ (填电解质或非电解质),写出硫酸铝的电离方程式___________ 。
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式为___________ ;用澄清石灰水检验CO2气体的离子方程式是___________ 。
(4)标明下列氧化还原反应MnO2 + 4HCl(浓) MnCl2+Cl2↑+ 2H2O电子转移的方向和数目
MnCl2+Cl2↑+ 2H2O电子转移的方向和数目___________ (标在方程式上),其中MnO2为___________ (填还原剂或氧化剂)。
(1)1.5mol CH4约含有
(2)碳酸钙是
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式为
(4)标明下列氧化还原反应MnO2 + 4HCl(浓)
 MnCl2+Cl2↑+ 2H2O电子转移的方向和数目
MnCl2+Cl2↑+ 2H2O电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题。
(1)下列物质中:
①CO2;②液态氯化氢;③乙醇;④熔融NaOH;⑤NH4Cl固体;⑥氨水。
能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①76g过氧乙酸(CH3COOOH)中含有的C原子数为___________ NA(设NA代表阿伏加德罗常数的值),含有的O原子的物质的量为___________ 。NA 个H2O2分子含有氧原子的物质的量为___________ mol。
②33.3g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为___________ 。
③写出氯气与氢氧化钙反应化学方程式并用双线桥标出电子转移的方向和数目___________ 。
(1)下列物质中:
①CO2;②液态氯化氢;③乙醇;④熔融NaOH;⑤NH4Cl固体;⑥氨水。
能导电的是
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①76g过氧乙酸(CH3COOOH)中含有的C原子数为
②33.3g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为
③写出氯气与氢氧化钙反应化学方程式并用双线桥标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】完成下列问题:
(1) 个氯气分子的物质的量是
个氯气分子的物质的量是___________ , 中含有的电子数为
中含有的电子数为___________ (用 表示)。
表示)。
(2)同温同压下,同体积的甲烷( )和二氧化碳物质的量之比为
)和二氧化碳物质的量之比为___________ ,密度之比为___________ 。
(3)要使 与
与 含相同数目的氢原子,则
含相同数目的氢原子,则 和
和 的质量之比为
的质量之比为___________ 。
(4)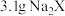 含有
含有 ,则
,则 的摩尔质量为
的摩尔质量为___________ ,X的相对原子质量为___________ 。
(1)
 个氯气分子的物质的量是
个氯气分子的物质的量是 中含有的电子数为
中含有的电子数为 表示)。
表示)。(2)同温同压下,同体积的甲烷(
 )和二氧化碳物质的量之比为
)和二氧化碳物质的量之比为(3)要使
 与
与 含相同数目的氢原子,则
含相同数目的氢原子,则 和
和 的质量之比为
的质量之比为(4)
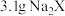 含有
含有 ,则
,则 的摩尔质量为
的摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据所学知识回答下列问题:
(1)将一小块新切的金属钠迅速放入平底烧瓶底部,按图甲所示塞紧瓶塞。过一段时间后可观察到的现象有_______ ,发生反应的化学方程式为_______
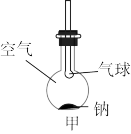
(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。

①能证明钠的密度比水的小的现象是_______
②能证明钠的熔点低的现象是_______
③能证明有氢氧化钠生成的现象是_______
(3)向Na2O2中滴加浓盐酸,试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式,并用单线桥法标出电子转移的方向和数目:_______ ,该反应中被还原的元素是_______ (填元素符号),氧化产物是_______ (填化学式)。
(1)将一小块新切的金属钠迅速放入平底烧瓶底部,按图甲所示塞紧瓶塞。过一段时间后可观察到的现象有

(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。

①能证明钠的密度比水的小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
(3)向Na2O2中滴加浓盐酸,试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求写出方程式:
(1)锌与硫酸的反应的离子方程式:_______
(2)钠与水反应的化学方程式:_______
(3)钠与氯气反应的化学方程式:_______
(4)氯气与氢氧化钠反应的化学方程式:_______
(5)氯气通入水中的化学方程式:_______
(1)锌与硫酸的反应的离子方程式:
(2)钠与水反应的化学方程式:
(3)钠与氯气反应的化学方程式:
(4)氯气与氢氧化钠反应的化学方程式:
(5)氯气通入水中的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】写出下列反应的方程式。
(1)金属钠投入足量水中:_______ 。
(2)金属铝投入足量NaOH溶液中:_______ 。
(3)氯气与石灰乳反应:_______ ;该反应是制取漂白粉的原理,其有效成分是:_______ 。
(4)用氯化铝溶液与氨水反应制取氢氧化铝沉淀:_______ 。
(1)金属钠投入足量水中:
(2)金属铝投入足量NaOH溶液中:
(3)氯气与石灰乳反应:
(4)用氯化铝溶液与氨水反应制取氢氧化铝沉淀:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求完成下列填空:
(1)书写下列物质电子式
①Cl2:______________ ;②CO2:_____________ ;③H2O2:________________ ;
(2)用电子式表示下列物质的形成过程
①MgCl2:___________________________ ;
②H2O:_____________________________ ;
(1)书写下列物质电子式
①Cl2:
(2)用电子式表示下列物质的形成过程
①MgCl2:
②H2O:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】有下列几种物质:①Ne ②NH4Cl ③NaOH ④Cl2 ⑤KNO3⑥CO2 ⑦H202 ⑧Na2O2。属于共价化合物得是______ (填序号,下同),只存在极性键的是______ ,既存在极性键又存在非极性键的是______ ,既存在极性键又存在离子键的是______ ,既存在离子键又存在非极性键的是______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)用电子式表示下列化合物的形成过程:
HClO :_______ ,MgCl2:_______ 。
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是_______ ;只含有非极性键的是_______ ;既含有极性键的是又含有非极性键的是_______ ;只含离子键的是_______ ;⑥含有什么键_______ ;属于离子化合物的是_______ ;属于共价化合物的是_______ 。
(1)用电子式表示下列化合物的形成过程:
HClO :
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下面是同学们熟悉的物质:①O2 ②金刚石 ③NaBr ④H2SO4 ⑤Na2CO3 ⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是___________ (填序号,下同);只含有离子键的是___________ ;既含有共价键又含有离子键的是___________ ;只存在分子间作用力的是___________ 。
(2)属于共价化合物的是___________ ;属于离子化合物的是___________ 。
(3)将NaHSO4溶于水,破坏了NaHSO4中的___________ ,写出其电离方程式:___________ ;NaHSO4在熔融状态下电离,破坏了___________ ,写出其电离方程式:___________ 。
(1)这些物质中,只含有共价键的是
(2)属于共价化合物的是
(3)将NaHSO4溶于水,破坏了NaHSO4中的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下列几种物质:
①MgCl2 ②H2O ③Al ④H2O2 ⑤KCl ⑥Ca(OH)2 ⑦HClO ⑧I2 ⑨He
(1)只含有离子键的是(选填序号,下同)___ 。
(2)含有共价键的离子化合物是___ 。
(3)共价化合物是___ 。
①MgCl2 ②H2O ③Al ④H2O2 ⑤KCl ⑥Ca(OH)2 ⑦HClO ⑧I2 ⑨He
(1)只含有离子键的是(选填序号,下同)
(2)含有共价键的离子化合物是
(3)共价化合物是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下表为元素周期表的一部分,a、b、c……为其中几种元素。回答下列问题:

(1)写出b在元素周期表中的位置___________ ;画出元素f的原子结构示意图___________ 。
(2)元素d和g的气态氢化物中,更稳定的是___________ (写化学式)。
(3)元素d、e、g中原子半径由大到小的顺序为___________ (用元素符号表示)。
(4)元素e、g形成的化合物的电子式为___________ ,所含化学键类型为___________ 。
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:___________ 。

(1)写出b在元素周期表中的位置
(2)元素d和g的气态氢化物中,更稳定的是
(3)元素d、e、g中原子半径由大到小的顺序为
(4)元素e、g形成的化合物的电子式为
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:
您最近一年使用:0次



