表为元素周期表的一部分,a、b、c……为其中几种元素。回答下列问题:
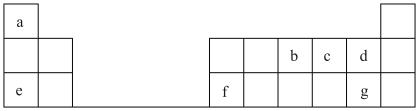
(1)写出b在元素周期表中的位置_______ 。
(2)元素d和g的气态氢化物中,更稳定的是_______ (写化学式)。
(3)元素d、e、g中原子半径由大到小的顺序为_______ (用元素符号表示)。
(4)元素e、g形成的化合物的电子式为_______ ,所含化学键类型为_______ 。
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:_______ 。

(1)写出b在元素周期表中的位置
(2)元素d和g的气态氢化物中,更稳定的是
(3)元素d、e、g中原子半径由大到小的顺序为
(4)元素e、g形成的化合物的电子式为
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:
更新时间:2024-04-10 09:24:52
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】表为元素周期表的一部分。
请回答有关问题:
(1)元素⑥的最高价氧化物对应的水化物为_______ (填名称)。
(2)请写出元素①的简单氢化物的电子式:_______ ,该化合物中存在的化学键类型是_______ (填英文字母)。
A.离子键 B.共价键 C.离子键和共价键
(3)请写出碳元素在周期表中的位置:_______ 。
(4)②、⑥、⑦三种元素的简单氢化物稳定性由强到弱排序为_______ (用化学式及“>”表示)。
(5)元素⑤的单质与元素③最高价氧化物对应的水化物反应的离子方程式为_______ 。
(6)请写出元素⑧的单质与水反应的化学方程式:_______ 。
| I A | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ① | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 4 | ⑧ |
(1)元素⑥的最高价氧化物对应的水化物为
(2)请写出元素①的简单氢化物的电子式:
A.离子键 B.共价键 C.离子键和共价键
(3)请写出碳元素在周期表中的位置:
(4)②、⑥、⑦三种元素的简单氢化物稳定性由强到弱排序为
(5)元素⑤的单质与元素③最高价氧化物对应的水化物反应的离子方程式为
(6)请写出元素⑧的单质与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼 的是:_____ (填元素符号),原子结构示意图为_____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______ ,碱性最强的化合物的电子式 是:_____________ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:________ ,该化合物属于_____ (填 “共价”或“离子”)化合物。
(4)表示①与H的化合物的化学式_________________ ,该化合物是由____________ (填“极性”“非极性”)键形成的。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1)在这些元素中,化学性质
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与H的化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
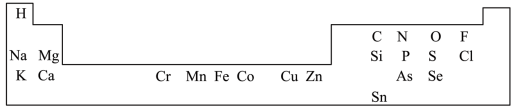
【推荐3】一些元素在周期表中的分布情况如图:___________ 。
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(3)Sn的价电子数为___________ 。
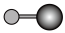
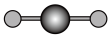
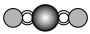
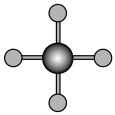
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
(6)用电子式表示 的形成过程
的形成过程___________ 。
(7)在下列物质中:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是___________ ;既存在离子键又存在极性键的是___________ 。
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序
(3)Sn的价电子数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
| A | B | C | D |
 |  |  |  |
|
|
|
|
| 直线形 | 直线形 | 直线形 | 平面正方形 |
| A.A | B.B | C.C | D.D |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
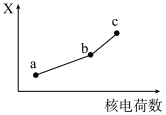
| A.若a、b、c表示ⅠA族金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示ⅦA族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)用电子式表示
 的形成过程
的形成过程(7)在下列物质中:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有部分元素的性质与原子(或分子)结构如下表所示:
(1)画出元素T的原子结构示意图:_________________ 。
(2)元素Y与Z相比金属性较强的是Y,下列不能证明这一事实的是____ (填字母)。
a.Y的最外层电子数比Z少
b.Y单质与水反应比Z单质与水反应剧烈
c.Y最高价氧化物对应的水化物的碱性比Z的强
(3)写出X形成单质的电子式_________________ 。(用元素符号表示)
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-)______ r(Yn+)(填“>”,“<”或“=”)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式___________________________ 。
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 最高正价与最低负价的代数和为2,常温下单质为气体 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的金属离子中半径最小 |
(1)画出元素T的原子结构示意图:
(2)元素Y与Z相比金属性较强的是Y,下列不能证明这一事实的是
a.Y的最外层电子数比Z少
b.Y单质与水反应比Z单质与水反应剧烈
c.Y最高价氧化物对应的水化物的碱性比Z的强
(3)写出X形成单质的电子式
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g分别代表某种化学元素。请依据这7种元素回答下列问题。
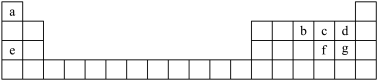
(1)上述7种元素中非金属性最强的是____ (填元素符号,下同)。
(2)由c、f两种元素形成的具有漂白作用的物质,把该物质通入盛有g单质的水溶液中发生反应的离子反应方程式____ 。
(3)g在元素周期表中的位置是____ ,其最高价氧化物为____ 。
(4)e、f、g的离子半径由小到大的顺序是___ 。c、e、g三种元素形成原子个数比为1:1:1的化合物的电子式____ 。
(5)c和f元素对应的气态氢化物的沸点更高的是____ ,原因是____ 。
(6)写出f的最高价氧化物对应的水化物的浓溶液与木炭在加热条件下发生反应的化学方程式____ 。

(1)上述7种元素中非金属性最强的是
(2)由c、f两种元素形成的具有漂白作用的物质,把该物质通入盛有g单质的水溶液中发生反应的离子反应方程式
(3)g在元素周期表中的位置是
(4)e、f、g的离子半径由小到大的顺序是
(5)c和f元素对应的气态氢化物的沸点更高的是
(6)写出f的最高价氧化物对应的水化物的浓溶液与木炭在加热条件下发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素在周期表中的位置反映了元素的原子结构和性质。下图是元素周期表的一部分,请按要求回答下列问题:
(1)元素①位于元素周期表的第_______ 周期第_______ 族,它是形成化合物种类最多的元素。
(2)写出②的元素符号_______ 。
(3)画出元素④的原子结构示意图_______ 。
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是_______ (填化学式)。
(5)比较⑦和⑧的简单离子半径大小_______ >_______ (填离子符号)。
(6)写出元素⑧的单质与水反应的化学方程式:_______ 。
族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)写出②的元素符号
(3)画出元素④的原子结构示意图
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是
(5)比较⑦和⑧的简单离子半径大小
(6)写出元素⑧的单质与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)有下列物质: ①He ②N2 ③CaO ④CH4 ⑤Na2S ⑥KOH ⑦NaHCO3。
回答下列问题(填序号)
其中只含有共价键的是_______ ;只含有离子键的是_______ ;
既含有共价键又含有离子键的是_______ ;属于共价化合物的是_______ ;
属于离子化合物的是_______ ;
(2)下列变化中,不需要破坏化学键的是__________
A.氯化氢溶于水 B.加热氯酸钾使其分解 C.碘升华 D.氯化钠溶于水
回答下列问题(填序号)
其中只含有共价键的是
既含有共价键又含有离子键的是
属于离子化合物的是
(2)下列变化中,不需要破坏化学键的是
A.氯化氢溶于水 B.加热氯酸钾使其分解 C.碘升华 D.氯化钠溶于水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】用①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤MgCl2 ⑥Ar ⑦CO2 ⑧CaF2 ⑨NH4Cl
⑩CaO2 Ca(ClO)2
Ca(ClO)2  N2H4等物质填空。
N2H4等物质填空。
(1)只存在离子键的是________ (2) 由离子键和极性键构成的是_________
(3)由离子键和非极性键构成的是_________ (4) 由极性键和非极性键构成的是_________
(5)写出下列物质的电子式:Na2S2:_________ (NH4)2S:______
(6)写出下列物质的结构式:BCl3:_________ HClO:__________
(7)用电子式写出下列物质的形成过程:MgCl2:___________ 。
⑩CaO2
 Ca(ClO)2
Ca(ClO)2  N2H4等物质填空。
N2H4等物质填空。(1)只存在离子键的是
(3)由离子键和非极性键构成的是
(5)写出下列物质的电子式:Na2S2:
(6)写出下列物质的结构式:BCl3:
(7)用电子式写出下列物质的形成过程:MgCl2:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列几种物质:a.Na2O2b.CH3COOH c.NH4Cld.CO2e. NaOHf.Si。请回答下列问题:
(1)属于共价化合物的是___________ (填写编号,下同);含有非极性共价键的离子化合物是___________ 。
(2)NH4Cl溶于水需要破坏___________ (填写一种作用力名称,下同),干冰升华需要破坏___________ 。
(3)写出 CH3COOH 溶于水的电离方程式___________ 。
(4)试比较 d、e、f 三种晶体的熔点由高到低的顺序:___________ 。(填写编号)
(1)属于共价化合物的是
(2)NH4Cl溶于水需要破坏
(3)写出 CH3COOH 溶于水的电离方程式
(4)试比较 d、e、f 三种晶体的熔点由高到低的顺序:
您最近一年使用:0次