以下有关元素性质的说法正确的是
| A.①Na、K、Rb,②N、P、As,③O、S、Se,④S、P、Cl,元素的电负性依次增大的是④ |
B.某元素气态基态原子的逐级电离能( )分别为738、1451、7733、10540、13630、17995、21703,该元素位于第ⅢA族 )分别为738、1451、7733、10540、13630、17995、21703,该元素位于第ⅢA族 |
C.下列原子中,①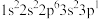 、② 、②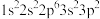 、③ 、③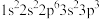 、④ 、④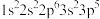 ,对应的第一电离能最大的是④ ,对应的第一电离能最大的是④ |
D.以下原子中,①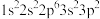 、② 、② 、③ 、③ 、④ 、④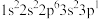 ,半径最大的是① ,半径最大的是① |
更新时间:2024-04-10 15:04:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列各物质或微粒性质的比较中正确的是
| A.离子半径: K+>O2->Al3+>S2->Cl- | B.离于的还原性: S2->Cl->Br->I- |
| C.酸性: HClO>H2SO4>H3PO4>H2SiO3 | D.非金属性: F>O>S |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组物质的性质比较中,正确的是
| A.酸性:HNO3>H2CO3>H2SiO3 |
| B.稳定性;H2S>H2O>HF |
| C.还原性:Cl->Br->I- |
| D.碱性:NaOH>Mg(OH)2>Ca(OH)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】现有四种前20号元素的有关信息如表所示:
下列说法不正确 的是
| 元素 | 相关信息 |
| W | 在前20号元素中,原子半径最大 |
| X | W+与X2-具有相同的电子层结构 |
| Y | 原子最外层电子数是内层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| A.原子半径大小顺序: W > X > Y > Z |
| B.X和Z与氢原子可形成甲、乙两种均为负一价的双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙可发生反应生成水 |
| C.Y与氯气可形成YCl4,该分子中各原子均满足8电子稳定结构 |
| D.W所处的主族中,全部是活泼金属元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于碱金属元素的叙述正确的是
| A.碱金属的密度随着原子序数的递增逐渐减小 |
| B.从上到下,碱金属元素的最高价氧化物对应水化物的碱性依次减弱 |
| C.碱金属元素阳离子的氧化性随着原子序数的递增依次增强 |
| D.钾与氧气或水反应比钠的反应剧烈,铷、铯的相应反应更剧烈 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:原子序数小于18的同一主族的两种元素X和Y,其原子半径:X<Y。下列说法正确的是
| A.若X和Y均位于VIIA,则键能大小为HX<HY |
| B.若X和Y均位于VIA,则H2X分子间易形成氢键 |
| C.若X和Y均位于IVA,则半径Y<X |
| D.若X和Y均位于IIA,则第一电离能大小为X<Y |
您最近一年使用:0次
【推荐2】下列事实的解释错误的是
| 事实 | 解释 | |
| A | 酸性:CH3COOH<CCl3COOH<CF3COOH | H的电负性小于氯原子,氯原子小于氟原子,电负性越强羟基上的氢原子越容易电离,酸性越强 |
| B | 第一电离能: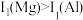 | Mg为3p轨道全空的稳定电子构型,而Al失去一个电子变为3p轨道全空的稳定电子构型 |
| C | O2与O3分子极性相同 | 二者都是由非极性键构成的分子 |
| D | 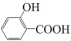 的沸点比 的沸点比 低 低 | 前者形成了分子内氢键,后者形成分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】五种短周期主族元素X、Y、Z、M、Q的原子序数依次增大,X的2p轨道半充满,Y的s能级电子数和p能级电子数相等, Z是至今发现的电负性最大的元素,M在元素周期表中处于周期序数等于族序数的位置,Q的单质被广泛用作半导体材料。下列叙述中不正确的是
| A.元素的第一电离能:X<Y<Z |
| B.气态氢化物的稳定性:X<Y<Z |
| C.气态氢化物分子的键角:Q>X>Y |
| D.最高价氧化物对应的水化物的酸性:X>Q>M |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某有机物在合成中具有重要作用,其分子结构如下图所示。W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、X原子序数之和等于Y的原子序数,Z、Q原子价电子数相同。下列说法错误 的是
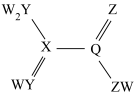

| A.X、Y、Z元素的氢化物沸点最高的是Z |
| B.Y、Z、Q元素电负性最大的是Z |
| C.Q的最高价氧化物是酸性氧化物 |
| D.该有机物既有酸性又有碱性 |
您最近一年使用:0次

 还原
还原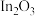
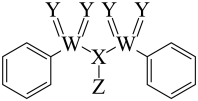
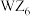 属于非极性分子
属于非极性分子

