MgCl2是制备金属Mg的原料。某研究小组用侯氏制碱法获得的NH4Cl制备MgCl2,同时实现NH3、CO2的循环利用的流程如图所示。
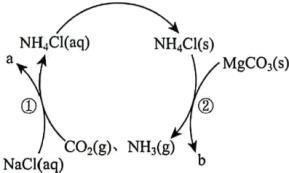
| A.a、b分别是Na2CO3、MgCl2 |
| B.将NH4Cl溶液直接蒸发结晶可以得到NH4Cl固体 |
C.理论上反应①消耗的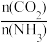 和反应②生成的 和反应②生成的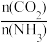 相等 相等 |
D.工业上由MgCl2制Mg的化学方程式:MgCl2(熔融) Mg+Cl2↑ Mg+Cl2↑ |
更新时间:2024-04-15 19:05:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于碳酸钠和碳酸氢钠的比较中,不正确的是
| A.相同温度下,二者在水中的溶解度不同,碳酸氢钠的溶解度小于碳酸钠 |
| B.二者的热稳定性不同,碳酸钠的热稳定性好于碳酸氢钠 |
C.二者等质量时分别和足量盐酸反应,碳酸钠生成 的量多于碳酸氢钠 的量多于碳酸氢钠 |
| D.二者在一定条件下可以相互转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列除杂试剂或方法正确且除杂过程涉及氧化还原反应的是
| 选项 | 物质 括号内为杂质 括号内为杂质 | 除杂试剂或方法 |
| A | NaCl溶液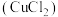 | 过量NaOH溶液、稀盐酸 |
| B |  溶液 溶液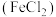 | Cl2 |
| C | 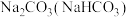 | 加热 |
| D | NH3(H2O) | 浓H2SO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室可由软锰矿(主要成分为 )制备
)制备 方法如下:
方法如下:
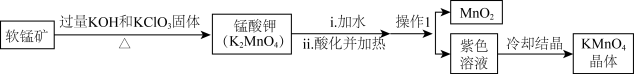
下列说法不正确的是
 )制备
)制备 方法如下:
方法如下:
下列说法不正确的是
A.软锰矿制锰酸钾时, 发生反应转移电子 发生反应转移电子 |
| B.实验室进行“操作1”时,玻璃棒的作用主要是引流 |
C.锰酸钾酸化过程氧化剂和还原剂的物质的量之比为 |
| D.酸化高锰酸钾溶液可用于消毒杀菌 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于Fe3+、Fe2+的说法错误的是( )
| A.用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2 |
| B.配制FeCl3溶液时,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度 |
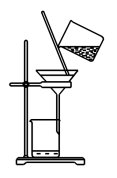
C.用如图装置可以制备Fe(OH)2沉淀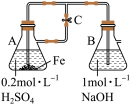 |
| D.向FeCl2溶液中加入少量铁粉是为了防止Fe2+被氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关物质的性质与用途具有对应关系的是
| A.二氧化锰具有较强的氧化性,可作H2O2分解的氧化剂 |
| B.铝能置换出氧化铁中的铁,可用于钢铁工业中大量冶炼铁 |
| C.AlCl3是电解质,可电解熔融AlCl3制铝 |
| D.油脂能在碱性条件下水解,可用于工业上制取肥皂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2008年北京奥运会主体育场——“鸟巢”,被《泰晤士报》评为全球“最强悍”工程。 “鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料。有关说法正确的是


| A.合金的熔点通常比组分金属高,硬度比组分金属小 |
| B.已知Ga处于ⅢA族,可推知氮化镓化学式为Ga3N2 |
| C.用金属铝与V2O5反应冶炼钒,铝作还原剂 |
| D.V原子序数为23,该原子的价电子构型为4s24p1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】海水中蕴含丰富的资源,对海水进行综合利用,可制备一系列物质(见下图),下列说法正确的是( )


| A.步骤①中,除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→盐酸→过滤 |
| B.步骤②中反应利用的原理是:相同条件下NaHCO3的溶解度比NaCl小 |
| C.步骤③在工业上通过向母液中加NaOH固体实现 |
| D.步骤④利用了Br2的挥发性、还原性,该步的作用是富集 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.用激光笔照射硫酸铜溶液,不能观察到“丁达尔效应” |
| B.海水提镁、炼铁、制造玻璃等工业都用到石灰石 |
| C.焰色试验使用的铂丝应用稀硫酸洗涤 |
| D.增味剂味精主要以淀粉为原料通过发酵法生产 |
您最近一年使用:0次

 固体中少量的
固体中少量的 :直接加热
:直接加热 中的
中的 :将混合物在氧气中加热
:将混合物在氧气中加热 气体:通过灼热的铜网
气体:通过灼热的铜网
 、
、 、
、 、
、 、
、 ,它们的原子序数依次增大,其中
,它们的原子序数依次增大,其中 ,
, ,
, ,
,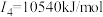 。下列说法正确的是
。下列说法正确的是




 溶液,得到无水
溶液,得到无水

