二氧化氯 常温常压下为气体,是一种高效的消毒剂,也可用于某些污染物的处理。
常温常压下为气体,是一种高效的消毒剂,也可用于某些污染物的处理。
Ⅰ. 的制备:
的制备:
(1)工业上采用亚氯酸钠 溶液和盐酸混合制取
溶液和盐酸混合制取 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
(2)用题图1所示装置进行电解(电极不反应),也可制得 。
。
_______ (填“减小”“增大”或“不变”)。
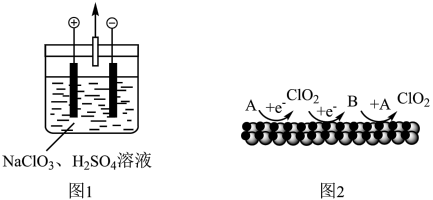
②阴极上产生 的机理如题图2所示(A、B均为含氯微粒,其他微粒未标出)。该机理可描述为
的机理如题图2所示(A、B均为含氯微粒,其他微粒未标出)。该机理可描述为_______ 。
Ⅱ. 的用途:
的用途:
(3) 可用于果蔬保鲜。
可用于果蔬保鲜。 使用时常用稳定剂来吸收、转化。不同稳定剂释放出
使用时常用稳定剂来吸收、转化。不同稳定剂释放出 浓度随时间变化趋势如题图3所示,其中效果较好的稳定剂是
浓度随时间变化趋势如题图3所示,其中效果较好的稳定剂是_______ (填“稳定剂Ⅰ”或“稳定剂Ⅱ”),原因是_______ 。 可用于去除水体中
可用于去除水体中 。某实验小组用弱碱性溶液模拟实际水体消毒过程中
。某实验小组用弱碱性溶液模拟实际水体消毒过程中 和
和 的反应,实验结果发现溶液中有黑色浑浊产生,溶液中微粒浓度变化如题图4所示。
的反应,实验结果发现溶液中有黑色浑浊产生,溶液中微粒浓度变化如题图4所示。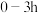 内,发生的主要反应的离子方程式为
内,发生的主要反应的离子方程式为_______ 。
②在 时,耗氯量增幅较大的可能原因是
时,耗氯量增幅较大的可能原因是_______ 。
 常温常压下为气体,是一种高效的消毒剂,也可用于某些污染物的处理。
常温常压下为气体,是一种高效的消毒剂,也可用于某些污染物的处理。Ⅰ.
 的制备:
的制备:(1)工业上采用亚氯酸钠
 溶液和盐酸混合制取
溶液和盐酸混合制取 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)用题图1所示装置进行电解(电极不反应),也可制得
 。
。

②阴极上产生
 的机理如题图2所示(A、B均为含氯微粒,其他微粒未标出)。该机理可描述为
的机理如题图2所示(A、B均为含氯微粒,其他微粒未标出)。该机理可描述为Ⅱ.
 的用途:
的用途:(3)
 可用于果蔬保鲜。
可用于果蔬保鲜。 使用时常用稳定剂来吸收、转化。不同稳定剂释放出
使用时常用稳定剂来吸收、转化。不同稳定剂释放出 浓度随时间变化趋势如题图3所示,其中效果较好的稳定剂是
浓度随时间变化趋势如题图3所示,其中效果较好的稳定剂是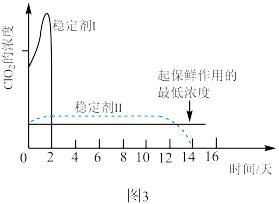
 可用于去除水体中
可用于去除水体中 。某实验小组用弱碱性溶液模拟实际水体消毒过程中
。某实验小组用弱碱性溶液模拟实际水体消毒过程中 和
和 的反应,实验结果发现溶液中有黑色浑浊产生,溶液中微粒浓度变化如题图4所示。
的反应,实验结果发现溶液中有黑色浑浊产生,溶液中微粒浓度变化如题图4所示。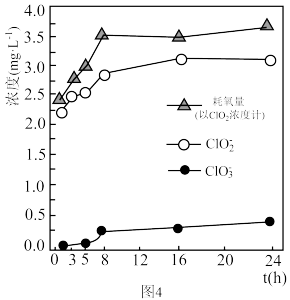
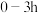 内,发生的主要反应的离子方程式为
内,发生的主要反应的离子方程式为②在
 时,耗氯量增幅较大的可能原因是
时,耗氯量增幅较大的可能原因是
更新时间:2024-04-19 11:12:16
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】我国自主开发的“钛战甲”是一种钛合金材料,为深潜万米的“奋斗者”号建造了世界最大、搭载人数最多的潜水器载人舱球壳。TiCl4是制备钛及其化合物的重要中间体,可利用下列装置在实验室制备TiCl4(夹持装置略去):
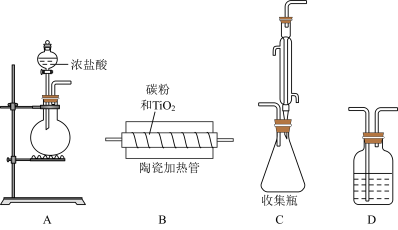
已知:
①TiO2+2C+2Cl2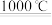 TiCl4+2CO
TiCl4+2CO
②TiCl4为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应
③PdCl2的盐酸溶液可吸收CO而生成黑色颗粒Pd
回答下列问题:
(1)盛放浓盐酸的仪器名称为______ ,圆底烧瓶内所装试剂可为______ (填编号)。
①MnO2 ②KMnO4 ③浓H2SO4
写出其中发生的离子反应方程式______ 。
(2)装置的连接顺序为______ (D装置可重复使用)。
(3)对于实验过程的控制,开始的操作为______ (填①或②),实验结束的操作为_____ (填③或④)。
①先打开分液漏斗活塞,一段时间后,再陶瓷管通电加热
②先陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
③先陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再陶瓷管断电停止加热
(4)装置C左边进气的细长导管作用为______ 。
(5)吸收尾气中CO的的化学方程式_____ 。
(6)所得的TiCl4可用Mg制Ti,该过程可在______ 气氛围保护下进行 (填编号) 。
①氮气 ②氧气 ③水蒸气 ④氩气

已知:
①TiO2+2C+2Cl2
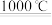 TiCl4+2CO
TiCl4+2CO②TiCl4为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应
③PdCl2的盐酸溶液可吸收CO而生成黑色颗粒Pd
回答下列问题:
(1)盛放浓盐酸的仪器名称为
①MnO2 ②KMnO4 ③浓H2SO4
写出其中发生的离子反应方程式
(2)装置的连接顺序为
(3)对于实验过程的控制,开始的操作为
①先打开分液漏斗活塞,一段时间后,再陶瓷管通电加热
②先陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
③先陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再陶瓷管断电停止加热
(4)装置C左边进气的细长导管作用为
(5)吸收尾气中CO的的化学方程式
(6)所得的TiCl4可用Mg制Ti,该过程可在
①氮气 ②氧气 ③水蒸气 ④氩气
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】钠、镁、铝的单质及其化合物是中学阶段重点研究的物成。
(1)按性质分类,Na2O2____________ (填“属于”或“不属于”)碱性氧化物。
(2)用离子方程式说明Al(OH)3是两性氢氧化物:____________________ 。
(3)某同学用如图所示装置进行实验探究有关钠、镁、铝的化合物的性质(夹持仪器省略)。将液体A遂满加入到固体B中,回答下列问题:
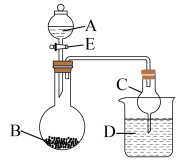
①若A为70%硫酸溶液,B为Na2SO3,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中发生反应的化学方程式为________________________ 。
②若A为水,B为Mg3N2,C中盛有AlC13溶液,旋开E,足够长的时间后,C中发生反应的离子方程式为__________________________ 。
③若A为浓盐酸,B为NaClO3,C中盛有KI-淀粉溶液,旋开E后,C中的现象是________________ ,继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3,写出该反应的化学方程式: _______________ 。
(1)按性质分类,Na2O2
(2)用离子方程式说明Al(OH)3是两性氢氧化物:
(3)某同学用如图所示装置进行实验探究有关钠、镁、铝的化合物的性质(夹持仪器省略)。将液体A遂满加入到固体B中,回答下列问题:

①若A为70%硫酸溶液,B为Na2SO3,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中发生反应的化学方程式为
②若A为水,B为Mg3N2,C中盛有AlC13溶液,旋开E,足够长的时间后,C中发生反应的离子方程式为
③若A为浓盐酸,B为NaClO3,C中盛有KI-淀粉溶液,旋开E后,C中的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种高效且多功能的新型绿色净水剂,一种以Mn、Fe及MnO2制备高铁酸钾和重要的催化剂MnO2的流程如下图所示:
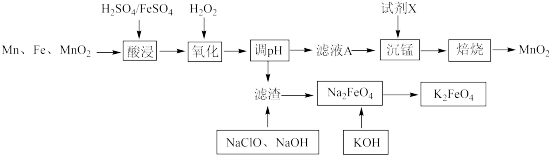
已知:部分金属离子在溶液中沉淀的pH见下表。

回答下列问题:
(1)酸浸的目的是在酸性条件下 将
将 还原成稳定的
还原成稳定的 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
(2)调节pH的范围是_______ ,由滤渣生成 的离子方程式为
的离子方程式为_______ 。
(3)已知试剂X为 ,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是
,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是_______ ,若用 替代试剂X,沉锰得到的固体混合物中可能会混有
替代试剂X,沉锰得到的固体混合物中可能会混有_______ 杂质。
(4)某温度下,若要从 含
含 的循环母液中沉淀
的循环母液中沉淀 (浓度降至
(浓度降至 ),理论上需加入
),理论上需加入 固体的物质的量不少于
固体的物质的量不少于_______ mol。(已知该温度下 的
的 ,不考虑水解和溶液体积变化)
,不考虑水解和溶液体积变化)
(5)在水处理中, 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是
胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是_______ 。

已知:部分金属离子在溶液中沉淀的pH见下表。
| 金属离子 |  |  |  |
| 开始沉淀的pH | 1.9 | 7.0 | 8.1 |
| 完全沉淀的pH | 3.2 | 9.0 | 10.1 |

回答下列问题:
(1)酸浸的目的是在酸性条件下
 将
将 还原成稳定的
还原成稳定的 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(2)调节pH的范围是
 的离子方程式为
的离子方程式为(3)已知试剂X为
 ,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是
,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是 替代试剂X,沉锰得到的固体混合物中可能会混有
替代试剂X,沉锰得到的固体混合物中可能会混有(4)某温度下,若要从
 含
含 的循环母液中沉淀
的循环母液中沉淀 (浓度降至
(浓度降至 ),理论上需加入
),理论上需加入 固体的物质的量不少于
固体的物质的量不少于 的
的 ,不考虑水解和溶液体积变化)
,不考虑水解和溶液体积变化)(5)在水处理中,
 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是
胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素。
(1)氯原子结构示意图是______________ ,碘在元素周期表中的位置是____________ ,HI的稳定性比HBr________ (填写“强”或“弱”)。
(2)向浓缩的海水中通入Cl2,可将Br-转化为Br2。再用“空气吹出法” 将Br2从浓海水中吹出,并用纯碱浓溶液吸收,生成NaBr、NaBrO3等。当有1 mol Br2被纯碱吸收时,转移的电子数为____________ 。
下图是NaClO的发生装置。该装置主要利用了电解饱和食盐水的原理,可实现对海水的消毒和灭藻。
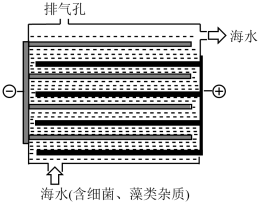
(3)写出装置中产生NaClO的化学方程式___________ 。海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH) 2和CaCO3。 生成CaCO3的离子方程式是_________________ 。若每隔5-10 min倒换一次电极电性,可有效地解决阴极的结垢问题。试用电极反应式并结合必要的文字进行解释___________ 。
NaOH溶液吸收SO2得Na2SO3,可用Na2SO3吸收SO2。在SO2被吸收的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下:
(4)从上表可判断,NaHSO3溶液呈_____ (填“酸性”、“碱性”、“中性”),请用平衡原理解释:__________________ 。
(5)当吸收液呈中性时,溶液中离子浓度关系正确的是_________ (选填字母)。
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
d.c(Na+)>c(SO32-)>c(HSO3-)>c(H+)=c(OH-)
(1)氯原子结构示意图是
(2)向浓缩的海水中通入Cl2,可将Br-转化为Br2。再用“空气吹出法” 将Br2从浓海水中吹出,并用纯碱浓溶液吸收,生成NaBr、NaBrO3等。当有1 mol Br2被纯碱吸收时,转移的电子数为
下图是NaClO的发生装置。该装置主要利用了电解饱和食盐水的原理,可实现对海水的消毒和灭藻。

(3)写出装置中产生NaClO的化学方程式
NaOH溶液吸收SO2得Na2SO3,可用Na2SO3吸收SO2。在SO2被吸收的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
(5)当吸收液呈中性时,溶液中离子浓度关系正确的是
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
d.c(Na+)>c(SO32-)>c(HSO3-)>c(H+)=c(OH-)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:
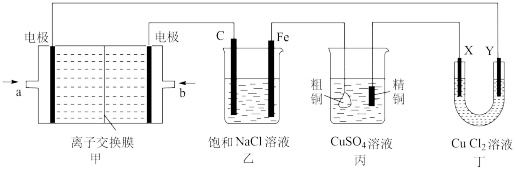
(1)甲装置是甲烷燃料电池(电解质溶液为KOH 溶液)的结构示意图,则a处通入的是___________ (填CH4”或“O2),电极上发生的电板反应是 ___________ 。
(2)在乙装置中,总反应的离子方程式是___________ 。
(3)如果两装置中精铜电极的质量增加了6.4g,则甲装置中消耗的CH4的质量为___________ 。
(4)丁装置中在通电一段时间后,Y电极上发生的电极反应是___________ 。
(5)若将乙装置单独拿出并用导线将两电极相接,则C电极上发生的电极反应为___________ 。

(1)甲装置是甲烷燃料电池(电解质溶液为KOH 溶液)的结构示意图,则a处通入的是
(2)在乙装置中,总反应的离子方程式是
(3)如果两装置中精铜电极的质量增加了6.4g,则甲装置中消耗的CH4的质量为
(4)丁装置中在通电一段时间后,Y电极上发生的电极反应是
(5)若将乙装置单独拿出并用导线将两电极相接,则C电极上发生的电极反应为
您最近一年使用:0次
【推荐3】二氧化氯(ClO2)是高效、广谱、快速、安全的杀菌消毒剂,被认为是“第四代消毒剂”。电解法是目前最为热门的生产ClO2的方法之一。直接电解氯酸钠(NaClO3)溶液自动催化循环制备高纯ClO2的实验装置示意图如图所示。
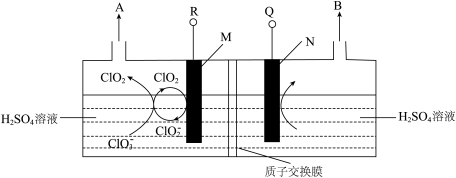
回答下列问题(不考虑H+放电):
(1)亚氯酸根离子( )中氯元素的化合价为
)中氯元素的化合价为________ 价。NaClO3在水中的电离方程式为________________ 。
(2)已知铅酸蓄电池的工作原理为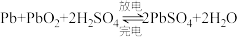
①电解氯酸钠溶液时,M电极上发生________ (填“氧化”或“还原”)反应。
②电解氯酸钠溶液时,若以铅酸蓄电池作为电源,则R应与________ (填“Pb”或“PbO2”)电极相连,N电极上的电极反应式为________________ 。
(3)亚氯酸盐具有较强氧化性。可以用ClO2与H2O2和NaOH溶液反应制备NaClO2,制备时的化学方程式为________ 。反应每消耗2.24 L标准状况下的ClO2气体,可生成气体物质的质量为________ 。若要除去水中超标的亚氯酸盐,下列物质最适宜的是________ (填标号)。
A.明矾 B.氯化钾 C.盐酸 D.硫酸亚铁
(4)由图示信息等,可以判断下列说法错误的是________(填标号)。

回答下列问题(不考虑H+放电):
(1)亚氯酸根离子(
 )中氯元素的化合价为
)中氯元素的化合价为(2)已知铅酸蓄电池的工作原理为
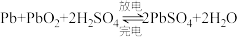
①电解氯酸钠溶液时,M电极上发生
②电解氯酸钠溶液时,若以铅酸蓄电池作为电源,则R应与
(3)亚氯酸盐具有较强氧化性。可以用ClO2与H2O2和NaOH溶液反应制备NaClO2,制备时的化学方程式为
A.明矾 B.氯化钾 C.盐酸 D.硫酸亚铁
(4)由图示信息等,可以判断下列说法错误的是________(填标号)。
| A.氯酸钠与硫酸溶液反应可以产生ClO2 | B. 促进了 促进了 ,转化成为ClO2 ,转化成为ClO2 |
| C.电解进行时,M极的电势高于N极 | D.电解时, 穿过质子交换膜移向M极 穿过质子交换膜移向M极 |
您最近一年使用:0次



