氯的化合物在生活中有着广泛的用途。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生Cl-和少量的 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为Cl-除去。
转化为Cl-除去。
①关于二氧化氯的说法不正确的是_______ 。
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去 的离子方程式为
的离子方程式为_______ 。
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为:ClO2+H2O2+NaOH=NaClO2+O2+H2O(未配平)。
①ClO2的氧化性_______ H2O2的氧化性(填“大于”或“小于”)。
②为测定产品中NaClO2的纯度,进行如下实验:准确称取1.000g上述产品,溶于水配成100.00mL溶液,取10.00mL待测液,加入过量KI溶液,酸性条件下发生反应: +4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2
+4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2 =2I-+
=2I-+ )。计算该样品的纯度为
)。计算该样品的纯度为_______ 。(写出计算过程)
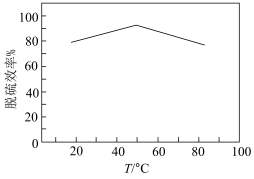
③工业上常用NaClO2溶液对燃煤烟气进行脱硫。已知NaClO2溶液具有强氧化性,酸性条件下NaClO2发生歧化反应生成ClO2,ClO2易溶于水,具有强氧化性,可氧化SO2.在实验室模拟脱硫过程:先加稀硫酸调节NaClO2吸收液的pH为5,再向其中通入含SO2的模拟烟气。测得脱硫反应后,溶液中的阴离子为Cl-,则SO2的氧化产物是_______ 。测得脱硫效率(即SO2的吸收率)随温度变化的曲线如下图所示。_______ 。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生Cl-和少量的
 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为Cl-除去。
转化为Cl-除去。①关于二氧化氯的说法不正确的是
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去
 的离子方程式为
的离子方程式为(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为:ClO2+H2O2+NaOH=NaClO2+O2+H2O(未配平)。
①ClO2的氧化性
②为测定产品中NaClO2的纯度,进行如下实验:准确称取1.000g上述产品,溶于水配成100.00mL溶液,取10.00mL待测液,加入过量KI溶液,酸性条件下发生反应:
 +4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2
+4I-+4H+=2H2O+2I2+Cl-,杂质不与I-反应。以淀粉作指示剂,再加入0.2000mol/LNa2S2O3溶液,恰好完全反应时消耗的Na2S2O3溶液的体积为20.00mL。(已知:I2+2 =2I-+
=2I-+ )。计算该样品的纯度为
)。计算该样品的纯度为③工业上常用NaClO2溶液对燃煤烟气进行脱硫。已知NaClO2溶液具有强氧化性,酸性条件下NaClO2发生歧化反应生成ClO2,ClO2易溶于水,具有强氧化性,可氧化SO2.在实验室模拟脱硫过程:先加稀硫酸调节NaClO2吸收液的pH为5,再向其中通入含SO2的模拟烟气。测得脱硫反应后,溶液中的阴离子为Cl-,则SO2的氧化产物是
更新时间:2024-04-25 21:47:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】乳酸亚铁 常用作缺铁性贫血的补铁剂,能溶于水。
常用作缺铁性贫血的补铁剂,能溶于水。
(1)一般由乳酸钙与氯化亚铁两水溶液混合制得,通过重结晶提纯。
①写出制备乳酸亚铁的离子方程式___________ 。
②1mol乳酸亚铁受热至75℃和170℃时失水,失水质量分别为___________ g、___________ g。
③画出乳酸亚铁的空间立体结构___________ 。
(2)乳酸亚铁还原性的检验
①取乳酸亚铁溶于水,加入酸性高锰酸钾溶液,搅拌后紫色慢慢褪去,溶液变成棕黄色。1mol乳酸亚铁消耗了0.2mol ,化学方程式为
,化学方程式为___________ 。
②1mol乳酸亚铁溶液与5%的双氧水反应,反应剧烈且消耗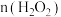 大于1.5mol。控制反应速率后,多次实验,发现消耗
大于1.5mol。控制反应速率后,多次实验,发现消耗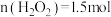 。消耗
。消耗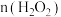 大于1.5mol的原因:
大于1.5mol的原因:___________ 、___________ 。
③双氧水与乳酸亚铁的反应速率远大于酸性高锰酸钾,为了进一步探寻原因,实验设计如下:___________ 。
 常用作缺铁性贫血的补铁剂,能溶于水。
常用作缺铁性贫血的补铁剂,能溶于水。(1)一般由乳酸钙与氯化亚铁两水溶液混合制得,通过重结晶提纯。
①写出制备乳酸亚铁的离子方程式
②1mol乳酸亚铁受热至75℃和170℃时失水,失水质量分别为
③画出乳酸亚铁的空间立体结构
(2)乳酸亚铁还原性的检验
①取乳酸亚铁溶于水,加入酸性高锰酸钾溶液,搅拌后紫色慢慢褪去,溶液变成棕黄色。1mol乳酸亚铁消耗了0.2mol
 ,化学方程式为
,化学方程式为②1mol乳酸亚铁溶液与5%的双氧水反应,反应剧烈且消耗
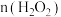 大于1.5mol。控制反应速率后,多次实验,发现消耗
大于1.5mol。控制反应速率后,多次实验,发现消耗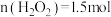 。消耗
。消耗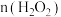 大于1.5mol的原因:
大于1.5mol的原因:③双氧水与乳酸亚铁的反应速率远大于酸性高锰酸钾,为了进一步探寻原因,实验设计如下:
您最近半年使用:0次
【推荐2】将25.02克绿矾溶于硫酸中,加入3.03克KNO3恰好将其中的亚铁离子全部反应。
(1)该反应的氧化剂是___________ 。反应中硫酸的作用是___________ 。
(2)该反应的还原产物是___________ 。
(3)写出该反应的化学方程式________________________________________________ 。
(4)当有1.01克KNO3完全反应则生成的还原产物为_______ 升(标准状态)。转移的电子为_______ mol。
(1)该反应的氧化剂是
(2)该反应的还原产物是
(3)写出该反应的化学方程式
(4)当有1.01克KNO3完全反应则生成的还原产物为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】运用所学知识,回答下列问题。
I、向硫酸铜溶液中逐滴加入KI溶液至恰好反应完全,观察到产生白色沉淀CuI,蓝色溶液变为棕色。该反应的离子方程式为__________ ;取一定量上述反应后的上层棕色清液于一支试管中,加入一定量的苯,振荡,此时观察到的现象是________ 。
II、工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

回答下列问题:
(1)上述反应是否都是氧化还原反应_________ (填“是”或“否”);写出反应①的化学方程式_____ 。
(2)反应①后过滤的沉淀为_______ ,简述确定此物质中金属元素及其价态的操作过程_______ 。
I、向硫酸铜溶液中逐滴加入KI溶液至恰好反应完全,观察到产生白色沉淀CuI,蓝色溶液变为棕色。该反应的离子方程式为
II、工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

回答下列问题:
(1)上述反应是否都是氧化还原反应
(2)反应①后过滤的沉淀为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁是人类利用最为广泛的金属之一,工业炼铁一般用一氧化碳作还原剂。
(1)已知Fe2O3在高炉中有下列反应:Fe2O3+CO 2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是
2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是_________ 。
a.7:3 b.21: 8 c.14: 5 d.7:2
(2)若m(Fe):m(O)=3:1,则Fe2O3与FeO的物质的量之比为_________ ,Fe2O3被CO还原的物质的量分数为____________ 。
(3)3.04 g Fe2O3和FeO的混合固体粉末在加热条件下用足量CO使金属氧化物完全还原,生成的CO2气体通入含0.04 mol Ca(OH)2的澄清石灰水后,产生3.00 g白色沉淀。计算固体粉末中Fe2O3的质量。(保留1位小数)____________
(4)常温下,称取不同铁锈样品溶入足量盐酸,向溶液中加入足量NaOH溶液生成沉淀,然后过滤、洗涤、灼烧,得到Fe2O3固体,实验过程中产品无损失。
实验数据记录如下:
上述实验①②③④所用铁锈均不含杂质,且实验数据可靠。通过计算,分析和比较上表4组数据,给出结论。_______________
(1)已知Fe2O3在高炉中有下列反应:Fe2O3+CO
 2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是
2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是a.7:3 b.21: 8 c.14: 5 d.7:2
(2)若m(Fe):m(O)=3:1,则Fe2O3与FeO的物质的量之比为
(3)3.04 g Fe2O3和FeO的混合固体粉末在加热条件下用足量CO使金属氧化物完全还原,生成的CO2气体通入含0.04 mol Ca(OH)2的澄清石灰水后,产生3.00 g白色沉淀。计算固体粉末中Fe2O3的质量。(保留1位小数)
(4)常温下,称取不同铁锈样品溶入足量盐酸,向溶液中加入足量NaOH溶液生成沉淀,然后过滤、洗涤、灼烧,得到Fe2O3固体,实验过程中产品无损失。
实验数据记录如下:
实验序号 | 铁锈质量/g | 氧化铁质量/g |
① | 0.856 | 0.640 |
② | 1.424 | 1.280 |
③ | 0.979 | 0.880 |
④ | 1.070 | 0.800 |
上述实验①②③④所用铁锈均不含杂质,且实验数据可靠。通过计算,分析和比较上表4组数据,给出结论。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学工业为疫情防控提供了强有力的物质支撑。次氯酸钠和二氧化氯(分子式为ClO2,其中Cl元素的化合价为+4价)在水处理等方面有广泛应用,是一种高效安全的灭菌消毒剂。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为_______ ;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是_______ 。
(2)ClO2的制备方法,有下列两种:
方法Ⅰ:2NaClO3 + 4HCl =2ClO2↑ + Cl2↑+ 2NaCl + 2H2O
方法Ⅱ:2NaClO3 + H2O2 +H2SO4 = 2ClO2↑ + O2↑+ Na2SO4 +2H2O
方法Ⅰ反应中,氧化产物为_______ (填化学式);方法Ⅱ反应中,产生1mol ClO2气体,电子转移_______ mol。
(3)将ClO2溶于水得到溶液,为测定其浓度,进行以下实验操作:
步骤1 取待测ClO2溶液20.00mL于锥形瓶中;
步骤2 用稀硫酸调节溶液至酸性,加入足量的KI晶体充分反应,使ClO2转化为Cl-;发生的反应为:4ClO2 + 20 KI +8H2SO4=4KCl +10I2 + 8 X + 8H2O
步骤3 逐滴加入0.1500mol·L-1的Na2S2O3溶液,发生的反应为:I2 + 2Na2S2O3= Na2S4O6 +2NaI,当将步骤2中反应生成的I2恰好完全反应时,消耗Na2S2O3溶液的体积为24.00mL。
①写出步骤2反应方程式中的X的化学式为_______ ;
②计算:ClO2溶液的物质的量浓度为_______ mol·L-1(写出计算过程)。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为
(2)ClO2的制备方法,有下列两种:
方法Ⅰ:2NaClO3 + 4HCl =2ClO2↑ + Cl2↑+ 2NaCl + 2H2O
方法Ⅱ:2NaClO3 + H2O2 +H2SO4 = 2ClO2↑ + O2↑+ Na2SO4 +2H2O
方法Ⅰ反应中,氧化产物为
(3)将ClO2溶于水得到溶液,为测定其浓度,进行以下实验操作:
步骤1 取待测ClO2溶液20.00mL于锥形瓶中;
步骤2 用稀硫酸调节溶液至酸性,加入足量的KI晶体充分反应,使ClO2转化为Cl-;发生的反应为:4ClO2 + 20 KI +8H2SO4=4KCl +10I2 + 8 X + 8H2O
步骤3 逐滴加入0.1500mol·L-1的Na2S2O3溶液,发生的反应为:I2 + 2Na2S2O3= Na2S4O6 +2NaI,当将步骤2中反应生成的I2恰好完全反应时,消耗Na2S2O3溶液的体积为24.00mL。
①写出步骤2反应方程式中的X的化学式为
②计算:ClO2溶液的物质的量浓度为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)向Ba(HCO3)2溶液中滴加少量的NaOH溶液,请写出发生反应的离子方程式:________________________________________ ;在以上溶液中继续滴加NaOH溶液至过量,请写出此步反应的离子方程式:______________________________ 。
(2)在氯化钾与氯化钙的混和物中,钾离子与钙离子的物质的量之比为1∶2,则该混合物中KCl的质量分数为________ ;含有1mol氯离子的该混合物的质量为_____________ 。
(2)在氯化钾与氯化钙的混和物中,钾离子与钙离子的物质的量之比为1∶2,则该混合物中KCl的质量分数为
您最近半年使用:0次



