将25.02克绿矾溶于硫酸中,加入3.03克KNO3恰好将其中的亚铁离子全部反应。
(1)该反应的氧化剂是___________ 。反应中硫酸的作用是___________ 。
(2)该反应的还原产物是___________ 。
(3)写出该反应的化学方程式________________________________________________ 。
(4)当有1.01克KNO3完全反应则生成的还原产物为_______ 升(标准状态)。转移的电子为_______ mol。
(1)该反应的氧化剂是
(2)该反应的还原产物是
(3)写出该反应的化学方程式
(4)当有1.01克KNO3完全反应则生成的还原产物为
2011·上海·零模 查看更多[1]
(已下线)上海中学、复旦附中等八校2011届高三联合调研化学试题
更新时间:2020-03-31 14:18:56
|
相似题推荐
【推荐1】如下图为铁及其化合物的“价一类"二维图。
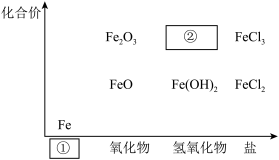
(1)填写二维图缺失的类别①______ 和化学式②______ 。
(2)某同学利用以下试剂(①Cl2②Fe③NaOH④H2SO4⑤AgNO3)
研究FeCl3性质、进行了如下预测:
从物质类别上看,FeCl3属于______ ,可能与______ 发生复分解反应(填上述试剂对应的序号)。
从化合价角度看,Fe3+具有______ 性,可能与______ 发生氧化还原反应(填上述试剂对应的序号)。
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应: Cu+2FeCl3=CuCl2+2FeCl2该反应的离子方程式为______ 。
(4)为了探究Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如图所示。请回答:

实验Ⅰ、Ⅱ的现象和结论如下表:
①实验Ⅰ的现象为______ 。
②实验Ⅱ的结论为______ 。
③实验Ⅱ中的AgNO3完全反应后,抽出铜丝,洗净后干燥、称重,发现铜丝比反应前增重7.6g,则反应转移的电子为______ mol。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂(①Cl2②Fe③NaOH④H2SO4⑤AgNO3)
研究FeCl3性质、进行了如下预测:
从物质类别上看,FeCl3属于
从化合价角度看,Fe3+具有
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应: Cu+2FeCl3=CuCl2+2FeCl2该反应的离子方程式为
(4)为了探究Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如图所示。请回答:

实验Ⅰ、Ⅱ的现象和结论如下表:
| 实验编号 | 实验现象 | 实验结论 |
| Ⅰ | ① | 氧化性:Cu2+>Fe2+ |
| Ⅱ | 溶液变蓝色 | ② |
②实验Ⅱ的结论为
③实验Ⅱ中的AgNO3完全反应后,抽出铜丝,洗净后干燥、称重,发现铜丝比反应前增重7.6g,则反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】木炭与浓硫酸反应可表示为:C +2H2SO4(浓) CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(1)木炭作_____ (填“氧化剂”或“还原剂”),硫酸______ (填“被氧化”或“被还原”)。
(2)若消耗了1 mol H2SO4,则生成_____ mol SO2。
 CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。(1)木炭作
(2)若消耗了1 mol H2SO4,则生成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铜是生物必需的微量元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。
(1)写出铜与稀硝酸反应的化学方程式_____________________________ 。
(2)为了保护环境和节约资源,通常先用 和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式
和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式__________________________ 。
(3)工业上以黄铜矿为原料,采用火法溶炼工艺生产铜,该工艺的中间过程会发生反应: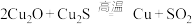 ,该反应的氧化剂是
,该反应的氧化剂是________ ;当生成 时,反应中转移的电子为
时,反应中转移的电子为______  。
。
(4)研究性学习小组用“间接碘量法”测定某试样中 (不含能与I-反应的氧化性杂质)的含量,取
(不含能与I-反应的氧化性杂质)的含量,取 试样配成
试样配成 溶液,每次取
溶液,每次取 ,滴加
,滴加 溶液后有白色碘化物沉淀生成,写出该反应的离子方程式
溶液后有白色碘化物沉淀生成,写出该反应的离子方程式__________________________ 。
(5)继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫化硫酸钠标准溶液滴定,发生反应的化学方程式为: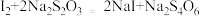 ,平均消耗
,平均消耗 的
的 溶液
溶液 。则试样中
。则试样中 的质量分数为
的质量分数为______________________ 。
(1)写出铜与稀硝酸反应的化学方程式
(2)为了保护环境和节约资源,通常先用
 和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式
和稀硫酸的混合溶液溶出废旧卬刷电路板中的铜,最终实现铜的回收利用,写出溶出铜的离子方程式(3)工业上以黄铜矿为原料,采用火法溶炼工艺生产铜,该工艺的中间过程会发生反应:
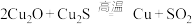 ,该反应的氧化剂是
,该反应的氧化剂是 时,反应中转移的电子为
时,反应中转移的电子为 。
。(4)研究性学习小组用“间接碘量法”测定某试样中
 (不含能与I-反应的氧化性杂质)的含量,取
(不含能与I-反应的氧化性杂质)的含量,取 试样配成
试样配成 溶液,每次取
溶液,每次取 ,滴加
,滴加 溶液后有白色碘化物沉淀生成,写出该反应的离子方程式
溶液后有白色碘化物沉淀生成,写出该反应的离子方程式(5)继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫化硫酸钠标准溶液滴定,发生反应的化学方程式为:
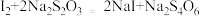 ,平均消耗
,平均消耗 的
的 溶液
溶液 。则试样中
。则试样中 的质量分数为
的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】“84”消毒液的主要成分为NaClO,“洁厕灵”的有效成分为浓盐酸,家庭室内切不可将两者混合使用,因为:NaClO + 2HCl(浓) =NaCl + A↑ + H2O(已配平),某兴趣小组在化学实验室的通风橱内探究上述反应,请回答下列问题:
(1)A的名称为__________ 。NaClO对应的酸性氧化物的化学式为______ 。
(2)上述反应中的五种物质,其中属于电解质的有______________________ (至少写出三种化学式 ),依据盐对应的酸碱强弱程度,可将盐分为四类;
A.强酸强碱盐; B.强碱弱酸盐; C.强酸弱碱盐; D.弱酸弱碱盐;
则上述反应中生成的NaClO属于________ 类,NaCl属于________ 类(用字母代号填空)。
(3)为吸收实验结束后的有毒尾气,可向反应废液中加入______________ (填化学式),若要收集纯净、干燥的氯气,可先后将气体通入装有_________ 的洗气瓶洗气(用字母代号填空)。
A.饱和食盐水、石灰乳 B. 浓硫酸、饱和食盐水
C. 饱和食盐水、浓硫酸 D. 饱和碳酸钠、浓硫酸
(4)为增强消毒液的消毒效果,可向消毒液中加入适量的稀盐酸,用离子方程式表示其反应的原理:________ 。该反应说明稀盐酸和浓盐酸在性质上________________ (填“相同”或“不同”)。
(1)A的名称为
(2)上述反应中的五种物质,其中属于电解质的有
A.强酸强碱盐; B.强碱弱酸盐; C.强酸弱碱盐; D.弱酸弱碱盐;
则上述反应中生成的NaClO属于
(3)为吸收实验结束后的有毒尾气,可向反应废液中加入
A.饱和食盐水、石灰乳 B. 浓硫酸、饱和食盐水
C. 饱和食盐水、浓硫酸 D. 饱和碳酸钠、浓硫酸
(4)为增强消毒液的消毒效果,可向消毒液中加入适量的稀盐酸,用离子方程式表示其反应的原理:
您最近一年使用:0次
【推荐2】已知氧化性:BrO3->IO3->Br2>I2。向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加KBrO3的物质的量的关系如图所示。请回答下列问题:

(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为__ ,还原产物是__ 。
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式___ 。
(3)①已知反应:2BrO3-+I2→2IO3-+Br2;有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___ ,并说明理由:___ 。
(4)计算c→d过程中消耗KBrO3的物质的量___ 。(写出计算过程)

(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式
(3)①已知反应:2BrO3-+I2→2IO3-+Br2;有同学由此得出氧化性:I2>Br2的结论,你认为是否正确
(4)计算c→d过程中消耗KBrO3的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.完成下列问题
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
(2)工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性(填“氧化”或者“还原”)。下列不能实现上述转化的物质是___________ 。
A. B.
B. C.
C. D.
D.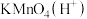
(3)在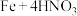 (稀)
(稀) 的反应中,若
的反应中,若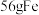 参加反应时,被还原的
参加反应时,被还原的 为
为___________ g。
Ⅱ.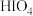 主要以
主要以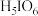 形式存在,
形式存在,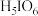 是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化
是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化 。
。
(4)请完成并配平下列离子反应。________
 ___________
___________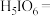 ___________
___________ ___________
___________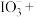 ___________
___________ ___________
___________
(5)根据以上离子方程式判断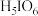 是
是___________ 酸(填“强”或“弱”)。
(6)上述反应,被氧化的元素是___________ (填元素符号)。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
(2)工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有A.
 B.
B. C.
C. D.
D.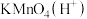
(3)在
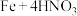 (稀)
(稀) 的反应中,若
的反应中,若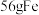 参加反应时,被还原的
参加反应时,被还原的 为
为Ⅱ.
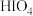 主要以
主要以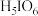 形式存在,
形式存在,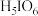 是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化
是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化 。
。(4)请完成并配平下列离子反应。
 ___________
___________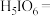 ___________
___________ ___________
___________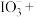 ___________
___________ ___________
___________(5)根据以上离子方程式判断
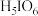 是
是(6)上述反应,被氧化的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】用双线桥标出下面反应的电子转移方向和数目_____ ,并按要求回答问题:6NaOH+3Cl2 NaClO3+5NaCl+3H2O,氧化剂是
NaClO3+5NaCl+3H2O,氧化剂是___ ;氧化产物是___ ;氧化剂与还原剂的物质的量之比为___ 。
 NaClO3+5NaCl+3H2O,氧化剂是
NaClO3+5NaCl+3H2O,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空。
(1)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体 ,请写出该过程的离子方程式:
,请写出该过程的离子方程式:_______ 。
(2)某无色溶液中的溶质可能由下列离子组成: 、
、 、
、 、
、 、
、 、
、 、
、 ,某同学为检验其成分,进行了如下实验:
,某同学为检验其成分,进行了如下实验:
①向适量原溶液中加入过量的稀盐酸,有无色气体a和无色溶液b生成;
②向无色溶液b中加入过量的 溶液,有白色沉淀c生成,过滤,得滤液d;
溶液,有白色沉淀c生成,过滤,得滤液d;
③取少量滤液d,加入过量的稀硝酸酸化,再滴加 溶液,有白色沉淀e生成。
溶液,有白色沉淀e生成。
依据以上实验可以推断,原溶液中一定含有大量的_______ (用离子符号表示,下同);可能含有_______ 。
(3) 常用作补铁剂,在酸性(常用稀硫酸酸化)条件下,
常用作补铁剂,在酸性(常用稀硫酸酸化)条件下, 能将
能将 中
中 价的Cr转化为
价的Cr转化为 价的Cr。则反应中氧化剂与还原剂的物质的量之比为
价的Cr。则反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)某一反应体系中反应物和生成物共有六种物质: 、
、 、
、 、NaCl、NaOH、
、NaCl、NaOH、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程: ,则该反应的化学方程式为
,则该反应的化学方程式为_______ 。
(5)向 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 的物质的量与所加盐酸体积之间的关系如图所示。
的物质的量与所加盐酸体积之间的关系如图所示。

①盐酸的物质的量浓度为_______  。
。
②当滴入盐酸的体积为12.5mL时,溶液中 为
为_______ 。
(1)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体
 ,请写出该过程的离子方程式:
,请写出该过程的离子方程式:(2)某无色溶液中的溶质可能由下列离子组成:
 、
、 、
、 、
、 、
、 、
、 、
、 ,某同学为检验其成分,进行了如下实验:
,某同学为检验其成分,进行了如下实验:①向适量原溶液中加入过量的稀盐酸,有无色气体a和无色溶液b生成;
②向无色溶液b中加入过量的
 溶液,有白色沉淀c生成,过滤,得滤液d;
溶液,有白色沉淀c生成,过滤,得滤液d;③取少量滤液d,加入过量的稀硝酸酸化,再滴加
 溶液,有白色沉淀e生成。
溶液,有白色沉淀e生成。依据以上实验可以推断,原溶液中一定含有大量的
(3)
 常用作补铁剂,在酸性(常用稀硫酸酸化)条件下,
常用作补铁剂,在酸性(常用稀硫酸酸化)条件下, 能将
能将 中
中 价的Cr转化为
价的Cr转化为 价的Cr。则反应中氧化剂与还原剂的物质的量之比为
价的Cr。则反应中氧化剂与还原剂的物质的量之比为(4)某一反应体系中反应物和生成物共有六种物质:
 、
、 、
、 、NaCl、NaOH、
、NaCl、NaOH、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程: ,则该反应的化学方程式为
,则该反应的化学方程式为(5)向
 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 的物质的量与所加盐酸体积之间的关系如图所示。
的物质的量与所加盐酸体积之间的关系如图所示。
①盐酸的物质的量浓度为
 。
。②当滴入盐酸的体积为12.5mL时,溶液中
 为
为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有一稀硫酸和稀硝酸的混合溶液,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合液,向其中加入过量的铁粉:
反应过程中发生的离子反应方程式:_______________ ;____________
产生的气体的总体积为______ L。
反应过程中发生的离子反应方程式:
产生的气体的总体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】向含Fe(NO3)3、Cu(NO3)2、HNO3的稀溶液中逐渐加入铁粉,c(Fe2+)的变化如图所示。

(1)横坐标0~1段反应的离子方程式为:____________________ 。
(2)忽略溶液体积的变化,则原溶液c( )为
)为___________________ 。

(1)横坐标0~1段反应的离子方程式为:
(2)忽略溶液体积的变化,则原溶液c(
 )为
)为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在浓硝酸中放入铜片:
(1)开始反应的化学方程式为____ ,实验现象为____ ;该反应生成的气体溶于水发生反应的化学方程式是____ 。
(2)若铜有剩余,则反应将要结束时的反应方程式为____ 。
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,发生反应的离子方程式是____ 。
(4)若将12.8g铜跟一定量的浓硝酸反应,铜消耗完时,共产生5.6L(标准状况)气体。则所消耗的HNO3的物质的量为____ ,反应中表现氧化性的硝酸的物质的量为____ 。
(1)开始反应的化学方程式为
(2)若铜有剩余,则反应将要结束时的反应方程式为
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,发生反应的离子方程式是
(4)若将12.8g铜跟一定量的浓硝酸反应,铜消耗完时,共产生5.6L(标准状况)气体。则所消耗的HNO3的物质的量为
您最近一年使用:0次

 的质量是
的质量是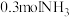 分子在标准状况下的体积
分子在标准状况下的体积 溶液中
溶液中 中氢原子的数目
中氢原子的数目 反应中氧化剂和还原剂物质的量之比
反应中氧化剂和还原剂物质的量之比

