用双线桥标出下面反应的电子转移方向和数目_____ ,并按要求回答问题:6NaOH+3Cl2 NaClO3+5NaCl+3H2O,氧化剂是
NaClO3+5NaCl+3H2O,氧化剂是___ ;氧化产物是___ ;氧化剂与还原剂的物质的量之比为___ 。
 NaClO3+5NaCl+3H2O,氧化剂是
NaClO3+5NaCl+3H2O,氧化剂是
更新时间:2021-05-01 13:02:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:3C+2K2Cr2O7 +8H2SO4===3CO2↑+2K2SO4
+2Cr2(SO4)3 +8H2O。
(1)请用双线桥法标出电子转移方向和数目________________________________ 。
(2)上述反应中氧化剂是______ (填化学式),被氧化的元素是________ (填元素符号)。
(3)H2SO4 在上述反应中表现出来的性质是____________ (填序号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_________ L。
+2Cr2(SO4)3 +8H2O。
(1)请用双线桥法标出电子转移方向和数目
(2)上述反应中氧化剂是
(3)H2SO4 在上述反应中表现出来的性质是
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)已知实验室制备NO的反应为:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑ + 4H2O。
①反应中氧化剂是_______ ; 被氧化的元素是_______ ;氧化产物是_______ 。
②若有2 g NO生成,有_______ g HNO3被还原。
(2)请配平下列方程式,并用双线桥法标出下列反应电子转移的方向和数目_______ 。
_______Al +_______NaNO3 + _______NaOH= _______NaAlO2 + _______N2↑ + _______H2O
(3)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2 → O2。
①该反应中的氧化剂是_______
②写出该反应的化学方程式_______
(1)已知实验室制备NO的反应为:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑ + 4H2O。
①反应中氧化剂是
②若有2 g NO生成,有
(2)请配平下列方程式,并用双线桥法标出下列反应电子转移的方向和数目
_______Al +_______NaNO3 + _______NaOH= _______NaAlO2 + _______N2↑ + _______H2O
(3)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2 → O2。
①该反应中的氧化剂是
②写出该反应的化学方程式
您最近半年使用:0次
【推荐3】把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:______________ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式:_____________________ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为
②配平该反应的方程式:
您最近半年使用:0次
【推荐1】SiO2、KNO3能与分解出的金属钠发生反应生成Na2SiO3,化学方程式为: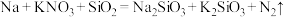 (未配平)
(未配平)
(1)配平化学方程式,并用单线桥法标出电子转移的方向和数目。
___________Na+___________ KNO3+___________ SiO2=___________Na2SiO3+___________K2SiO3+___________N2↑___________
(2)在该反应中KNO3体现___________ (填“氧化性”或“还原性”),Na2SiO3为___________ (填“氧化产物”或“还原产物”)。
(3)当反应转移5mol电子时,生成标准状况下的氮气___________ L。
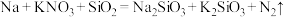 (未配平)
(未配平)(1)配平化学方程式,并用单线桥法标出电子转移的方向和数目。
___________Na+___________ KNO3+___________ SiO2=___________Na2SiO3+___________K2SiO3+___________N2↑
(2)在该反应中KNO3体现
(3)当反应转移5mol电子时,生成标准状况下的氮气
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】汽车安全气囊的药剂含有NaN3、Fe2O3、KClO4、NaHCO3等。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热,N2使气囊迅速膨胀,从而起到保护作用。
(1)KClO4中氯元素的化合价是_________ ,因此具有_________ (填“还原性”或“氧化性”)。
(2)Fe2O3可处理产生的Na,反应为:6Na+Fe2O3=3Na2O+2Fe,请用单线桥 表示电子转移的方向和数目______________________ 。
(3)NaHCO3具有_________ 的性质,可用于吸收产气过程中释放的热量。
(1)KClO4中氯元素的化合价是
(2)Fe2O3可处理产生的Na,反应为:6Na+Fe2O3=3Na2O+2Fe,请用
(3)NaHCO3具有
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)实验室制备氧气可以用加热氯酸钾的方法实现,其发生的反应为2KClO3 2KCl+O2↑,其中被氧化的元素是
2KCl+O2↑,其中被氧化的元素是_______ (填元素符号),还原产物是_______ (填化学式)。
(2)下列反应方程式:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是_______ (填写化学式),若反应中发生氧化反应的HCl个数为12,反应中转移的电子数为_______
(3)根据化学反应MnO2+HCl(浓) MnCl2+Cl2 ↑+H2O(未配平),回答下列有关问题:
MnCl2+Cl2 ↑+H2O(未配平),回答下列有关问题:
①该反应的离子方程式为_______ (已知浓HCl可拆分为H+和Cl-)
②反应中氧化产物和还原产物的个数比_______
③用双线桥表示电子得失_______
(1)实验室制备氧气可以用加热氯酸钾的方法实现,其发生的反应为2KClO3
 2KCl+O2↑,其中被氧化的元素是
2KCl+O2↑,其中被氧化的元素是(2)下列反应方程式:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
(3)根据化学反应MnO2+HCl(浓)
 MnCl2+Cl2 ↑+H2O(未配平),回答下列有关问题:
MnCl2+Cl2 ↑+H2O(未配平),回答下列有关问题:①该反应的离子方程式为
②反应中氧化产物和还原产物的个数比
③用双线桥表示电子得失
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属切削加工废液中含有2%~5%的亚硝酸钠( )。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。
)。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。
(1)写出亚硝酸钠和氯化铵反应的化学方程式_________ 。
(2)第二步反应中,1mol亚硝酸铵完全分解,共有_________ mol电子转移。
 )。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。
)。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。(1)写出亚硝酸钠和氯化铵反应的化学方程式
(2)第二步反应中,1mol亚硝酸铵完全分解,共有
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与生产、生活、环境息息相关。从化学视角回答下列问题:
(1)我国科学家研发了一种室温下“可呼吸”的Na—CO2充电电池。电池的总反应为:3CO2+4Na=2Na2CO3+C,该电池中不能存在水,否则可能引起电池爆炸,用离子方程式表示其原因_______ ;
(2)亚硝酸钠被称为工业盐,有毒,但在肉类制品加工中又可以加入极少量用作发色剂、防微生物剂、防腐剂,在漂白、电镀和金属处理等方面有应用。已知NaNO2能发生反应:_______NaNO2+_______HI→_______NO↑+_______I2+_______NaI+_______H2O
①配平并写出上述化学方程式_______ ;
②该反应中HI表现的性质是_______ ;氧化剂与还原剂的个数之比为_______ 。
(1)我国科学家研发了一种室温下“可呼吸”的Na—CO2充电电池。电池的总反应为:3CO2+4Na=2Na2CO3+C,该电池中不能存在水,否则可能引起电池爆炸,用离子方程式表示其原因
(2)亚硝酸钠被称为工业盐,有毒,但在肉类制品加工中又可以加入极少量用作发色剂、防微生物剂、防腐剂,在漂白、电镀和金属处理等方面有应用。已知NaNO2能发生反应:_______NaNO2+_______HI→_______NO↑+_______I2+_______NaI+_______H2O
①配平并写出上述化学方程式
②该反应中HI表现的性质是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】氰化钠广泛用于电镀、金的提取及有机合成中,含氰废水属于高毒类,必须对其进行处理。
(1)向NaCN溶液中通入CO2能发生反应:NaCN+H2O+CO2=HCN+NaHCO3。说明酸性:HCN___ (填“>”或“<”)H2CO3。
(2)含CN-浓度较低的废水可直接用FeSO4 ▪7H2O处理,得到一种蓝色沉淀M,M的摩尔质量为324 g • mol-1,则M的化学式为_______ 。
(3)pH在7.5〜10之间用铜作催化剂的条件下,用SO2-空气处理含氰废水会生成NH3、碳酸氢盐及硫酸盐,已知参与反应的SO2与O2的物质的量之比为1:1,则该反应的离子方程式为___________ 。
(4)工业上常用碱性氯化法处理含氰废水,其原理如下:
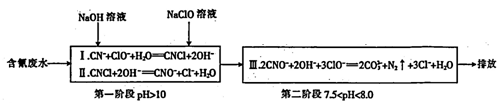
①第一阶段的中间体CNC1中碳元素的化合价为________ 。
②某工厂含氰废水中NaCN的含量为147 mg • L-1,处理10m3这样的废水,理论上需要5 mol • L-1的NaClO 溶液_______ L。
(1)向NaCN溶液中通入CO2能发生反应:NaCN+H2O+CO2=HCN+NaHCO3。说明酸性:HCN
(2)含CN-浓度较低的废水可直接用FeSO4 ▪7H2O处理,得到一种蓝色沉淀M,M的摩尔质量为324 g • mol-1,则M的化学式为
(3)pH在7.5〜10之间用铜作催化剂的条件下,用SO2-空气处理含氰废水会生成NH3、碳酸氢盐及硫酸盐,已知参与反应的SO2与O2的物质的量之比为1:1,则该反应的离子方程式为
(4)工业上常用碱性氯化法处理含氰废水,其原理如下:

①第一阶段的中间体CNC1中碳元素的化合价为
②某工厂含氰废水中NaCN的含量为147 mg • L-1,处理10m3这样的废水,理论上需要5 mol • L-1的NaClO 溶液
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】钠和钠的化合物有许多重要的用途,碳酸钠可与氯气发生反应,涉及的反应如下: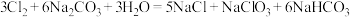
(1)用双线桥法标出电子转移的方向和数目_______________ 。
(2)该反应的离子方程式为___________________ 。
(3)该反应中氧化剂与还原剂的个数之比是_________ ,若1个 被氧化时,转移的电子是
被氧化时,转移的电子是_________ 个。
(4)少量的钠应保存在_____ 中;钠着火时应采取的灭火措施是_________ ,不能用水灭火,原因是_________________  涉及反应的离子方程式
涉及反应的离子方程式 。
。
(5)在实验室配制好的NaOH溶液中通入过量的二氧化碳时发生的离子反应是______ 。
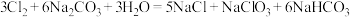
(1)用双线桥法标出电子转移的方向和数目
(2)该反应的离子方程式为
(3)该反应中氧化剂与还原剂的个数之比是
 被氧化时,转移的电子是
被氧化时,转移的电子是(4)少量的钠应保存在
 涉及反应的离子方程式
涉及反应的离子方程式 。
。(5)在实验室配制好的NaOH溶液中通入过量的二氧化碳时发生的离子反应是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)已知2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O,该反应中,氧化剂是_______ ,氧化产物是_____ 。若生成氯气11.2L(标准状况),则转移电子的物质的量为_____ mol。
(2)配置0.2mol/L的NaCl溶液450mL, 需要用到的仪器有托盘天平(含砝码)、药匙、烧杯、玻璃棒、_____________ 和_________ ,需要用托盘天平称取NaCl__________ g。
(3)漂白粉的有效成分是_______________
(4)已知每1 克氢气完全燃烧生成水蒸气时将放出121kJ热量,写出该反应的热化学方程式___________________________________________
(2)配置0.2mol/L的NaCl溶液450mL, 需要用到的仪器有托盘天平(含砝码)、药匙、烧杯、玻璃棒、
(3)漂白粉的有效成分是
(4)已知每1 克氢气完全燃烧生成水蒸气时将放出121kJ热量,写出该反应的热化学方程式
您最近半年使用:0次



