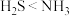在溶液中用光照射 催化剂产生光电子和空穴
催化剂产生光电子和空穴 ,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是
,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是
 催化剂产生光电子和空穴
催化剂产生光电子和空穴 ,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是
,可以在常温常压下使甲烷转化为甲醇和氢气,其反应机理如图所示(部分产物和步骤未标出)。下列说法错误的是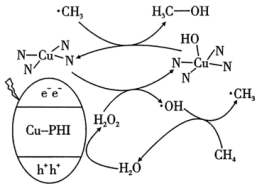
A.空穴 参与发生的反应为 参与发生的反应为 |
| B.反应过程中有非极性键的生成,没有非极性键的断裂 |
| C.生成的甲醇因能与水形成分子间氢键而易溶于水 |
D.该反应的化学方程式为 |
更新时间:2024-04-28 20:15:42
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】新型纳米材料氧缺位铁酸盐(MFe2Ox),能使SO2、NO2等氧化物转化为单质。转化流程如图所示,下列有关该转化过程的叙述不正确的是
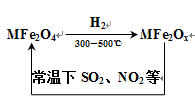
| A.MFe2O4表现了氧化性 |
| B.若MFe2Ox与SO2发生反应的物质的量之比为3:1,则x=10/3 |
| C.在处理该废气过程中,每处理含1molNO2的废气转移电子数4NA个 |
| D.MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列反应的离子方程式正确的是
A. 与 与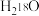 反应: 反应: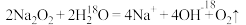 |
B.用 溶液吸收废气中的 溶液吸收废气中的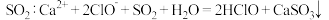 |
C. 与稀硝酸反应:当 与稀硝酸反应:当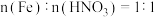 时, 时, |
D. 溶液与少量 溶液与少量 溶液反应: 溶液反应: |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】根据表中信息,判断下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A.表中①组的反应只可能有一种元素被氧化和一种元素被还原 |
| B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2 |
| C.由表中①②组反应推测:ClO3-、Br-、H+、Fe2+不能在浓溶液中大量共存 |
| D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2+ 6H+=2Mn2++ 4O2↑+ 6H2O |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中Z、Q在同一周期。相关信息如表:
下列说法正确的是
| 元素 | 相关信息 |
| X | 最外层电子数是核外电子总数的一半 |
| Y | 最高化合价和最低化合价之和为零 |
| Z | 最外层电子数与最内层电子数之和等于次外层电子数 |
| Q | 同周期元素中原子半径最小 |
| A.常温时,X单质能与水发生剧烈反应 |
B.Y与Q元素组成的 分子中只含极性共价键 分子中只含极性共价键 |
| C.Y、Z、Q最高价氧化物对应水化物的酸性依次减弱 |
| D.第五周期且与Q同主族元素的单质在常温常压下呈液态 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】焦炭是重要的工业原料,用作冶金、燃料、制电石、制硅等,2C +SiO2 Si +2CO↑,3C +CaO
Si +2CO↑,3C +CaO CaC2 +CO↑。设NA是阿伏加德罗常数的值,下列说法正确的是
CaC2 +CO↑。设NA是阿伏加德罗常数的值,下列说法正确的是
 Si +2CO↑,3C +CaO
Si +2CO↑,3C +CaO CaC2 +CO↑。设NA是阿伏加德罗常数的值,下列说法正确的是
CaC2 +CO↑。设NA是阿伏加德罗常数的值,下列说法正确的是| A.常温常压下,11.2L CO含有的分子数小于0.5NA |
| B.64g CaC2含有阴阳离子总数为3NA |
| C.若12g焦炭参加反应,以上两个反应中焦炭均失去2NA个电子 |
| D.lmol SiO2晶体含有共价键数目为2NA |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe、Sm、As、F、O组成的化合物。下列说法正确的是
| A.元素As与N同族,可预测AsH3分子中As-H键间的键角大于NH3中N-H键间的键角 |
| B.NH3的水溶液中存在不同的氢键,其中根据氨水显碱性可以推测NH3和H2O间存在的主要氢键形式可能为(NH3)N…H-O(H2O) |
| C.配合物Fe(CO)n可用作催化剂,Fe(CO)n内中心原子价电子数与配位体提供电子总数之和为18,则n=4 |
| D.每个H2O分子最多可与两个H2O分子形成两个氢键 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】液氨是一种很好的溶剂,液氨可以微弱的电离产生NH 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 的说法正确的是
的说法正确的是
 和NH
和NH 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成NH2OH(羟胺)。在有NH 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成N2、NO、NO2、N2O4(无色)、HNO3等。下列有关NH2OH、NH3、NH 、NO
、NO 的说法正确的是
的说法正确的是| A.NH2OH难溶于水 | B.NO 的空间构型为直线形 的空间构型为直线形 |
C.NH3的键角比NH 中的大 中的大 | D.[Cu(NH3)4]2+中提供孤电子对的原子是Cu |
您最近半年使用:0次

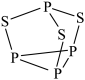
 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是