元素周期律是自然科学的基本规律,也是无机化学的基础.下图为现代元素周期表的一部分,请回答下列问题:
(1)⑤和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;
(2)③、④、⑥、⑧的简单离子半径由大到小依次为___________ (用离子符号表示);
(3)由②的最低负价氢化物与最高正价氧化物的水化物反应所生成的物质中,所含化学键类型有:___________ 、___________ ;
(4)元素①②③④形成的简单气态氢化物的稳定性由弱到强的顺序排列为:___________ (用化学式表示)。
(5)某盐由③⑤⑦三种元素组成,向其水溶液中通入少量二氧化碳气体,出现白色胶状沉淀,写出该反应的离子方程式__________________________________ ;
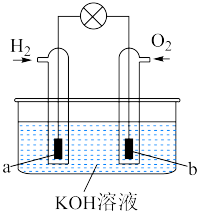
(6)氢气和③的单质可以作为燃料电池的两个电极反应气体,其装置如图所示_____ 极(填“正”或“负”),该电极上发生________ 反应(填“氧化”或“还原”);b极发生的电极反应方程式是__________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ||||||||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
(1)⑤和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
(2)③、④、⑥、⑧的简单离子半径由大到小依次为
(3)由②的最低负价氢化物与最高正价氧化物的水化物反应所生成的物质中,所含化学键类型有:
(4)元素①②③④形成的简单气态氢化物的稳定性由弱到强的顺序排列为:
(5)某盐由③⑤⑦三种元素组成,向其水溶液中通入少量二氧化碳气体,出现白色胶状沉淀,写出该反应的离子方程式
(6)氢气和③的单质可以作为燃料电池的两个电极反应气体,其装置如图所示
更新时间:2024-04-30 05:28:36
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
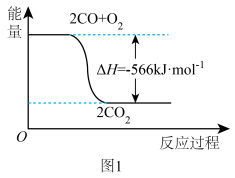
(1)已知常温下 转化成
转化成 的能量关系如图
的能量关系如图 所示。写出该反应的热化学方程式:
所示。写出该反应的热化学方程式:_______ 。
(2) 和
和 混合可作火箭推进剂,已知:
混合可作火箭推进剂,已知: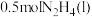 和足量氧气反应生成
和足量氧气反应生成 和
和 ,放出310.6kJ的热量;
,放出310.6kJ的热量;
 。
。
①反应 的
的
_______  。
。
② 和
和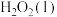 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
③将上述反应设计成原电池如图 所示,
所示, 溶液作为电解质溶液。
溶液作为电解质溶液。
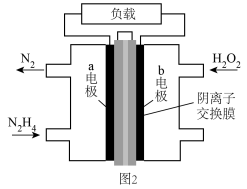
 极电极反应式为
极电极反应式为_______
(3)实验室用 盐酸与
盐酸与 某浓度的
某浓度的 溶液在如图
溶液在如图 所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。
所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。
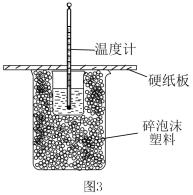
①该装置缺少一种玻璃仪器,该仪器的名称为_______ 。
②实验室提供了 和
和 两种浓度的
两种浓度的 溶液,应最好选择
溶液,应最好选择_______  的
的 溶液进行实验。
溶液进行实验。
③在测定中和反应的反应热的实验中,下列叙述正确的是_______ 。
A.测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度
B.中和反应的试验中,应快速将NaOH溶液一次倒入盛盐酸的小烧杯中
C.可以用氢氧化钾代替氢氧化钠,浓硫酸代替稀盐酸
D.在测定中和反应的反应热实验中,每完成一次反应热热测定,至少需要读三次温度。
(1)已知常温下
 转化成
转化成 的能量关系如图
的能量关系如图 所示。写出该反应的热化学方程式:
所示。写出该反应的热化学方程式:
(2)
 和
和 混合可作火箭推进剂,已知:
混合可作火箭推进剂,已知: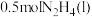 和足量氧气反应生成
和足量氧气反应生成 和
和 ,放出310.6kJ的热量;
,放出310.6kJ的热量;
 。
。①反应
 的
的
 。
。②
 和
和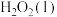 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为③将上述反应设计成原电池如图
 所示,
所示, 溶液作为电解质溶液。
溶液作为电解质溶液。
 极电极反应式为
极电极反应式为(3)实验室用
 盐酸与
盐酸与 某浓度的
某浓度的 溶液在如图
溶液在如图 所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。
所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。
①该装置缺少一种玻璃仪器,该仪器的名称为
②实验室提供了
 和
和 两种浓度的
两种浓度的 溶液,应最好选择
溶液,应最好选择 的
的 溶液进行实验。
溶液进行实验。③在测定中和反应的反应热的实验中,下列叙述正确的是
A.测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度
B.中和反应的试验中,应快速将NaOH溶液一次倒入盛盐酸的小烧杯中
C.可以用氢氧化钾代替氢氧化钠,浓硫酸代替稀盐酸
D.在测定中和反应的反应热实验中,每完成一次反应热热测定,至少需要读三次温度。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】文献表明:工业上,向炽热铁屑中通入HCl生产无水FeCl2;相同条件下,草酸根(C2O42-)的还原性强于Fe2+。某化学研究性小组进行以下实验检验这一结论并测定三草酸合铁酸钾晶体[K3Fe(C2O4)3・xH2O]中草酸根含量和结晶水含量。用如图所示装置制取无水FeCl2

(1)仪器a的名称为____ ,B中的试剂为________ 。
(2)欲制得纯净的FeCl2,实验过程需先点燃A处酒精灯,原因是________ 。
(3)若用D的装置进行尾气处理,存在的问题是________ 、________ 。
(4)某小组设计使用如图装置直接比较Fe2+和C2O42-的还原性强弱,并达到了预期的目的。
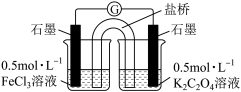
左池石墨电极为___ 极,写出右池电极反应式:________ 。
(5)为测定三草酸合铁酸钾晶体中草酸根的含量和结晶水的含量,进行了如下实验:
滴定过程:①称量mg三草酸合铁酸钾晶体样品,配制成250mL溶液
②取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO4溶液滴定,恰好消耗VmLamol•L-1KMnO4溶液。C2O42-被全部转化的现象是___ 。
③该晶体中C2O42-的质量分数为___ 。
误差分析:若盛放酸性KMnO4溶液的滴定管未用标准液润洗,会使结晶水x的数值___ 。(填“偏高”“偏低”“无影响”)

(1)仪器a的名称为
(2)欲制得纯净的FeCl2,实验过程需先点燃A处酒精灯,原因是
(3)若用D的装置进行尾气处理,存在的问题是
(4)某小组设计使用如图装置直接比较Fe2+和C2O42-的还原性强弱,并达到了预期的目的。

左池石墨电极为
(5)为测定三草酸合铁酸钾晶体中草酸根的含量和结晶水的含量,进行了如下实验:
滴定过程:①称量mg三草酸合铁酸钾晶体样品,配制成250mL溶液
②取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO4溶液滴定,恰好消耗VmLamol•L-1KMnO4溶液。C2O42-被全部转化的现象是
③该晶体中C2O42-的质量分数为
误差分析:若盛放酸性KMnO4溶液的滴定管未用标准液润洗,会使结晶水x的数值
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
I.空间站是以水为介质将不同形式的能量相互转化。原理如图所示。装置x为电解水,装置y为燃料电池。

(1)太阳能电池的能量转化形式为_______ (填字母)。
A.化学能转化为电能 B.电能转化为化学能 C.太阳能转化为电能
(2)装置x工作时,产生O2的电极为_____ 极(填“阳”或“阴”)。
(3)装置y工作时,若电解质溶液为稀硫酸,则正极反应式为______ 。
II.氢能的利用包括氢的制备、储存和应用三个环节。
(4)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:_______ 。
(5)化工生产的副产物也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH- FeO
FeO +3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
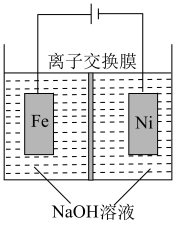
①电解一段时间后,c(OH—)降低的区域在______ (填“阴极室”或“阳极室”)。
②电解过程中,需将阴极产生的气体及时排出,其原因是______ 。
I.空间站是以水为介质将不同形式的能量相互转化。原理如图所示。装置x为电解水,装置y为燃料电池。

(1)太阳能电池的能量转化形式为
A.化学能转化为电能 B.电能转化为化学能 C.太阳能转化为电能
(2)装置x工作时,产生O2的电极为
(3)装置y工作时,若电解质溶液为稀硫酸,则正极反应式为
II.氢能的利用包括氢的制备、储存和应用三个环节。
(4)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:
(5)化工生产的副产物也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH-
 FeO
FeO +3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
①电解一段时间后,c(OH—)降低的区域在
②电解过程中,需将阴极产生的气体及时排出,其原因是
您最近半年使用:0次
【推荐1】研究化学反应的原理,对掌握物质的应用有重要的意义。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如图所示:
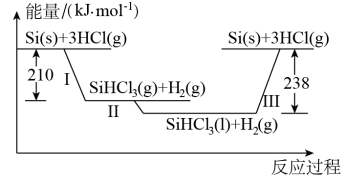
①反应Ⅰ的热化学方程式为___________ 。
②反应Ⅲ为___________ (选填“吸热”或“放热”)反应。
(2)氢氧燃料电池具有清洁高效等优点,简易装置如图所示。
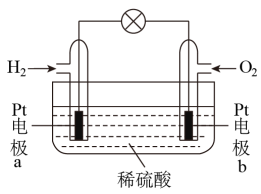
该电池的负极为___________ (选填“a”或“b”),电池工作过程中,电子的流向为___________ ,电池的总反应为___________ 。
(3)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
实验原理: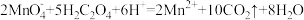
①探究实验中,提供6mol/L  的酸是
的酸是___________ (填化学式)。
②实验3中,V=___________ 。
③根据上表中的实验数据,可以得到的结论是___________ 。
④利用实验1中数据计算,用 的浓度变化表示的平均反应速率:
的浓度变化表示的平均反应速率:
___________  。
。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如图所示:

①反应Ⅰ的热化学方程式为
②反应Ⅲ为
(2)氢氧燃料电池具有清洁高效等优点,简易装置如图所示。

该电池的负极为
(3)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
实验原理:
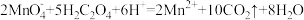
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液颜色褪至无色所需时间 | |||
0.6mol/L  溶液 溶液 |  | 0.2mol/L  溶液 溶液 | 6mol/L  | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | V | 1.0 | 2.0 | 6.4 |
 的酸是
的酸是②实验3中,V=
③根据上表中的实验数据,可以得到的结论是
④利用实验1中数据计算,用
 的浓度变化表示的平均反应速率:
的浓度变化表示的平均反应速率:
 。
。
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】(1)汽车尾气是城市空气污染的一个重要因素,一种CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,在高温熔融状态下能传导O2-(过程中无气体产生),则负极的反应式为___ 。
(2)以上述电池为电源,通过导线连接成图一电解池。
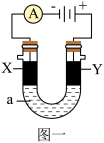
①若X、Y为石墨,a为2L0.1mol/LKCl溶液,写出电解总反应的离子方程式___ 。
②若X、Y分别为铜、银,a为1L0.2mol/LAgNO3溶液,写出Y电极反应式___ 。
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图二(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。
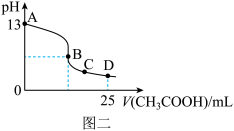
①结合图二计算,上述电解过程中消耗一氧化碳的质量为___ g。
②若图二的B点pH=7,则滴定终点在___ 区间(填“AB”、“BC”或“CD”)。
(2)以上述电池为电源,通过导线连接成图一电解池。

①若X、Y为石墨,a为2L0.1mol/LKCl溶液,写出电解总反应的离子方程式
②若X、Y分别为铜、银,a为1L0.2mol/LAgNO3溶液,写出Y电极反应式
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图二(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。

①结合图二计算,上述电解过程中消耗一氧化碳的质量为
②若图二的B点pH=7,则滴定终点在
您最近半年使用:0次
【推荐3】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是:(至少答出两点)_______ 。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:_______ 。
(2)氢气可用于制备H2O2。已知:
H2(g) + A(l) =B(l) ΔH1
O2(g) + B(l) =A(l) + H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g) + O2(g)= H2O2(l)的ΔH=_______ (用含ΔH1、ΔH2的式子表示)。
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______ 。
(4)化工生产的副产品氢气,也是氢气的一种来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe + 2H2O + 2OH- FeO
FeO + 3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO
+ 3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
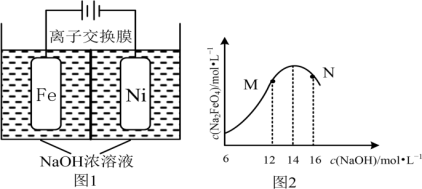
① 电解一段时间后,c(OH−)降低的区域在_______ (填“阴极室”或“阳极室”)。
② 电解过程中,须将阴极产生的气体及时排出,其原因是_______ 。
③ c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:_______ 。
(1)与汽油相比,氢气作为燃料的优点是:(至少答出两点)
(2)氢气可用于制备H2O2。已知:
H2(g) + A(l) =B(l) ΔH1
O2(g) + B(l) =A(l) + H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g) + O2(g)= H2O2(l)的ΔH=
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
(4)化工生产的副产品氢气,也是氢气的一种来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe + 2H2O + 2OH-
 FeO
FeO + 3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO
+ 3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
① 电解一段时间后,c(OH−)降低的区域在
② 电解过程中,须将阴极产生的气体及时排出,其原因是
③ c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分。请参照元素①~⑨在表中的位置,用相应化学用语回答下列问题:

(1)画出表中形成化合物种类最多的元素的原子结构示意图___________ ;考古工作者利用该元素的一种核素测定一些文物的年代,这种核素的原子符号为___________ 。写出该元素与原子半径最小的原子形成的10电子分子的结构式___________ ,上述分子的空间结构呈___________ 形。
(2)写出①③两种元素形成的18电子微粒的电子式___________ 。
(3)③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (填离子符号)④⑤⑥⑧形成的简单离子半径由大到小的顺序为___________ (填离子符号),用电子式表示⑤和⑧形成化合物的过程___________ 。
(4)有两种化合物A和B都由①④⑤⑧四种元素组成,若A与B在水溶液中能发生离子反应、则该反应的离子方程式为___________ 。

(1)画出表中形成化合物种类最多的元素的原子结构示意图
(2)写出①③两种元素形成的18电子微粒的电子式
(3)③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)有两种化合物A和B都由①④⑤⑧四种元素组成,若A与B在水溶液中能发生离子反应、则该反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】短周期主族元素W,X,Y,Z,M,Q的原子序数依次增大,在元素周期表中W的原子半径最小(稀有气体元素除外),X与Y相邻且Y的最外层电子数是次外层的3倍,Y,Z的最外层电子数之和与Q的最外层电子数相等,M是地壳中含量最多的金属元素。回答下列问题:
(1)X在元素周期表中的位置是_______ ;Q的元素符号是_______ 。
(2)M的离子结构示意图是_______ ;由W,Y,Z三种元素组成的既含离子键又含共价键的化合物的电子式是_______ 。
(3)简单氢化物的热稳定性:X_______ (填“小于”或“大于”)Y。
(4)X、Y、Z的简单离子的半径由小到大的顺序为_______ (用离子符号表示)。
(5)M单质与Z的最高价氧化物对应的水化物反应的化学方程式是_______ 。
(6)W和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是_______ (填化学式),此化合物可将碱性工业废水中的 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为_______ 。
(1)X在元素周期表中的位置是
(2)M的离子结构示意图是
(3)简单氢化物的热稳定性:X
(4)X、Y、Z的简单离子的半径由小到大的顺序为
(5)M单质与Z的最高价氧化物对应的水化物反应的化学方程式是
(6)W和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是
 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有八种短周期主族元素 ,其中
,其中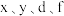 随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。
随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。 的最高价氧化物对应水化物溶液(浓度均为
的最高价氧化物对应水化物溶液(浓度均为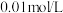 )的
)的 与原子序数的关系如图2所示。
与原子序数的关系如图2所示。

根据上述信息回答下列问题:
(1)g在元素周期表中的位置是___________ 。
(2)比较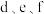 的简单离子半径大小为
的简单离子半径大小为____________________ (用离子符号表示); 的最高价氧化物对应的水化物酸性较强的是
的最高价氧化物对应的水化物酸性较强的是___________ (用化学式表示)。
(3)下列可作为比较e和f金属性强弱的依据是___________ (填字母)。
A.测等浓度相应氯化物水溶液的 B.测两种元素单质的硬度和熔、沸点
B.测两种元素单质的硬度和熔、沸点
C.比较单质作还原剂时失去的电子数目的多少D.比较单质与同浓度盐酸反应的剧烈程度
(4)由元素 组成的剧毒化合物
组成的剧毒化合物 不慎泄漏时,通常用过氧化氢溶液处理,以减少污染,反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为
不慎泄漏时,通常用过氧化氢溶液处理,以减少污染,反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为___________ 。
 ,其中
,其中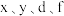 随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。
随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。 的最高价氧化物对应水化物溶液(浓度均为
的最高价氧化物对应水化物溶液(浓度均为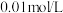 )的
)的 与原子序数的关系如图2所示。
与原子序数的关系如图2所示。
根据上述信息回答下列问题:
(1)g在元素周期表中的位置是
(2)比较
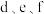 的简单离子半径大小为
的简单离子半径大小为 的最高价氧化物对应的水化物酸性较强的是
的最高价氧化物对应的水化物酸性较强的是(3)下列可作为比较e和f金属性强弱的依据是
A.测等浓度相应氯化物水溶液的
 B.测两种元素单质的硬度和熔、沸点
B.测两种元素单质的硬度和熔、沸点C.比较单质作还原剂时失去的电子数目的多少D.比较单质与同浓度盐酸反应的剧烈程度
(4)由元素
 组成的剧毒化合物
组成的剧毒化合物 不慎泄漏时,通常用过氧化氢溶液处理,以减少污染,反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为
不慎泄漏时,通常用过氧化氢溶液处理,以减少污染,反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F为短周期主族元素,其原子序数依次增大。A、B 两元素最高正价和最低负价之和为零。E和A同主族;D、F是地壳中含量最高的非金属元素和金属元素。
(1)写出C元素的元素名称_______ ,其在周期表中的位置__________________ 。E离子结构示意图为__________________ ;E2D2的电子式________________________ 。
(2)由A、C以原子个数比为5︰1组成的一种化合物,其中各原子均达到稳定结构,该化合物中所含化学键类型为_________________________ 。
(3)E2D2和A2D反应的离子方程式为__________________________________________ 。
(4)由C、E组成的一种离子化合物化学式为E3C,该化合物中两种离子的半径由大到小的顺序是____________ (用元素符号表示);该化合物遇水剧烈反应,该反应的化学方程式为___________________________________ 。
(1)写出C元素的元素名称
(2)由A、C以原子个数比为5︰1组成的一种化合物,其中各原子均达到稳定结构,该化合物中所含化学键类型为
(3)E2D2和A2D反应的离子方程式为
(4)由C、E组成的一种离子化合物化学式为E3C,该化合物中两种离子的半径由大到小的顺序是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分,回答以下问题:
(1) 与
与 的原子半径大小关系是:
的原子半径大小关系是:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)F与 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F___________  (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是___________ (填化学式)。
(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是___________ (填化学式)。
(4) 与
与 组成
组成
 所含的化学键类型为
所含的化学键类型为___________ (填“离子键”或“共价键”)。
(5)地壳中含量最高的金属元素是___________ ,能用来做光导纤维的是___________ 元素的氧化物(填元素符号)。
(6)C位于元素周期表中第___________ 周期第___________ 族,易以碳碳键和碳氢键形成甲烷 、乙烷
、乙烷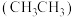 、乙烯
、乙烯 等烃类化合物。甲烷与乙烷属于
等烃类化合物。甲烷与乙烷属于___________ (填“同系物”或“同分异构体”);乙烷与乙烯可相互转化,如:

 生成
生成 的反应类型为
的反应类型为___________
| C | N | F | ||||
 |  |  |  |  |  |
 与
与 的原子半径大小关系是:
的原子半径大小关系是:
 (填“>”或“<”)。
(填“>”或“<”)。(2)F与
 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是
(4)
 与
与 组成
组成
 所含的化学键类型为
所含的化学键类型为(5)地壳中含量最高的金属元素是
(6)C位于元素周期表中第
 、乙烷
、乙烷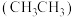 、乙烯
、乙烯 等烃类化合物。甲烷与乙烷属于
等烃类化合物。甲烷与乙烷属于
 生成
生成 的反应类型为
的反应类型为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
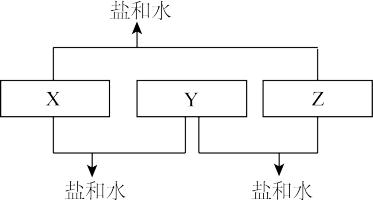
【推荐3】已知A、B、C、D为四种原子序数依次增大的短周期元素,A与D的原子序数之和等于B与C的原子序数之和,D的单质在通常状况下呈黄绿色,B、C、D处在同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且X、Y、Z间存在如图转化关系,回答下列问题:
(1)D的原子结构示意图为___________ 。
(2)A、B、D三种元素对应简单离子半径由大到小的顺序为___________ (用离子符号表示),A、D的最简单氢化物中呈碱性的是___________ (用化学式表示)。
(3)Y的溶液与C的单质反应的离子方程式为___________ 。
(4)A的最简单氢化物与D的单质反应可生成一种盐和A的单质,该盐的电子式是___________ ,发生反应的化学方程式为___________ 。
(5)向Y的溶液与Z反应生成的盐溶液中通入过量 后产生白色絮状沉淀,原因是
后产生白色絮状沉淀,原因是___________ (用离子方程式表示)。

(1)D的原子结构示意图为
(2)A、B、D三种元素对应简单离子半径由大到小的顺序为
(3)Y的溶液与C的单质反应的离子方程式为
(4)A的最简单氢化物与D的单质反应可生成一种盐和A的单质,该盐的电子式是
(5)向Y的溶液与Z反应生成的盐溶液中通入过量
 后产生白色絮状沉淀,原因是
后产生白色絮状沉淀,原因是
您最近半年使用:0次



