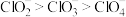氟硼酸铵( )易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。
)易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。 与HF反应后再用
与HF反应后再用 中和得到
中和得到 。下列叙述正确的是
。下列叙述正确的是
 )易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。
)易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。 与HF反应后再用
与HF反应后再用 中和得到
中和得到 。下列叙述正确的是
。下列叙述正确的是A.HF、 都是由极性键构成的极性分子 都是由极性键构成的极性分子 |
B.1mol 中含有配位键的数目为 中含有配位键的数目为 |
C. 与 与 的VSEPR模型相同 的VSEPR模型相同 |
D.推测 可与HF反应生成 可与HF反应生成 |
更新时间:2024-05-05 07:57:37
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】实验测得不同物质中氧原子之间的键长和键能的数据如下:
其中x、y的键能数据尚未测定,但可根据规律性推导键能的大小顺序为w>z>y>x,该规律是
| 粒子 | O | O | O2 | O |
| 键长/(10-12m) | 149 | 128 | 121 | 112 |
| 键能/(kJ·mol-1) | x | y | z=494 | w=628 |
| A.粒子所含的价层电子数越多,键能越大 |
| B.键长越大,键能越小 |
| C.粒子所含的价电子数越少,键能越大 |
| D.成键时电子对越偏移,键能越大 |
您最近一年使用:0次
【推荐2】检验Ni2+的反应原理如图:
2 +Ni2+→
+Ni2+→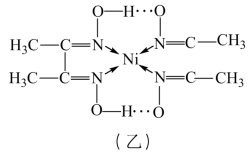 ↓+2H+
↓+2H+
下列说法不正确的是
2
 +Ni2+→
+Ni2+→ ↓+2H+
↓+2H+下列说法不正确的是
A.甲中 键与 键与 键的个数比是7∶1 键的个数比是7∶1 |
| B.乙中Ni2+的配位数是4 |
| C.乙分子内存在氢键 |
| D.C、N、O的第一电离能大小顺序为O>N>C |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】硫代碳酸钠能用于处理废水中的重金属离子,可通过如下反应制备:2NaHS(s)+CS2(l)=Na2CS3(s)+H2S(g),下列说法正确的是
| A.Na2CS3能被氧化 | B.CS2的空间结构为直线形 |
| C.NaHS晶体中阴阳离子的比例为1:2 | D.CS2的热稳定性比CO2的高 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 的最高正价与最低负价代数和为0,
的最高正价与最低负价代数和为0, 、
、 、
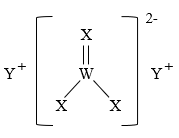
、 形成的化合物甲的结构如图所示,
形成的化合物甲的结构如图所示, 在同周期中原子半径最小。下列说法正确的是( )
在同周期中原子半径最小。下列说法正确的是( )
 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 的最高正价与最低负价代数和为0,
的最高正价与最低负价代数和为0, 、
、 、
、 形成的化合物甲的结构如图所示,
形成的化合物甲的结构如图所示, 在同周期中原子半径最小。下列说法正确的是( )
在同周期中原子半径最小。下列说法正确的是( )
A.原子半径大小: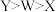 |
B.电负性大小: |
C. 、 、 形成的化合物为离子化合物 形成的化合物为离子化合物 |
| D.化合物甲中阴离子的空间构型为三角锥形 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列分子中,含极性键的非极性分子的是
| A.H2O | B.CH4 | C.NH3 | D.CO2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】膦(PH3)在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含之。它的分子是三角锥形。以下关于PH3的叙述中,正确的是( )
| A.PH3是非极性分子 |
| B.PH3分子中有未成键的电子对 |
| C.PH3中的P-H键的极性比NH3中N-H键的极性弱 |
| D.PH3分子中的P-H键是非极性键 |
您最近一年使用:0次

 分子的极性比
分子的极性比 的大
的大
 的分子构型为
的分子构型为 形,则二甲醚的分子骨架
形,则二甲醚的分子骨架 构型为
构型为