硅单质及其化合物应用广泛。请回答下列问题:
(1) 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)___________ 。
(2)硅单质可作为硅半导体材料。三氯甲硅烷( )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图:
石英砂 粗硅
粗硅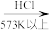
 (粗)
(粗)
 (纯)
(纯) 高纯硅
高纯硅
①写出制粗硅的化学方程式___________ 。
②整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式___________ 。
(3)新型陶瓷材料氮化硅( )可应用于原子反应堆,一种制备氮化硅的反应为:
)可应用于原子反应堆,一种制备氮化硅的反应为:
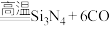 。若生成标准状况下33.6L CO时,反应过程中转移的电子数为
。若生成标准状况下33.6L CO时,反应过程中转移的电子数为___________ 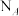 。
。
(1)
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)(2)硅单质可作为硅半导体材料。三氯甲硅烷(
 )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图:石英砂
 粗硅
粗硅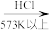
 (粗)
(粗)
 (纯)
(纯) 高纯硅
高纯硅①写出制粗硅的化学方程式
②整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式(3)新型陶瓷材料氮化硅(
 )可应用于原子反应堆,一种制备氮化硅的反应为:
)可应用于原子反应堆,一种制备氮化硅的反应为:
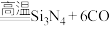 。若生成标准状况下33.6L CO时,反应过程中转移的电子数为
。若生成标准状况下33.6L CO时,反应过程中转移的电子数为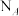 。
。
更新时间:2024-05-05 08:19:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求作答:
Ⅰ.现有以下8种物质:①熔融状态的NaCl、②NO2、③NaHCO3、④铜、⑤AgCl、⑥酒精、⑦NaOH溶液、⑧FeCl3溶液。
(1)上述物质中,属于电解质的是___________ 。(填序号)
(2)写出③溶于水的电离方程式:___________ 。
(3)写出③与⑦反应的离子方程式:___________ 。
Ⅱ.把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(4)用双线桥表示反应的电子转移方向和数目:___________ 。
(5)氧化剂与还原剂的分子数之比为:___________
(6)若反应中有6.8g氨发生氧化反应,则反应中生成氮气的质量为___________ g.
Ⅰ.现有以下8种物质:①熔融状态的NaCl、②NO2、③NaHCO3、④铜、⑤AgCl、⑥酒精、⑦NaOH溶液、⑧FeCl3溶液。
(1)上述物质中,属于电解质的是
(2)写出③溶于水的电离方程式:
(3)写出③与⑦反应的离子方程式:
Ⅱ.把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(4)用双线桥表示反应的电子转移方向和数目:
(5)氧化剂与还原剂的分子数之比为:
(6)若反应中有6.8g氨发生氧化反应,则反应中生成氮气的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图为一个五元环图案,小明在图案上依次写了五种物质,使图中相交的两种物质发生化学反应,A、B、C、D、E表示其相应的化学反应。

回答下列问题:
(1)反应A、B、C、D、E中属于氧化还原反应的是_______ (填字母)。
(2)上图的五个反应中,属于复分解反应的是:_______ (填字母)。
(3)反应A的离子方程式为_______ 。
(4)用双线桥分析反应B的离子方程式:_______ 。
(5)已知反应: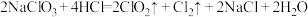 ,该反应的还原产物是
,该反应的还原产物是_______ (写化学式),该反应中氧化剂与还原剂质量之比_______ 。

回答下列问题:
(1)反应A、B、C、D、E中属于氧化还原反应的是
(2)上图的五个反应中,属于复分解反应的是:
(3)反应A的离子方程式为
(4)用双线桥分析反应B的离子方程式:
(5)已知反应:
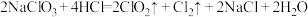 ,该反应的还原产物是
,该反应的还原产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐3】离子液体是一种室温熔融盐,为非水体系.由有机阳离子、Al2Cl7﹣和AlCl4﹣组成的离子液体做电解液时,可在钢制品上电镀铝.
(1)钢制品应接电源的_______ 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为________________ ,若改用AlCl3水溶液作电解液,则阴极产物为_____________ .
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为________ mol.
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有__________
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,_______ (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是__________________ (用离子方程式说明).
(1)钢制品应接电源的
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)①写出乙炔的结构式:_______
②写出漂白粉有效成分的化学式:_______ 。
(2)写出工业制取粗硅的化学方程式:_______ 。
(3)写出铜与稀硝酸反应的离子方程式:_______ 。
②写出漂白粉有效成分的化学式:
(2)写出工业制取粗硅的化学方程式:
(3)写出铜与稀硝酸反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硅在无机非金属材料中扮演着主要角色。回答下列问题:
(1)硅有非常重要的用途,请写出其中一种:_______ 。
(2)古瓷中所用颜料成分一直是个谜,近年来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi2Ox,铜为+2价),下列关于硅酸铜钡的说法不正确的是_______(填选项字母)。
(3)工业上提纯硅有多种路线,其中一种工艺流程如图所示:

①电弧炉中发生反应的化学方程式为_______ 。
②SiCl4与水反应生成两种酸,其反应化学方程式为_______ 。
③在流化床反应的产物中,除SiCl4外,还有SiHCl3、SiH2Cl2、SiH3Cl、FeCl3等,有关物质的沸点数据如下表所示,分离SiCl4和其他杂质的方法为_______ 。
④分离出SiCl4后的残余物中含有铁元素,为了测定残余物中铁元素的含量,先将残余物预处理,使铁元素还原成Fe2+,再用酸性KMnO4溶液与其反应,反应的离子方程式为_______ ,某同学称取1.000g残余物,经预处理后配制成100mL溶液,移取20.00mL试样溶液,用1.000×10-3mol·L-1酸性KMnO4溶液与其反应,KMnO4溶液恰好褪色时,消耗酸性KMnO4溶液20.00mL,则残余物中铁元素的质量分数是_______ 。
(1)硅有非常重要的用途,请写出其中一种:
(2)古瓷中所用颜料成分一直是个谜,近年来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi2Ox,铜为+2价),下列关于硅酸铜钡的说法不正确的是_______(填选项字母)。
| A.可用氧化物形式表示为BaO·CuO·2SiO2 |
| B.性质稳定,不易脱色 |
| C.x=6 |
| D.易溶解于强酸和强碱 |

①电弧炉中发生反应的化学方程式为
②SiCl4与水反应生成两种酸,其反应化学方程式为
③在流化床反应的产物中,除SiCl4外,还有SiHCl3、SiH2Cl2、SiH3Cl、FeCl3等,有关物质的沸点数据如下表所示,分离SiCl4和其他杂质的方法为
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/°C | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯碱工业中,通过电解饱和食盐水获得重要的化工原料。其中氯气用途十分广泛,除用于自来水消毒、生产漂白粉外,还用于生产盐酸、聚氯乙烯、氯苯等。
(1)写出电解饱和食盐水的化学方程式:_______ 。
(2)氯气用于生产半导体材料硅的流程如下:
①石英砂的主要成分是_______ ,在制备粗硅时,焦炭的作用是_______ 。
②写出四氯化硅得到高纯硅的化学方程式:_______ 。
(3)用于制造塑料薄膜、人造革、塑料管材和板材的聚氯乙烯(PVC塑料)就是以氯气和乙烯为主要原料通过三步主要反应生产的。三步反应的化学方程式分别为
①_______ ;
 ;
;
③_______ 。
其中①、③的反应类型分别为_______ 反应、_______ 反应。
(4)上述两种生产过程可得到同一种副产品,该副产品是_______ 。
(1)写出电解饱和食盐水的化学方程式:
(2)氯气用于生产半导体材料硅的流程如下:

①石英砂的主要成分是
②写出四氯化硅得到高纯硅的化学方程式:
(3)用于制造塑料薄膜、人造革、塑料管材和板材的聚氯乙烯(PVC塑料)就是以氯气和乙烯为主要原料通过三步主要反应生产的。三步反应的化学方程式分别为
①
 ;
;③
其中①、③的反应类型分别为
(4)上述两种生产过程可得到同一种副产品,该副产品是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。

回答下列问题:
(1)硅粉与HCl在300℃时反应生成SiHCl3气体和H2,当有1gSi反应时放出8.4kJ热量,该反应的热化学方程式为____ 。
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g) SiHCl3(g)+HCl(g) △H1>0
SiHCl3(g)+HCl(g) △H1>0
②3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0
③2SiCl4(g)+H2(g)+Si(s)+HCl(g) 3SiHCl3(g) △H3
3SiHCl3(g) △H3
反应③的△H3____ 0(填“>”或“<”)。
(3)由粗硅制备多晶硅过程中循环使用的物质除SiCl4、SiHCl3、Si外,还有____ (填化学式)。
(4)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能,利用键能可以衡量化学键的强弱,也可以计算化学反应的焓变。已知:
则SiO2与SiC中比较稳定的是____ (填化学式),工业上高纯硅可以通过下列反应制取:SiCl4(g)+2H2(g)=Si(s)+4HCl(g),该反应的△H=____ 。(提示:1mol晶体Si中含有2molSi-Si键)

回答下列问题:
(1)硅粉与HCl在300℃时反应生成SiHCl3气体和H2,当有1gSi反应时放出8.4kJ热量,该反应的热化学方程式为
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g)
 SiHCl3(g)+HCl(g) △H1>0
SiHCl3(g)+HCl(g) △H1>0②3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0③2SiCl4(g)+H2(g)+Si(s)+HCl(g)
 3SiHCl3(g) △H3
3SiHCl3(g) △H3反应③的△H3
(3)由粗硅制备多晶硅过程中循环使用的物质除SiCl4、SiHCl3、Si外,还有
(4)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能,利用键能可以衡量化学键的强弱,也可以计算化学反应的焓变。已知:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)SiO2在自然界中广泛存在,它是制备现代通讯材料___ (写该材料名称)的主要原料;以SiO2为原料,在工业上制备单质粗硅的化学方程式为___ ;在常温下,SiO2可与一种酸发生反应,该反应的化学方程式为___ 。该反应的重要应用是__ 。
(2)在一定体积的18mol/L的浓硫酸加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积___ (填“大于”“小于”或“等于”)100mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式__ 。
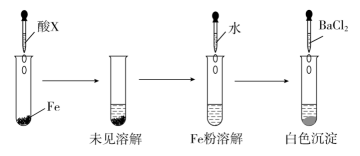
(3)根据下图操作及现象推断酸X为__ 。
(2)在一定体积的18mol/L的浓硫酸加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积
(3)根据下图操作及现象推断酸X为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】非金属元素在生产生活中扮演着重要角色。请根据题意填空;
(1)氨是一种极易溶于水的气体,其水溶液能使酚酞溶液变_______ (填“红”或“蓝”);
(2)SO2有一定的还原性,在葡萄酒的酿制过程中,添加适量的SO2,除可杀菌外,还可防止葡萄酒中的一些成分被_______ (填“氧化”或“还原”),起到保质作用;
(3)玻璃中的成分SiO2能与NaOH溶液反应: ,实验室中盛放NaOH溶液应选用带
,实验室中盛放NaOH溶液应选用带_______ (填“玻璃塞”或“橡胶塞”)的试剂瓶。
(1)氨是一种极易溶于水的气体,其水溶液能使酚酞溶液变
(2)SO2有一定的还原性,在葡萄酒的酿制过程中,添加适量的SO2,除可杀菌外,还可防止葡萄酒中的一些成分被
(3)玻璃中的成分SiO2能与NaOH溶液反应:
 ,实验室中盛放NaOH溶液应选用带
,实验室中盛放NaOH溶液应选用带
您最近一年使用:0次



