某化学兴趣小组用下图装置(部分夹持装置已略去)制取氨气并探究其性质。___________ 。(填化学式)
(2)气体通过C、D装置时,试纸颜色发生变化的是___________ (填字母),原因是氨水呈___________ 性。
(3)当E装置中集满 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是___________ 。
(4)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。___________ ,证明氨气具有___________ (填“氧化性”或“还原性”)。
(5)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为___________ mol∙L-1。
(6)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN加热时可溶于浓碱溶液并产生氨气,写出浓碱中发生反应的化学方程式:___________ 。

(2)气体通过C、D装置时,试纸颜色发生变化的是
(3)当E装置中集满
 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到E中的现象是(4)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(5)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为
(6)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN加热时可溶于浓碱溶液并产生氨气,写出浓碱中发生反应的化学方程式:
更新时间:2024-05-08 19:10:19
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知X、Y、Z、M、N、A均为短周期元素形成的常见单质或化合物,其转化关系如图所示(部分产物及条件略去)。

请回答下列问题:
(1)若A、X、Y均为单质,且A元素的主族序数是其周期数的两倍,则A原子的结构示意图为___________ ,由X生成Y的化学方程式为___________ 。
(2)若X为淡黄色固体,N为空气的成分之一,M为易溶于水的物质,且X与Z的摩尔质量相同,则N的电子式为___________ ;若X与水反应转移的电子物质的量为3 mol,则得到Z的物质的量为___________ mol。
(3)若X为二元化合物,所含金属元素原子的最内层电子数等于最外层电子数,常温下M为红棕色气体,则Y+A→Z的反应中,氧化剂与还原剂物质的量之比为___________ ,实验室检验Y气体的常用方法是___________ 。

请回答下列问题:
(1)若A、X、Y均为单质,且A元素的主族序数是其周期数的两倍,则A原子的结构示意图为
(2)若X为淡黄色固体,N为空气的成分之一,M为易溶于水的物质,且X与Z的摩尔质量相同,则N的电子式为
(3)若X为二元化合物,所含金属元素原子的最内层电子数等于最外层电子数,常温下M为红棕色气体,则Y+A→Z的反应中,氧化剂与还原剂物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学利用图所示装置探究Cl2与NH3的反应。其中A、F分别为NH3和Cl2的发生装置,C为纯净干燥的Cl2与NH3反应的装置。

回答下列问题:
(1)A装置中盛有浓氨水的仪器名称为________ ;B装置中盛有的药品是________ 。
(2)E装置的作用是________ ;F装置中发生反应的离子方程式为________ 。
(3)C装置内发生置换反应,并有浓厚的白烟产生,则C中发生反应的化学方程式为________ ,该反应中氧化剂与还原剂的物质的量之比为________ 。
(4)C装置的G处需连接一个装置,可选用图中的________ (填序号)。


回答下列问题:
(1)A装置中盛有浓氨水的仪器名称为
(2)E装置的作用是
(3)C装置内发生置换反应,并有浓厚的白烟产生,则C中发生反应的化学方程式为
(4)C装置的G处需连接一个装置,可选用图中的

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
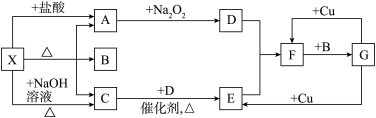
【推荐3】如图所示每一方框表示一种反应物或生成物,其中A、C、D、E、F在通常情况下均为气体,且加热X生成的A与C的物质的量之比为1∶1,B为常见液体。
试回答下列问题:
(1)X是________ (填化学式,下同),F是__________ 。
(2)A―→D反应的化学方程式为_______ 。
(3)G与Cu的反应中,G表现的性质为______ 。
(4)X与过量NaOH溶液反应生成C的离子方程式为_____________ 。
(5)以C、B、D为原料可生产G,若使amol C完全转化为G,理论上至少需要D___ mol。
试回答下列问题:
(1)X是
(2)A―→D反应的化学方程式为
(3)G与Cu的反应中,G表现的性质为
(4)X与过量NaOH溶液反应生成C的离子方程式为
(5)以C、B、D为原料可生产G,若使amol C完全转化为G,理论上至少需要D
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氨基甲酸铵(H2NCOONH4)是一种易水解、受热易分解的白色固体,某研究小组用下图所示的实验装置制备氨基甲酸铵,反应原理为:2NH3(g)+CO2(g)=H2NCOONH4(s) △H<0。
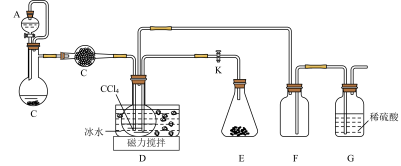
(1)仪器B的名称是________________ 。
(2)打开阀门K,装置E中由固体药品所产生的气体就立即进入装置D,则该固体药品的名称为________________ 。
(3)装置D为制备氨基甲酸铵的反应器(CCl4充当惰性介质),在合适催化剂下搅拌一段时间。
①反应在冰水浴中进行的原因为_______________________________________ 。
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,__________ (填操作名称)分离得到粗产品。
(4)仪器G的作用有:_______________________________________ 。
(5)该实验装置中有一处不足,改进方法是______________________________________ 。
(6)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式_________________ 。
(7)为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验,已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案(限选试剂:蒸馏水、澄清石灰水、Ba(OH)2溶液):用天平称取一定质量的样品,加水溶解,____________________ ,测量的数据取平均值进行计算。

(1)仪器B的名称是
(2)打开阀门K,装置E中由固体药品所产生的气体就立即进入装置D,则该固体药品的名称为
(3)装置D为制备氨基甲酸铵的反应器(CCl4充当惰性介质),在合适催化剂下搅拌一段时间。
①反应在冰水浴中进行的原因为
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,
(4)仪器G的作用有:
(5)该实验装置中有一处不足,改进方法是
(6)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式
(7)为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验,已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案(限选试剂:蒸馏水、澄清石灰水、Ba(OH)2溶液):用天平称取一定质量的样品,加水溶解,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外活动小组欲利用 CuO 与 NH3反应,研究 NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
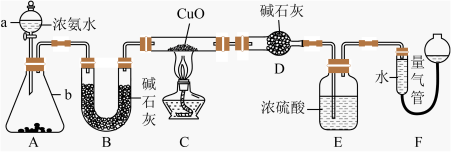
(1)仪器a的名称为_____ ;仪器b中可选择的试剂为________ (填名称)。
(2)实验室中,利用装置A,还可制取的无色气体是______ (填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______ 性,写出相应的化学方程式____________ 。
(4)E装置中浓硫酸的作用________ 。
(5)读取气体体积前,应对装置F进行的操作:__________ 。
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为___________ (用含m、n字母的代数式表示)。

(1)仪器a的名称为
(2)实验室中,利用装置A,还可制取的无色气体是
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有
(4)E装置中浓硫酸的作用
(5)读取气体体积前,应对装置F进行的操作:
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氨气是一种重要化合物,在工农业生产、生活中有着重要应用。
(1)下列装置可用于实验室制取少量氨气的是___________ (填序号)
a. b.
b. c.
c. d.
d.
(2)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸 固定装置略去
固定装置略去 :
:

① 装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是
装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是___________  填化学式
填化学式
② 装置中发生的化学反应方程式为
装置中发生的化学反应方程式为___________ 
③反应后,装置 中除存在较多的
中除存在较多的 外,还可能存在的一种阳离子是
外,还可能存在的一种阳离子是___________ ,试设计实验证明这种离子的存在___________ 。
④下列哪些装置可以同时起到装置 和
和 的作用
的作用___________  填代号
填代号
a. b.
b. c.
c. d.
d.
(3)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式___________  不必配平
不必配平 ,该反应生成的还原产物中化学键类型是
,该反应生成的还原产物中化学键类型是___________ 。
(1)下列装置可用于实验室制取少量氨气的是
a.
 b.
b. c.
c. d.
d.
(2)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸
 固定装置略去
固定装置略去 :
:
①
 装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是
装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是 填化学式
填化学式
②
 装置中发生的化学反应方程式为
装置中发生的化学反应方程式为
③反应后,装置
 中除存在较多的
中除存在较多的 外,还可能存在的一种阳离子是
外,还可能存在的一种阳离子是④下列哪些装置可以同时起到装置
 和
和 的作用
的作用 填代号
填代号
a.
 b.
b. c.
c. d.
d.
(3)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式
 不必配平
不必配平 ,该反应生成的还原产物中化学键类型是
,该反应生成的还原产物中化学键类型是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】为了说明稀硝酸与铜反应产生无色的一氧化氮气体,某同学设计了如图所示的实验装置。实验时,将分液漏斗的活塞打开,从U形管的长管口B注入稀硝酸,一直到U形管的短管口A单孔塞下沿且液面不再留有气泡为止。关闭活塞,并用酒精灯在U形管短管下微热。当铜丝上有气泡产生时,立即撤去酒精灯。试回答

(1)反应一段时间后,会出现什么现象__________________ ;_______________ ;_________________________________________________ 。
(2)若将活塞缓缓打开,分液漏斗内有何现象_______________________________________ 。
(3)写出生成一氧化氮的离子方程式 _______________________________________________ 。

(1)反应一段时间后,会出现什么现象
(2)若将活塞缓缓打开,分液漏斗内有何现象
(3)写出生成一氧化氮的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
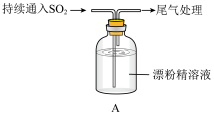
【推荐2】某学生对 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:
(1)pH试纸颜色的变化说明漂粉精溶液具有的性质是______ 。
(2)向水中持续通入 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。
①实验a目的是______ 。
②由实验a、b不能判断白雾中含有HCl,理由是______ 。
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是______ 。
(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是______ 。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:______ 。
 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
| ⅰ.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(2)向水中持续通入
 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的
 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。①实验a目的是
②由实验a、b不能判断白雾中含有HCl,理由是
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和
 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入
 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是②用离子方程式解释现象ⅲ中黄绿色褪去的原因:
您最近一年使用:0次