硫酸是在工业生产中极为重要的一种化工产品,而硫酸的浓度不同,性质也会不同。现有甲、乙两研究小组分别进行了如下实验探究:
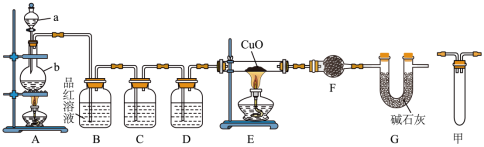
I.甲研究小组按下图装置进行实验,验证锌与浓硫酸反应生成物中的气体成分,取足量的Zn置于b中,向a中加入适量浓硫酸,经过一段时间的反应,Zn仍有剩余。_______ 。
(2)在反应初始阶段 ,装置A中发生的化学方程式为_______ 。
(3)装置C中若为酸性高锰酸钾溶液,则对应的离子方程式 为_____ 。
(4)装置G的名称为U形管,其作用为______ 。
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为______ 。
Ⅱ.乙研究小组为了利用稀硫酸制备CuSO4,进行了如下图所示的实验设计。
①2Fe3+ + Cu = 2Fe2+ + Cu2+
②∙∙∙∙∙∙
(6)反应②的离子方程式 为______ 。
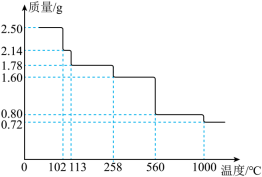
(7)取CuSO4·5H2O晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示,当达到120℃时,固体的成分为_______ 。
I.甲研究小组按下图装置进行实验,验证锌与浓硫酸反应生成物中的气体成分,取足量的Zn置于b中,向a中加入适量浓硫酸,经过一段时间的反应,Zn仍有剩余。
(2)在
(3)装置C中若为酸性高锰酸钾溶液,则对应的
(4)装置G的名称为U形管,其作用为
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为
Ⅱ.乙研究小组为了利用稀硫酸制备CuSO4,进行了如下图所示的实验设计。

①2Fe3+ + Cu = 2Fe2+ + Cu2+
②∙∙∙∙∙∙
(6)反应②的
(7)取CuSO4·5H2O晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示,当达到120℃时,固体的成分为
更新时间:2024-05-11 14:10:48
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】现有A~G七种中学常见物质,它们之间能发生如下反应(图中部分反应物、产物及反应条件未标出)。
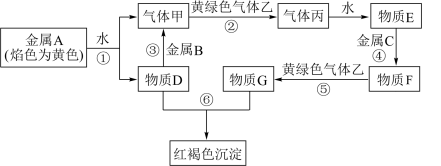
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B___________ 、C___________ 、乙___________ 。
(2)借助KSCN溶液检验物质F中金属阳离子的方法是___________ 。
(3)写出反应③和⑤的离子方程式:___________ 、___________ 。
(4)将物质F少许,置于试管中,并加入NaOH溶液,其现象为___________ ,发生反应的化学方程式为___________ 、___________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B
(2)借助KSCN溶液检验物质F中金属阳离子的方法是
(3)写出反应③和⑤的离子方程式:
(4)将物质F少许,置于试管中,并加入NaOH溶液,其现象为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:

请回答下列问题:
(1)①吸收器中生成 的离子方程式为(补充完整):
的离子方程式为(补充完整):_______ 。
_______ +_______
+_______ +_______=
+_______= _______↑+_______
_______↑+_______
②此氧化还原反应中,双氧水表现_______ 性;若2mol 完全反应,
完全反应,_______ (填“得到”或“失去”)的电子数为_______ 个,生成的气体产物的体积为_______ (标况下)。
(2)为了探究 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液
(3)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。
的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。 的有效氯含量为
的有效氯含量为_______ (计算结果保留两位小数)。
 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:
请回答下列问题:
(1)①吸收器中生成
 的离子方程式为(补充完整):
的离子方程式为(补充完整):_______
 +_______
+_______ +_______=
+_______= _______↑+_______
_______↑+_______②此氧化还原反应中,双氧水表现
 完全反应,
完全反应,(2)为了探究
 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液| 序号 | 实验操作 | 实验现象 | 实验结论 |
| ① | 将 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 | ||
| ② |  溶液 溶液 |  具有还原性 具有还原性 |
 的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。
的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】工业上由钛精矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+TiOSO4(aq)+2H2O(l)
水解TiOSO4(aq)+2H2O(l) H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)
简要工艺流程如图:
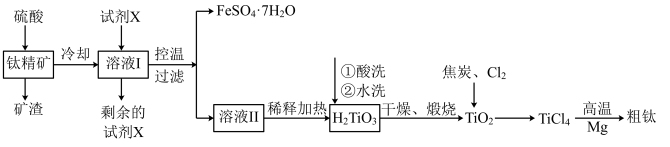
(1)矿渣主要成分____ ,试剂X为____ (填化学式)。
(2)为加快钛精矿的酸溶速率和浸取率,可采用循环浸取、延长时间、矿石粉碎、____ (写一种)等措施。
(3)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是____ 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是____ (填化学式)。
(4)TiO2与足量焦炭和Cl2在高温下反应的化学方程式____ 。
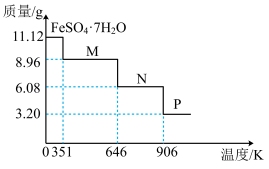
(5)取副产品绿矾FeSO4•7H2O(M=278g/mol)11.12g,隔绝空气加热时,样品质量随温度变化的曲线如图所示,分解产物M的化学式____ ,样品N加热至1000K得到P的化学方程式为____ 。
酸溶FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+TiOSO4(aq)+2H2O(l)
水解TiOSO4(aq)+2H2O(l)
 H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)简要工艺流程如图:

(1)矿渣主要成分
(2)为加快钛精矿的酸溶速率和浸取率,可采用循环浸取、延长时间、矿石粉碎、
(3)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是
(4)TiO2与足量焦炭和Cl2在高温下反应的化学方程式
(5)取副产品绿矾FeSO4•7H2O(M=278g/mol)11.12g,隔绝空气加热时,样品质量随温度变化的曲线如图所示,分解产物M的化学式

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】某冶炼厂利用镉熔炼碱渣(约含 及
及 、
、 、
、 )和铜镉渣(含
)和铜镉渣(含 、
、 、
、 、
、 等单质)联合工艺制备黄钠铁钒[
等单质)联合工艺制备黄钠铁钒[ ],并回收
],并回收 、
、 等金属。
等金属。

(1)滤渣Ⅰ主要含 和
和 ,请写出热水溶浸时发生反应的化学方程式:
,请写出热水溶浸时发生反应的化学方程式:_______ 。
(2)在 约为1.5时,制得黄钠铁矾[
约为1.5时,制得黄钠铁矾[ ]的离子方程式为
]的离子方程式为_______ 。
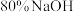 及
及 、
、 、
、 )和铜镉渣(含
)和铜镉渣(含 、
、 、
、 、
、 等单质)联合工艺制备黄钠铁钒[
等单质)联合工艺制备黄钠铁钒[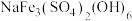 ],并回收
],并回收 、
、 等金属。
等金属。
(1)滤渣Ⅰ主要含
 和
和 ,请写出热水溶浸时发生反应的化学方程式:
,请写出热水溶浸时发生反应的化学方程式:(2)在
 约为1.5时,制得黄钠铁矾[
约为1.5时,制得黄钠铁矾[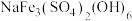 ]的离子方程式为
]的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】下图是关于 的实验装置图,回答下列问题:
的实验装置图,回答下列问题:___________ 。
(2)C中现象及反应的离子方程式___________ 。
(3)E中现象及反应的化学方程式___________ 。
(4)G的作用及反应的离子方程式___________ 。
 的实验装置图,回答下列问题:
的实验装置图,回答下列问题: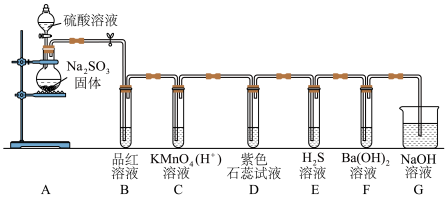
(2)C中现象及反应的离子方程式
(3)E中现象及反应的化学方程式
(4)G的作用及反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室里研究不同价态硫元素之间的转化

(1)A中发生反应的化学方程式为___________ 。
(2)B中的现象是___________ 。
(3)C中出现淡黄色沉淀,反应中Na2S做___________ (填“氧化剂”或“还原剂”)。
(4)D中溴水褪色,该反应S元素的价态变化是由+4价变为___________ 价。
(5)E的作用是吸收多余的SO2,离子方程式为___________ 。
(6)上述实验D体现SO2的性质是___________ 。

(1)A中发生反应的化学方程式为
(2)B中的现象是
(3)C中出现淡黄色沉淀,反应中Na2S做
(4)D中溴水褪色,该反应S元素的价态变化是由+4价变为
(5)E的作用是吸收多余的SO2,离子方程式为
(6)上述实验D体现SO2的性质是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是实验室制取 并验证
并验证 的某些性质的装置,试回答下列问题:
的某些性质的装置,试回答下列问题:
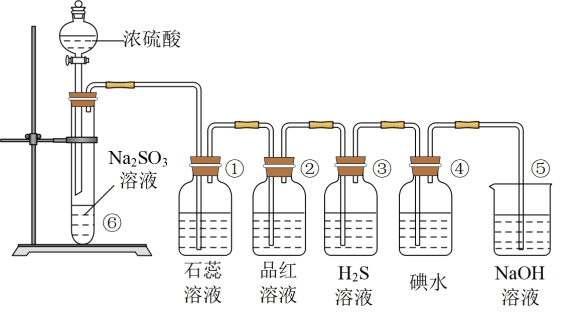
(1)在⑥中发生反应的化学方程式_______ 。
(2)①中的实验现象为_______ ,此实验证明 是
是_______ (填“酸性”或“碱性”)气体。
(3)②中的实验现象_______ ,证明 有
有_______ (填“漂白”“氧化”或“还原”)性。
(4)④中的实验现象是_______ ,证明 有
有_______ (填“漂白”“氧化”或“还原”)性。
(5)⑤的作用是_______ (用离子方程式表示)
 并验证
并验证 的某些性质的装置,试回答下列问题:
的某些性质的装置,试回答下列问题:
(1)在⑥中发生反应的化学方程式
(2)①中的实验现象为
 是
是(3)②中的实验现象
 有
有(4)④中的实验现象是
 有
有(5)⑤的作用是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】工业上用赤铁矿(主要含 、,还含有少量的
、,还含有少量的 、
、 等杂质)制备绿矾(
等杂质)制备绿矾(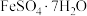 )的流程如下:
)的流程如下:
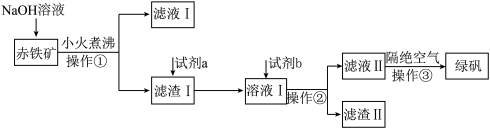
(1) 溶液加入赤铁矿中发生反应的离子方程式为
溶液加入赤铁矿中发生反应的离子方程式为_______ 。
(2)试剂 为
为_______ (填化学式);“溶液I”中氧化性最强的阳离子为_______ (填化学式);操作②需要使用到的玻璃仪器有_______ 。
(3)若取2mL“滤液Ⅰ”加入试管中,然后通入足量CO2,产生的现象是_______ ;另取2mL“滤液Ⅱ”加入试管中,并向该溶液中滴入稀 酸化的
酸化的 溶液,观察到溶液由浅绿色变成棕黄色,请写出该反应的离子方程式
溶液,观察到溶液由浅绿色变成棕黄色,请写出该反应的离子方程式_______ 。
(4)8.34g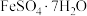 (
(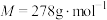 )样品受热分解过程中样品质量随温度变化的曲线如图所示:
)样品受热分解过程中样品质量随温度变化的曲线如图所示:

①温度为78℃时,固体物质M的化学式为_______ 。
②取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种常见硫的氧化物生成,写出由P生成Q的化学方程式_______ 。
 、,还含有少量的
、,还含有少量的 、
、 等杂质)制备绿矾(
等杂质)制备绿矾(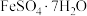 )的流程如下:
)的流程如下:
(1)
 溶液加入赤铁矿中发生反应的离子方程式为
溶液加入赤铁矿中发生反应的离子方程式为(2)试剂
 为
为(3)若取2mL“滤液Ⅰ”加入试管中,然后通入足量CO2,产生的现象是
 酸化的
酸化的 溶液,观察到溶液由浅绿色变成棕黄色,请写出该反应的离子方程式
溶液,观察到溶液由浅绿色变成棕黄色,请写出该反应的离子方程式(4)8.34g
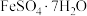 (
(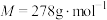 )样品受热分解过程中样品质量随温度变化的曲线如图所示:
)样品受热分解过程中样品质量随温度变化的曲线如图所示:
①温度为78℃时,固体物质M的化学式为
②取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种常见硫的氧化物生成,写出由P生成Q的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】根据如图所示装置 部分仪器已略去
部分仪器已略去 回答下列有关问题。
回答下列有关问题。

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是___________ (填“Ⅰ”或“Ⅱ”),对应的试管中发生反应的化学方程式为___________ ;
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花燃烧。写出Na2O2与CO2反应的化学方程式,并用单线桥法标出电子转移的方向和数目:___________ ;
(3)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的CO2气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为___________ 。
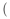 部分仪器已略去
部分仪器已略去 回答下列有关问题。
回答下列有关问题。 
(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花燃烧。写出Na2O2与CO2反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
(3)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的CO2气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】草酸铁晶体Fe2(C2O4)3·xH2O[Fe2(C2O4)3式量为376]通过相关处理后可溶于水,且能做净水剂,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
步骤1:称量4.66g草酸铁晶体进行处理后,配制成250mL一定物质的量浓度的溶液。
步骤2:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时MnO 被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤3:用0.0200mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1mL,滴定中MnO 被还原成Mn2+。
被还原成Mn2+。
重复步骤2、步骤3的操作2次,分别滴定消耗0.0200mol·L-1KMnO4溶液为V2、V3mL。
记录数据如下表:
请回答下列问题:
(1)草酸铁溶液能做净水剂的原因____ (用离子方程式表示)。
(2)该实验步骤1和步骤3中使用的仪器除托盘天平、铁架台、滴定管夹、烧杯、玻璃棒外,一定需用下列仪器中的____ (填序号)。
A.酸式滴定管 B.碱式滴定管 C.250mL容量瓶 D.锥形瓶 E.胶头滴管 F.漏斗
(3)加入锌粉的目的是____ 。
(4)步骤3滴定时是否选择指示剂____ (是或否);写出步骤3中发生反应的离子方程式___ 。
(5)在步骤2中,若加入的KMnO4溶液的量不够,则测得的铁含量__ (填“偏低”、“偏高”或“不变”);实验测得该晶体中结晶水的个数x为___ 。
步骤1:称量4.66g草酸铁晶体进行处理后,配制成250mL一定物质的量浓度的溶液。
步骤2:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时MnO
 被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。步骤3:用0.0200mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1mL,滴定中MnO
 被还原成Mn2+。
被还原成Mn2+。重复步骤2、步骤3的操作2次,分别滴定消耗0.0200mol·L-1KMnO4溶液为V2、V3mL。
记录数据如下表:
| 实验编号 | KMnO4溶液的浓度(mol·L-1) | KMnO4溶液滴入的体积(mL) |
| 1 | 0.0200 | V1=20.02 |
| 2 | 0.0200 | V2=20.12 |
| 3 | 0.0200 | V3=19.98 |
(1)草酸铁溶液能做净水剂的原因
(2)该实验步骤1和步骤3中使用的仪器除托盘天平、铁架台、滴定管夹、烧杯、玻璃棒外,一定需用下列仪器中的
A.酸式滴定管 B.碱式滴定管 C.250mL容量瓶 D.锥形瓶 E.胶头滴管 F.漏斗
(3)加入锌粉的目的是
(4)步骤3滴定时是否选择指示剂
(5)在步骤2中,若加入的KMnO4溶液的量不够,则测得的铁含量
您最近一年使用:0次

 、
、 、
、 和
和 ,为鉴别它们,进行如下实验:
,为鉴别它们,进行如下实验:
 ②+③+⑥:
②+③+⑥:

