由原子序数依次增大的短周期元素W、X、Y、Z、M组成的一种新型刚性建筑防水材料的结构如图所示,下列说法正确的是

A.原子半径: |
B.简单氢化物的沸点: |
C.化合物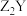 和 和 中阴阳离子的个数比均为 中阴阳离子的个数比均为 |
| D.同周期第一电离能比Y大的元素有2种 |
更新时间:2024-05-12 11:04:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是
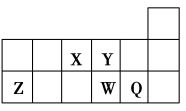

| A.原子半径Y<Z<W |
| B.元素Y的最高正化合价比元素X的最高正化合价高 |
| C.元素W的最高价氧化物对应的水化物的酸性比Q的弱 |
| D.元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列微粒中半径最小的是( )
| A.Ca2+ | B.K+ | C.S2- | D.K |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是
| A.同周期元素中ⅦA族元素的原子半径最大 |
| B.ⅥA族元素的原子,其原子半径越大,越容易得到电子 |
| C.室温时,0族元素的单质都是气体 |
| D.所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素。B元素原子最高能级的不同轨道都有电子,并且自旋方向相同。C元素原子的价层电子排布式nsnnp2n。D元素原子中只有三个能层,最外层只有一种自旋方向的电子。E元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
| A.元素A与B形成化合物,均为气态 |
| B.B、C、D元素第一电离能:C>B>D |
| C.元素C、D形成的化合物中,阴阳离子个数比为1∶2 |
| D.元素C、E只能形成一种黑色化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】我国嫦娥五号探测器带回月球土壤样本,经分析发现其构成与地球土壤类似。土壤中含有短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15,X、Y、Z为同周期相邻元素,且均不与W同族,下列结论正确的是
A.原子半径大小顺序为: | B.Y单质的导电性能弱于Z单质的 |
| C.化合物XW中的化学键为离子键 | D.Z最高价氧化物水化物的酸性强于碳酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】现有三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3。则下列有关比较中正确的是
| A.第一电离能:③>②>① |
| B.原子半径:③>②>① |
| C.电负性:③>②>① |
| D.最高正化合价:③=②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次递增。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D四种元素第一电离能最大的是_______________ 。
(2)B的氯化物的熔点比D的氯化物的熔点__________ (填“高”或“低”),理由是_________________________ 。
(3)A的简单氢化物分子中的中心原子采取_______ 杂化,E的低价氧化物分子的立体构型是_______________ 。用KMnO4酸性溶液吸收该氧化物时,该反应的离子方程式为:_____________________________________________________________ 。
(4)F的核外电子排布式是___________ ,F的高价离子与A的简单氢化物形成的配离子的化学式为____________ 。

(5)A、F形成某种化合物的晶胞结构如图所示(其中A显-3价),若晶胞边长为a pm,阿伏加 德罗常数为NA,则该晶体的密度计算式为ρ=________________ g/cm3。
(1)A、B、C、D四种元素第一电离能最大的是
(2)B的氯化物的熔点比D的氯化物的熔点
(3)A的简单氢化物分子中的中心原子采取
(4)F的核外电子排布式是

(5)A、F形成某种化合物的晶胞结构如图所示(其中A显-3价),若晶胞边长为a pm,阿伏加 德罗常数为NA,则该晶体的密度计算式为ρ=
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】“暖冰”是科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成的。用“暖冰”做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液呈血红色。则下列说法不正确的是( )


| A.该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 |
| B.水凝固形成20℃时的“暖冰”所发生的变化是化学变化 |
| C.该条件下H2燃烧的产物中可能含有一定量的H2O2 |
| D.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是:
①非极性分子中一定含有非极性键;
②S-Sσ键与s-pσ键的电子云形状相同;
③含有π键的化合物与只含σ键的化合物的化学性质不同;
④冰中存在极性共价键和氢键两种化学键的作用
⑤Cu(OH)2是一种蓝色的沉淀,既溶于硝酸、浓硫酸,也能溶于氨水中
⑥氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为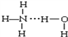
①非极性分子中一定含有非极性键;
②S-Sσ键与s-pσ键的电子云形状相同;
③含有π键的化合物与只含σ键的化合物的化学性质不同;
④冰中存在极性共价键和氢键两种化学键的作用
⑤Cu(OH)2是一种蓝色的沉淀,既溶于硝酸、浓硫酸,也能溶于氨水中
⑥氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为
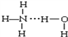
| A.①③⑥ | B.①②⑤ | C.③⑤⑥ | D.②③④ |
您最近一年使用:0次

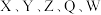 的原子序数依次增大且分占三个短周期,Z原子最外层电子数是内层电子数的3倍,
的原子序数依次增大且分占三个短周期,Z原子最外层电子数是内层电子数的3倍, 与
与 可形成离子个数比为
可形成离子个数比为 的离子化合物,
的离子化合物, 原子在同周期主族元素中原子半径最小,
原子在同周期主族元素中原子半径最小, 的原子序数之和为15,下列判断
的原子序数之和为15,下列判断 与
与
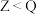
 和
和 均可发生水解反应,其中
均可发生水解反应,其中
 中的N均为
中的N均为 杂化
杂化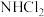 不能和
不能和 形成氢键但是
形成氢键但是

