下列各组热化学方程式中,化学反应的ΔH前者大于后者的有
①H2(g)+F2(g)=2HF(g) ΔH1 H2(g)+Cl2(g)=2HCl(g) ΔH2
②C8H8(l)+ O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+
O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+ O2(g)=8CO2(g)+9H2O(l) ΔH4
O2(g)=8CO2(g)+9H2O(l) ΔH4
③2N2(g)+6H2(g) 4NH3(g) ΔH5 N2(g)+3H2(g)
4NH3(g) ΔH5 N2(g)+3H2(g) 2NH3(g) ΔH6
2NH3(g) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
⑤NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH9 HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH10
①H2(g)+F2(g)=2HF(g) ΔH1 H2(g)+Cl2(g)=2HCl(g) ΔH2
②C8H8(l)+
 O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+
O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+ O2(g)=8CO2(g)+9H2O(l) ΔH4
O2(g)=8CO2(g)+9H2O(l) ΔH4③2N2(g)+6H2(g)
 4NH3(g) ΔH5 N2(g)+3H2(g)
4NH3(g) ΔH5 N2(g)+3H2(g) 2NH3(g) ΔH6
2NH3(g) ΔH6④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
⑤NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH9 HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH10
| A.2项 | B.3项 | C.4项 | D.5项 |
更新时间:2024-05-12 18:48:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】N2与O2化合生成NO是自然界固氮的重要方式之一。如图显示了该反应中的能量变化。下列说法不正确的是
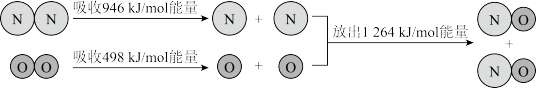

| A.N≡N键的键能大于O=O键的键能 |
| B.该反应中产物所具有的总能量高于反应物所具有的总能量 |
| C.完全断开1molNO中的化学键需吸收1264kJ能量 |
| D.生成NO的热化学方程式为:N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列热化学反应方程式书写正确的是:
| A.乙醇的燃烧热为1366.8 kJ/mol:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H=-1366.8kJ/mol |
| B.1 mol H2(g)与适量O2(g)反应生成H2O(g),放出241.8 kJ热量:2H2(g)+O2(g)=2H2O(g) △H=-241.8 kJ/mol |
| C.1 mol N2(g)与适量O2(g)反应生成NO2(g),吸收68 kJ热量:N2(g)+2O2(g)=2NO2(g) △H=+68 kJ/mol |
| D.中和热为57.3 kJ/mol:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) △H=-57.3 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol现有下列反应
(1)H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O (l);
(2)H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O (l):
(3)HCl(aq)+NH3·H2O(aq)=NH4C1(aq)+H2O (l);
(4)HCl(aq)+浓NaOH(aq)=NaCl(aq)+H2O (l);
其中反应热符合△H=-57.3kJ/mol的是
(1)H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O (l);
(2)H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O (l):
(3)HCl(aq)+NH3·H2O(aq)=NH4C1(aq)+H2O (l);
(4)HCl(aq)+浓NaOH(aq)=NaCl(aq)+H2O (l);
其中反应热符合△H=-57.3kJ/mol的是
| A.(1)(2) | B.(2)(3) | C.(3)(4) | D.都不符合 |
您最近一年使用:0次
【推荐2】探究小组在25℃和101kPa下进行中和热测定,取用 的盐酸和
的盐酸和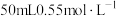 的NaOH溶液(密度均为
的NaOH溶液(密度均为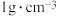 )。实验数据如下:已知:中和后生成的溶液的比热容为
)。实验数据如下:已知:中和后生成的溶液的比热容为 ,该实验条件下,中和热的理论值为
,该实验条件下,中和热的理论值为 。下列说法不正确的是
。下列说法不正确的是
 的盐酸和
的盐酸和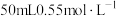 的NaOH溶液(密度均为
的NaOH溶液(密度均为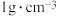 )。实验数据如下:已知:中和后生成的溶液的比热容为
)。实验数据如下:已知:中和后生成的溶液的比热容为 ,该实验条件下,中和热的理论值为
,该实验条件下,中和热的理论值为 。下列说法不正确的是
。下列说法不正确的是| 实验序号 | 起始温度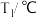 | 终止温度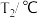 | 温度差 | ||
| HCl | NaOH | 平均值 | |||
| 1 | 25.4 | 25.0 | 25.2 | 28.5 | 3.3 |
| 2 | 24.5 | 24.5 | 24.5 | 27.5 | 3.0 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
| A.该实验计算出中和热的平均值低于理论值 |
| B.造成实验误差的原因可能是溶液混合后未及时盖好量热计杯盖 |
| C.实验时,可用0.25mol·L-1的稀硫酸代替盐酸 |
| D.实验中,NaOH溶液用量越大,所测中和热数值越大 |
您最近一年使用:0次
【推荐1】下列说法正确的是( )
A.若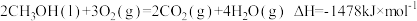 ,则CH3OH(l)的燃烧热为739kJ·mol-1 ,则CH3OH(l)的燃烧热为739kJ·mol-1 |
B.已知25℃、101KPa 下,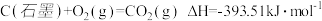 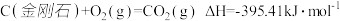 ,则石墨比金刚石更稳定 ,则石墨比金刚石更稳定 |
C.已知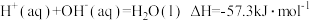 ,则20.0gNaOH固体与稀盐酸完全中和,放出28.65kJ的热量 ,则20.0gNaOH固体与稀盐酸完全中和,放出28.65kJ的热量 |
| D.中和热测定实验中,不可用环形铜质搅拌棒代替环形玻璃搅拌棒,实验至少需测3次温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:(1)H2O(g)=H2O(l) △H1=-Q1kJ/mol
(2)CH3OH(g)=CH3OH(l) △H2=-Q2kJ/mol
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H3=-Q3kJ/mol
Q1、Q2、Q3均大于0.若要使32g液态甲醇完全燃烧并恢复到室温,放出的热量为( )
(2)CH3OH(g)=CH3OH(l) △H2=-Q2kJ/mol
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H3=-Q3kJ/mol
Q1、Q2、Q3均大于0.若要使32g液态甲醇完全燃烧并恢复到室温,放出的热量为( )
| A.Q1+Q2+Q3 | B.5Q3+Q2-2Q1 |
| C.0.5Q3-Q2+2Q1 | D.0.5(Q1+Q2+Q3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.燃烧热的数值都会随反应物的用量不同而改变,故1mol S(s)和2mol S(s)的燃烧热不相等 |
| B.已知:2C(s)+2O2(g)=2CO2(g)ΔH=akJ/mol;2C(s)+2O2(g)=2CO(g)ΔH=bkJ/mol 则a>b |
| C.H2(g)的燃烧热为285.8kJ/mol,则表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol |
| D.反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ/mol,在低温条件下不能自发进行,但在高温条件下能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据热化学方程式:S(s)+O2(g)==SO2(g) ΔH=a kJ·mol-1(a=-297.2)。S相对原子质量为32,分析下列说法,其中不正确的是( )
| A.S(s)在O2(g)中燃烧的反应是放热反应 |
| B.S(g)+O2(g)==SO2(g) ΔH=b kJ·mol-1,则a>b |
| C.1 mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)具有的能量之和 |
| D.16 g固态硫在空气中充分燃烧,可吸收148.6 kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的是
| A.含20.0gNaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示中和反应反应热的热化学方程式为:2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.8kJ/mol |
| B.已知C2H5OH(1)的燃烧热是1366.8kJ/mol,则C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)反应的△H=-1366.8kJ/mol |
C.一定条件下2SO2(g)+O2(g) 2SO3(g) △H1,2SO2(g)+O2(g) 2SO3(g) △H1,2SO2(g)+O2(g) 2SO3(l) △H2,则△H1>△H2 2SO3(l) △H2,则△H1>△H2 |
D.在一定温度和压强下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ/mol 2NH3(g) △H=-38.6kJ/mol |
您最近一年使用:0次

 在空气中完全燃烧,生成
在空气中完全燃烧,生成 和液态水,放出39.75kJ热量,则燃烧的热化学方程式为
和液态水,放出39.75kJ热量,则燃烧的热化学方程式为






 (1)时放出的热量是
(1)时放出的热量是
 的数值偏小
的数值偏小 异丁烷
异丁烷
 ,则正丁烷比异丁烷稳定
,则正丁烷比异丁烷稳定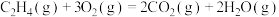
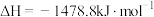 ,则
,则 的燃烧热为
的燃烧热为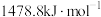

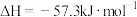 ,则稀
,则稀 和稀
和稀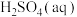 完全反应生成
完全反应生成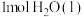 时,放出57.3kJ热量
时,放出57.3kJ热量
 ;
;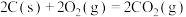
 ,则
,则