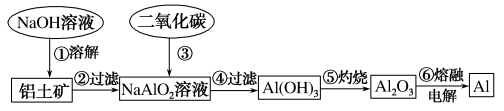
(过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧化系漂白剂,是碳酸钠和过氧化氢形成的不稳定加合物,易溶于水,难溶于乙醇。制备相关资料如下。
(过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧化系漂白剂,是碳酸钠和过氧化氢形成的不稳定加合物,易溶于水,难溶于乙醇。制备相关资料如下。制备装置:如图所示。
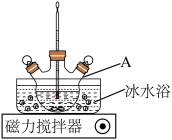
i.按图组装仪器,控制实验温度不超过15℃;
ii.往A中加入25mL的过氧化氢(质量分数为30%)、硫酸镁和硅酸钠各0.1g,控温搅拌至所有试剂完全溶解;
iii.冷却至一定温度,加入100mL饱和碳酸钠溶液,搅拌反应30min,静置结晶;
iv.利用真空泵抽滤,滤饼用无水乙醇洗涤2~3次,通风橱风干得到产品过碳酸钠,滤液回收利用。
回答下列问题:
(1)仪器A的名称为
(2)制备过程中,为了避免温度升高,导致产率下降,“加入100mL饱和碳酸钠溶液”的正确方法是
(3)步骤iv用无水乙醇洗涤的原因是
(4)下列有关过碳酸钠说法错误的是___________。
| A.过碳酸钠是一种混合物 |
| B.过碳酸钠既具有碳酸钠的性质,又具有双氧水性质 |
| C.往酸性高锰酸钾溶液中加入足量过碳酸钠,溶液褪成无色 |
| D.过碳酸钠既可用作绿色漂白剂也可用作鱼塘供氧剂 |
(5)采用下列装置验证过碳酸钠中碳酸钠和过氧化氢的物质的量之比是2∶3(不考虑过碳酸钠含有杂质)。
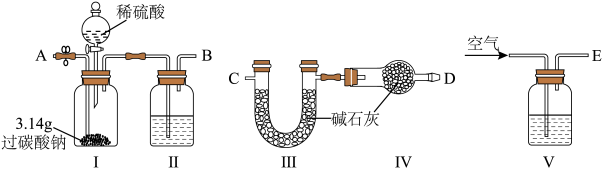
 中的试剂为
中的试剂为②装置接口的连接顺序为
③若实验操作准确,则装置
 理论上应增重
理论上应增重
更新时间:2024-05-29 20:26:30
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】一种利用含AgCl的废渣制取AgNO3的工艺流程如下:
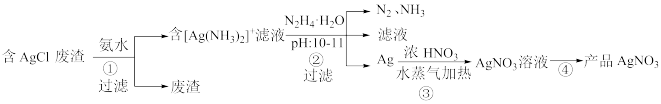
(1)步骤①用氨水浸取时,温度不宜超过35℃,其原因是___ 。在氨水浓度、固液质量比和温度均一定时,为提高银的浸取率还可采取的措施是____ ;浸取时发生反应的离子方程式为____ 。
(2)步骤②中发生反应的离子方程式为______ 。
(3)步骤③中,银与浓硝酸反应生成等物质的量的NO和NO2,当消耗了10.8g Ag时,有______ molHNO3参与了反应。
(4)步骤④的操作为______ ,100℃下烘干得产品AgNO3。
(5)上述流程中发生了氧化还原反应的步骤有______ (用“①”“②”“③”“④”填空)。
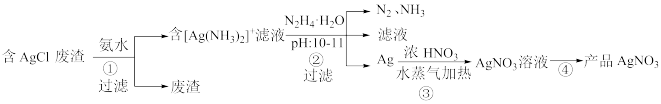
(1)步骤①用氨水浸取时,温度不宜超过35℃,其原因是
(2)步骤②中发生反应的离子方程式为
(3)步骤③中,银与浓硝酸反应生成等物质的量的NO和NO2,当消耗了10.8g Ag时,有
(4)步骤④的操作为
(5)上述流程中发生了氧化还原反应的步骤有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示:

已知: ①Al3+、Al(OH)3、AlO2-有如下转化关系: ;
;
②碳酸不能溶解Al(OH)3。
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是_______________ 。
(2)溶液2中含有的金属阳离子是_______ ;气体2的成分是________ 。
(3)溶液2转化为固体3的反应的离子方程式是__________ 。
(4)固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4,并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是_____________ 。
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是____________ 。
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是____________ 。
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是_____________ 。

已知: ①Al3+、Al(OH)3、AlO2-有如下转化关系:
 ;
;②碳酸不能溶解Al(OH)3。
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是
(2)溶液2中含有的金属阳离子是
(3)溶液2转化为固体3的反应的离子方程式是
(4)固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4,并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】[Co(NH3)6]Cl3(三氯化六氨合钴)属于经典配合物,实验室以Co为原料制备[Co(NH3)6]Cl3的方法和过程如下:
I.制备CoCl2
已知:钴单质与氯气在加热条件下反应可制得纯净CoCl2,钴单质在300℃以上易被氧气氧化;CoCl2熔点为86℃,易潮解。制备装置如图:

(1)试剂X通常是_______ (填名称)。
(2)试剂Z的作用为_______ 。
(3)为了获得更纯净的CoCl2,开始点燃N处酒精喷灯的标志是_______ 。
II.制备[Co(NH3)6]Cl3——配合、氧化
已知:①Co2+不易被氧化;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3在水中的溶解度曲线如图所示:

③加入少量浓盐酸有利于[Co(NH3)6]Cl3析出。
(4)按图组装好装置→_______(填序号,下同)→打开磁力搅拌器→控制温度在10℃以下→_______→_______→加热至60℃左右,恒温20min→在冰水中冷却所得混合物,即有晶体析出(粗产品)。_______

①缓慢加入H2O2溶液
②滴加稍过量的浓氨水
③向三颈烧瓶中加入活性炭、CoCl2、NH4Cl和适量水
(5)氧化阶段发生反应的离子方程式为_______ 。
(6)粗产品可用重结晶法提纯:向粗产品中加入80℃左右的热水,充分搅拌后,______ ,冷却后向滤液中加入少量_______ ,边加边搅拌,充分静置后过滤,用无水乙醇洗涤晶体2~3次,低温干燥,得纯产品[Co(NH3)6]Cl3。
I.制备CoCl2
已知:钴单质与氯气在加热条件下反应可制得纯净CoCl2,钴单质在300℃以上易被氧气氧化;CoCl2熔点为86℃,易潮解。制备装置如图:

(1)试剂X通常是
(2)试剂Z的作用为
(3)为了获得更纯净的CoCl2,开始点燃N处酒精喷灯的标志是
II.制备[Co(NH3)6]Cl3——配合、氧化
已知:①Co2+不易被氧化;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3在水中的溶解度曲线如图所示:

③加入少量浓盐酸有利于[Co(NH3)6]Cl3析出。
(4)按图组装好装置→_______(填序号,下同)→打开磁力搅拌器→控制温度在10℃以下→_______→_______→加热至60℃左右,恒温20min→在冰水中冷却所得混合物,即有晶体析出(粗产品)。

①缓慢加入H2O2溶液
②滴加稍过量的浓氨水
③向三颈烧瓶中加入活性炭、CoCl2、NH4Cl和适量水
(5)氧化阶段发生反应的离子方程式为
(6)粗产品可用重结晶法提纯:向粗产品中加入80℃左右的热水,充分搅拌后,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】是中学重要的试剂。某小组以重晶石为原料制备氯化钡晶体。
实验(一)制备BaS并验证其气体产物(装置如图)。
主反应: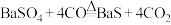
副反应:
(1)通入CO之前,先通入一段时间 ,这样操作的目的是
,这样操作的目的是_______ 。
(2)从a、b、c、d中选择合适的一组试剂:_______ (填标号)。
实验(二)制备 (装置如图)。
(装置如图)。_______ ,实验过程中观察到烧杯中产生黑色沉淀,写出相应的离子方程式为_______ 。
(4)实验完毕后,从 溶液中分离产品的操作是蒸发浓缩、
溶液中分离产品的操作是蒸发浓缩、_______ 、过滤、洗涤、低温干燥。
(5)实验室用11.65g (摩尔质量为233
(摩尔质量为233 )最终制得,9.76g
)最终制得,9.76g (摩尔质量为244
(摩尔质量为244 ),则该过程中Ba的损耗率为
),则该过程中Ba的损耗率为_______ 。
实验(一)制备BaS并验证其气体产物(装置如图)。

主反应:
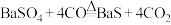
副反应:

(1)通入CO之前,先通入一段时间
 ,这样操作的目的是
,这样操作的目的是(2)从a、b、c、d中选择合适的一组试剂:
| B | C | D | E | |
| a | 品红溶液 | NaOH溶液 | 澄清石灰水 | 溴水 |
| b | 溴水 | 品红溶液 | 澄清石灰水 | 酸性高锰酸钾溶液 |
| c | 酸性高锰酸钾溶液 | 溴水 | NaOH溶液 | 品红溶液 |
| d | 品红溶液 | 溴水 | 品红溶液 | 澄清石灰水 |
实验(二)制备
 (装置如图)。
(装置如图)。
(4)实验完毕后,从
 溶液中分离产品的操作是蒸发浓缩、
溶液中分离产品的操作是蒸发浓缩、(5)实验室用11.65g
 (摩尔质量为233
(摩尔质量为233 )最终制得,9.76g
)最终制得,9.76g (摩尔质量为244
(摩尔质量为244 ),则该过程中Ba的损耗率为
),则该过程中Ba的损耗率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】地球上的氮元素对动植物有重要作用,其中氨的合成与应用是当前的研究热点。
(1)人工固氮最主要的方法是Haber-Bosch法。通常用以铁为主的催化剂在400~500℃和10~30MPa的条件下,由氮气和氢气直接合成氨。写出反应的化学方程式___ 。
(2)如图所示为实验装置模拟工业生产制备少量硝酸。

①实验室制取氨气的化学方程式是___ ;检验氨气的方法为___ 。
②实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上,由此可知该反应是___ 反应(填“吸热”或“放热”),反应的化学方程式是____ 。
③B中试剂为____ ,NaOH溶液的作用是___ 。
④控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是__ ,白烟的化学式是___ 。欲使氨气尽可能完全转化为硝酸,理论上n(NH3):n(O2)的最佳比例为___ 。
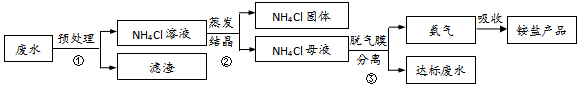
(3)某氨氮废水资源化利用和处理的流程如图所示(部分物质已略去)。
①预处理过程中需要去除硫酸根,可选用的试剂是___ 。
②蒸发结晶过程中不宜温度过高,其原因是___ (用化学方程式表示)。
③在脱气膜分离过程中,调控膜内pH可以分离出NH3,NH3再与吸收液反应得到铵盐产品。请写出调节pH分离得到NH3的离子方程式____ 。
④上述流程中,包含过滤的分离操作是___ (填序号)。
(1)人工固氮最主要的方法是Haber-Bosch法。通常用以铁为主的催化剂在400~500℃和10~30MPa的条件下,由氮气和氢气直接合成氨。写出反应的化学方程式
(2)如图所示为实验装置模拟工业生产制备少量硝酸。

①实验室制取氨气的化学方程式是
②实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上,由此可知该反应是
③B中试剂为
④控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是
(3)某氨氮废水资源化利用和处理的流程如图所示(部分物质已略去)。

①预处理过程中需要去除硫酸根,可选用的试剂是
②蒸发结晶过程中不宜温度过高,其原因是
③在脱气膜分离过程中,调控膜内pH可以分离出NH3,NH3再与吸收液反应得到铵盐产品。请写出调节pH分离得到NH3的离子方程式
④上述流程中,包含过滤的分离操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】次硫酸氢钠甲醛(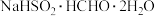 ,其相对分子质量为154)俗称吊白块,在空气中易被氧化,120℃时会分解,在印染、医药及原子能工业中应用广泛。某实验小组以浓
,其相对分子质量为154)俗称吊白块,在空气中易被氧化,120℃时会分解,在印染、医药及原子能工业中应用广泛。某实验小组以浓 、
、 、HCHO和Zn为原料制备次硫酸氢钠甲醛。回答下列问题:
、HCHO和Zn为原料制备次硫酸氢钠甲醛。回答下列问题:
(1)制备 :实验室常用
:实验室常用 与浓
与浓 反应制取
反应制取 。
。
① 分子的空间结构为
分子的空间结构为___________ 。
②工业生产中常用氨水处理废气中 ,写出足量氨水吸收
,写出足量氨水吸收 的离子方程式:
的离子方程式:___________ 。
(2)制备 溶液:在三颈烧瓶中加入一定量
溶液:在三颈烧瓶中加入一定量 固体和
固体和 ,搅拌溶解,再缓慢通入
,搅拌溶解,再缓慢通入 ,实验装置如图所示(夹持仪器已省略)。
,实验装置如图所示(夹持仪器已省略)。 溶液吸收
溶液吸收 的过程中,
的过程中,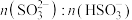 及
及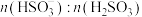 等于1时,溶液的pH分别为7.2、2。
等于1时,溶液的pH分别为7.2、2。
①装置E的作用是___________ ,装置X的名称为___________ 。
②常温下,当溶液中 时,溶液的pH为
时,溶液的pH为___________ 。
(3)制备次硫酸氢钠甲醛:(2)中充分反应后,将装置D中导气管换成橡皮塞,向三颈烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤。
①生成 [副产物为
[副产物为 ]时发生反应的化学方程式为
]时发生反应的化学方程式为___________ 。
②将上述抽滤所得的滤液经___________ 步骤,过滤得到产品。
(4)测定产品的纯度:准确称取8.0 g产品,完全溶于水配成100 mL溶液,取20.00 mL所配溶液,加入过量碘完全反应后(已知 不能氧化甲醛,S元素转化为
不能氧化甲醛,S元素转化为 ,杂质不反应),加入
,杂质不反应),加入 溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体2.33 g。产品的纯度为
溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体2.33 g。产品的纯度为___________ 。
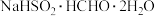 ,其相对分子质量为154)俗称吊白块,在空气中易被氧化,120℃时会分解,在印染、医药及原子能工业中应用广泛。某实验小组以浓
,其相对分子质量为154)俗称吊白块,在空气中易被氧化,120℃时会分解,在印染、医药及原子能工业中应用广泛。某实验小组以浓 、
、 、HCHO和Zn为原料制备次硫酸氢钠甲醛。回答下列问题:
、HCHO和Zn为原料制备次硫酸氢钠甲醛。回答下列问题:(1)制备
 :实验室常用
:实验室常用 与浓
与浓 反应制取
反应制取 。
。①
 分子的空间结构为
分子的空间结构为②工业生产中常用氨水处理废气中
 ,写出足量氨水吸收
,写出足量氨水吸收 的离子方程式:
的离子方程式:(2)制备
 溶液:在三颈烧瓶中加入一定量
溶液:在三颈烧瓶中加入一定量 固体和
固体和 ,搅拌溶解,再缓慢通入
,搅拌溶解,再缓慢通入 ,实验装置如图所示(夹持仪器已省略)。
,实验装置如图所示(夹持仪器已省略)。
 溶液吸收
溶液吸收 的过程中,
的过程中,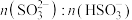 及
及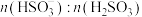 等于1时,溶液的pH分别为7.2、2。
等于1时,溶液的pH分别为7.2、2。①装置E的作用是
②常温下,当溶液中
 时,溶液的pH为
时,溶液的pH为(3)制备次硫酸氢钠甲醛:(2)中充分反应后,将装置D中导气管换成橡皮塞,向三颈烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤。
①生成
 [副产物为
[副产物为 ]时发生反应的化学方程式为
]时发生反应的化学方程式为②将上述抽滤所得的滤液经
(4)测定产品的纯度:准确称取8.0 g产品,完全溶于水配成100 mL溶液,取20.00 mL所配溶液,加入过量碘完全反应后(已知
 不能氧化甲醛,S元素转化为
不能氧化甲醛,S元素转化为 ,杂质不反应),加入
,杂质不反应),加入 溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体2.33 g。产品的纯度为
溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体2.33 g。产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】ClO2是一种优良的消毒剂,其溶解度约是Cl2的5倍,但温度过高浓度过大时均易发生分解,因此常将其制成KClO2固体,以便运输和贮存。制备KClO2固体的实验装置如图所示,其中A装置制备ClO2,B装置制备KClO2。请回答下列问题:

(1)A中制备ClO2的化学方程式为__ 。
(2)与分液漏斗相比,本实验使用滴液漏斗,其优点是__ 。加入H2SO4需用冰盐水冷却,是为了防止液体飞溅和__ 。
(3)实验过程中通入空气的目的是__ ,空气流速过快,会降低KClO2产率,试解释其原因__ 。
(4)ClO2通入KOH溶液生成KClO2的同时还有可能生成的物质__ 。
a.KCl b.KClO c.KClO3 d.KClO4
(5)KClO2变质分解为KClO3和KCl,取等质量的变质前后的KClO2试样配成溶液,分别与足量的FeSO4溶液反应消耗Fe2+的物质的量__ (填“相同”、“不相同”“无法确定”)。

(1)A中制备ClO2的化学方程式为
(2)与分液漏斗相比,本实验使用滴液漏斗,其优点是
(3)实验过程中通入空气的目的是
(4)ClO2通入KOH溶液生成KClO2的同时还有可能生成的物质
a.KCl b.KClO c.KClO3 d.KClO4
(5)KClO2变质分解为KClO3和KCl,取等质量的变质前后的KClO2试样配成溶液,分别与足量的FeSO4溶液反应消耗Fe2+的物质的量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯乙酸(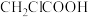 )是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法是用纯的
)是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法是用纯的 与冰醋酸在催化剂的作用下发生反应:
与冰醋酸在催化剂的作用下发生反应: ,已知:
,已知: 易与水反应。某课外兴趣小组的同学用下图所示装置进行合成氯乙酸的实验探究:
易与水反应。某课外兴趣小组的同学用下图所示装置进行合成氯乙酸的实验探究:
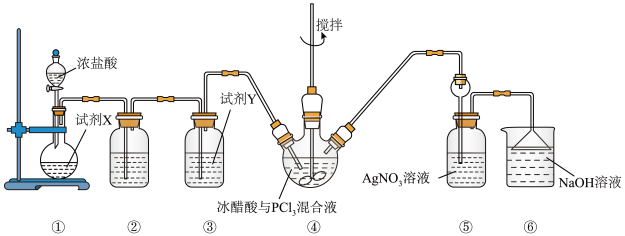
已知:ⅰ、冰醋酸为不含水的纯醋酸;
ⅱ、除上图中给出的试剂外,实验室还提供了 、
、 、
、 、浓硫酸、饱和的
、浓硫酸、饱和的 溶液、饱和的
溶液、饱和的 溶液,供实验小组的同学选用。
溶液,供实验小组的同学选用。
(1)按上图组装好仪器后,在添加药品之前应进行的实验操作是___________ ,装置①中发生反应的化学方程式为___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(2)装置②的作用是___________ ,③中所装试剂Y的名称为___________ 。
(3)本实验___________ (填“能”或“不能”)通过装置⑤中产生白色沉淀这一现象判断该反应中有 生成,原因
生成,原因___________ 。
(4)装置⑥中漏斗的作用:___________ ;请写出⑥中发生反应的离子方程式___________ 。
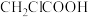 )是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法是用纯的
)是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法是用纯的 与冰醋酸在催化剂的作用下发生反应:
与冰醋酸在催化剂的作用下发生反应: ,已知:
,已知: 易与水反应。某课外兴趣小组的同学用下图所示装置进行合成氯乙酸的实验探究:
易与水反应。某课外兴趣小组的同学用下图所示装置进行合成氯乙酸的实验探究:
已知:ⅰ、冰醋酸为不含水的纯醋酸;
ⅱ、除上图中给出的试剂外,实验室还提供了
 、
、 、
、 、浓硫酸、饱和的
、浓硫酸、饱和的 溶液、饱和的
溶液、饱和的 溶液,供实验小组的同学选用。
溶液,供实验小组的同学选用。(1)按上图组装好仪器后,在添加药品之前应进行的实验操作是
(2)装置②的作用是
(3)本实验
 生成,原因
生成,原因(4)装置⑥中漏斗的作用:
您最近一年使用:0次