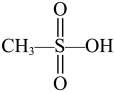
物质结构决定物质性质。下列性质差异与结构因素匹配不正确的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:HF>HI | 氢键 |
| B | 熔点:Na>K | 原子半径 |
| C | 硬度:金刚石>SiC | 晶体类型 |
| D | I2在溶剂中的溶解度:CCl4>H2O | 分子的极性 |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-19 18:52:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】研究表明,结构中含有 、
、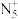 的含氮含能材料如
的含氮含能材料如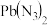 、
、 均可以用于炸药。下列说法正确的是
均可以用于炸药。下列说法正确的是
 、
、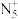 的含氮含能材料如
的含氮含能材料如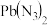 、
、 均可以用于炸药。下列说法正确的是
均可以用于炸药。下列说法正确的是| A.Pb属于副族元素 | B. 的空间构型为直线形 的空间构型为直线形 |
| C.基态As原子核外最高能级电子云形状为球形 | D.基态F原子中,电子运动状态有7种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关表述正确的是
⑴-OH 与 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
⑵sp2杂化轨道:
⑶Fe2+的离子结构示意图:
⑷CO2的分子模型示意图:
⑸丙烷的分子结构模型示意图:
⑹次氯酸的电子式为
⑺ 名称为1,3-二甲基-2-丁 烯
名称为1,3-二甲基-2-丁 烯
⑻熔化时NaHSO4的电离方程式为NaHSO4=Na++HSO4-
⑼乙炔的最简式 CH≡CH
⑴-OH 与
 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同⑵sp2杂化轨道:

⑶Fe2+的离子结构示意图:

⑷CO2的分子模型示意图:

⑸丙烷的分子结构模型示意图:

⑹次氯酸的电子式为

⑺
 名称为1,3-二甲基-2-丁 烯
名称为1,3-二甲基-2-丁 烯⑻熔化时NaHSO4的电离方程式为NaHSO4=Na++HSO4-
⑼乙炔的最简式 CH≡CH
| A.(1)(2)(4)(6) | B.(2)(3)(5) | C.(1)(4)(5)(8) | D.(1)(2)(5)(8) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的是
| A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构; |
| B.P4和CH4都是正四面体分子且键角都为109o28ˊ; |
| C.CO2、SO2都是直线形的分子 |
| D.CH2=CH2分子中共有五个σ键和一个π键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是( )
| A.沸点高低:CH4>SiH4>GeH4 |
| B.键角大小:BeCl2>BF3>NH3>H2O |
| C.熔点高低:金刚石>石墨>食盐 |
| D.键能大小:O-H>P-H>S-H |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的大π键,下列说法错误的是
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的大π键,下列说法错误的是
 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的大π键,下列说法错误的是
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的大π键,下列说法错误的是| A.吡啶为极性分子 |
| B.吡啶显碱性,能与酸反应 |
C.吡啶中N原子的价层孤电子对占据 杂化轨道 杂化轨道 |
| D.在水中的溶解度,吡啶远大于苯 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关叙述正确的是
A.在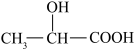 分子中含有1个手性C原子 分子中含有1个手性C原子 |
| B.氢键是一种特殊化学键,它广泛地存在于自然界中 |
| C.碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子 |
| D.含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】周期表中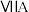 族元素及其化合物应用广泛。电解
族元素及其化合物应用广泛。电解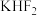 与
与 的混合物时,
的混合物时, 转化为
转化为 ;加热
;加热 与浓
与浓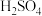 的混合物,可制得
的混合物,可制得 。氯还可形成
。氯还可形成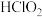 、
、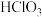 、
、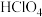 等多种含氧酸。
等多种含氧酸。 是
是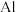 级高效安全灭菌消毒剂;
级高效安全灭菌消毒剂;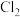 与
与 反应可制备有机溶剂
反应可制备有机溶剂 。在照相底片的定影过程中,底片上未曝光的
。在照相底片的定影过程中,底片上未曝光的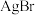 浸入
浸入 溶液转变成
溶液转变成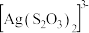 而溶解。氯化碘
而溶解。氯化碘 性质与卤素单质相似,常用作分析化学试剂。下列物质结构与性质或物质性质与用途
性质与卤素单质相似,常用作分析化学试剂。下列物质结构与性质或物质性质与用途不具有 对应关系的是
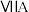 族元素及其化合物应用广泛。电解
族元素及其化合物应用广泛。电解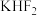 与
与 的混合物时,
的混合物时, 转化为
转化为 ;加热
;加热 与浓
与浓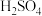 的混合物,可制得
的混合物,可制得 。氯还可形成
。氯还可形成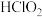 、
、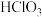 、
、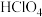 等多种含氧酸。
等多种含氧酸。 是
是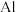 级高效安全灭菌消毒剂;
级高效安全灭菌消毒剂;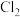 与
与 反应可制备有机溶剂
反应可制备有机溶剂 。在照相底片的定影过程中,底片上未曝光的
。在照相底片的定影过程中,底片上未曝光的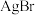 浸入
浸入 溶液转变成
溶液转变成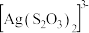 而溶解。氯化碘
而溶解。氯化碘 性质与卤素单质相似,常用作分析化学试剂。下列物质结构与性质或物质性质与用途
性质与卤素单质相似,常用作分析化学试剂。下列物质结构与性质或物质性质与用途A.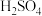 分子间存在氢键,呈粘稠状 分子间存在氢键,呈粘稠状 |
B. 具有强氧化性,可用作灭菌消毒剂 具有强氧化性,可用作灭菌消毒剂 |
C. 为正四面体形分子,具有可燃性 为正四面体形分子,具有可燃性 |
D.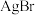 见光易分解,可用作感光材料 见光易分解,可用作感光材料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法不正确 的是
| A.键角:H2O<NH3 | B.键长:Cl-Cl<Br-Br |
| C.酸性:CH3COOH<CH2ClCOOH | D.沸点:对羟基苯甲醛<邻羟基苯甲醛 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某电池材料结构如图所示。X、Y、Z、M、W为同周期主族元素。X原子的最外层电子数是W原子次外层电子数的3倍,下列说法正确的是


| A.M的单质可以保存在煤油中 |
| B.该电池材料中存在离子键、极性键、非极性键、配位键 |
C.氢化物的沸点为 |
D.原子半径为 |
您最近一年使用:0次

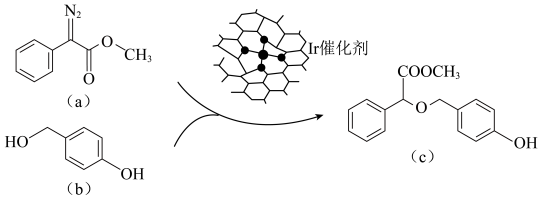
 ,则Ir属于第Ⅷ族元素
,则Ir属于第Ⅷ族元素