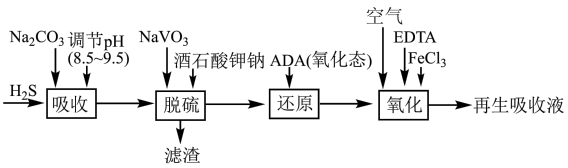
蒽醌二磺酸钠法(ADA法)对合成氨原料气进行脱硫(H2S)的工艺流程如图所示,该工艺的优势之一在于只要向“再生吸收液”不断通如空气即可实现连续吸收H2S气体。
ii.酒石酸钾钠、EDTA可分别与V4+、Fe3+形成可溶性配合物。
(1)“吸收”时,发生反应的离子方程式为___________ 。
(2)“脱硫”时,NaVO3先转化为Na2V4O9同时可得到S,则该转化过程反应的化学方程式为___________ 。
(3)“还原”时,氧化态ADA(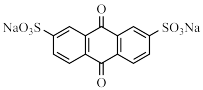 )转化为还原态ADA(
)转化为还原态ADA(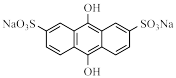 ),同时NaVO3得以再生。该转化过程需要消耗NaOH,但该工艺中并没有再加入该试剂的原因为
),同时NaVO3得以再生。该转化过程需要消耗NaOH,但该工艺中并没有再加入该试剂的原因为___________ ,Na2V4O9参与反应过程中氧化剂和还原剂的物质的量之比为___________ 。
(4)“氧化”时,ADA(还原态)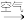 ADA(氧化态),同时有H2O2生成。从氧化还原反应角度分析,FeCl3的作用可能是
ADA(氧化态),同时有H2O2生成。从氧化还原反应角度分析,FeCl3的作用可能是___________ ;加入EDTA的目的是___________ 。
(5)“再生吸收液”中可循环使用的物质有___________ (填选项字母)。
A.NaOH B.酒石酸钾钠 C.NaVO3 D.EDTA E.ADA
ii.酒石酸钾钠、EDTA可分别与V4+、Fe3+形成可溶性配合物。
(1)“吸收”时,发生反应的离子方程式为
(2)“脱硫”时,NaVO3先转化为Na2V4O9同时可得到S,则该转化过程反应的化学方程式为
(3)“还原”时,氧化态ADA(
 )转化为还原态ADA(
)转化为还原态ADA( ),同时NaVO3得以再生。该转化过程需要消耗NaOH,但该工艺中并没有再加入该试剂的原因为
),同时NaVO3得以再生。该转化过程需要消耗NaOH,但该工艺中并没有再加入该试剂的原因为(4)“氧化”时,ADA(还原态)
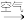 ADA(氧化态),同时有H2O2生成。从氧化还原反应角度分析,FeCl3的作用可能是
ADA(氧化态),同时有H2O2生成。从氧化还原反应角度分析,FeCl3的作用可能是(5)“再生吸收液”中可循环使用的物质有
A.NaOH B.酒石酸钾钠 C.NaVO3 D.EDTA E.ADA
更新时间:2024-05-22 10:25:51
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】某学生对固体A(两种元素组成的纯净物)进行了如下实验。已知C在医疗上可以用作检查肠胃的内服药剂,不易被X射线透过。
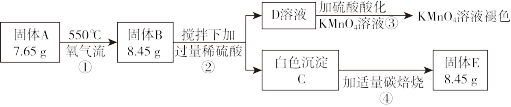
请回答:
(1)固体A的化学式是___________ ,步骤③的离子反应方程式是___________ 。
(2)写出步骤④的化学反应方程式:___________
(3)物质F由硫、氯两种元素组成,与D中某种溶质分子具有相同的空间结构,其结构式为___________ , F能与水反应产生淡黄色沉淀与刺激性气味气体,将少量该气体分别通入不含O2的25mL0.1mol/L BaCl2溶液、不含O2的25ml 0.1mol/L Ba(NO3)2溶液中,溶液pH变化前者___________ 后者(填“>”、“<”或“=”),原因是(用离子方程式表示) ___________
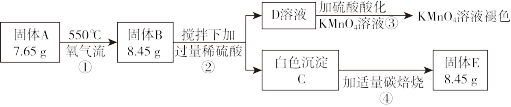
请回答:
(1)固体A的化学式是
(2)写出步骤④的化学反应方程式:
(3)物质F由硫、氯两种元素组成,与D中某种溶质分子具有相同的空间结构,其结构式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】高铁酸钾( )是新型多功能水处理剂,其生产工艺如图所示:
)是新型多功能水处理剂,其生产工艺如图所示:
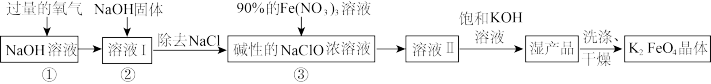
已知:
① 与NaOH溶液反应的产物与反应温度有关,温度较低时产物为NaCl、NaClO和
与NaOH溶液反应的产物与反应温度有关,温度较低时产物为NaCl、NaClO和 ;温度较高时产物为NaCl、
;温度较高时产物为NaCl、 和
和 。
。
②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出 与NaOH溶液在较高温度下反应的离子方程式:
与NaOH溶液在较高温度下反应的离子方程式:___________ 。
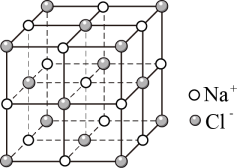
(2)向“溶液Ⅰ”中加入NaOH固体起到的作用有降低NaCl的溶解度___________ 、___________ ;NaCl晶胞结构如图,设晶胞边长为a pm, 为阿伏加德罗常数的值,则距离最近的
为阿伏加德罗常数的值,则距离最近的 间的距离为
间的距离为___________ pm,该晶体的密度为___________ (填含a、 的表达式)
的表达式) 。
。
(3)配制NaOH溶液时,将44g NaOH固体溶解在100mL水中,所得溶液的密度为1.33 ,则该溶液的物质的量浓度为
,则该溶液的物质的量浓度为___________ (保留1位小数) 。
。
(4)步骤③发生的反应中氧化剂与还原剂的物质的量之比n(氧化剂)∶n(还原剂)=________ 。对“湿产品”进行“洗涤、干燥”时,洗涤剂最好选用________ (填标号)溶液和异丙醇。
A. B.
B. C.
C.
(5)从环境保护的角度看,制备 较好的方法为电解法。维持一定的电流强度和电解温度,KOH起始浓度对
较好的方法为电解法。维持一定的电流强度和电解温度,KOH起始浓度对 浓度的影响如图(电解液体积相同的情况下进行的实验)。
浓度的影响如图(电解液体积相同的情况下进行的实验)。
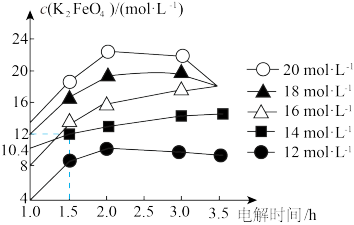
适宜的电解时间应选用___________ h;当KOH起始浓度为14 时,1.0~1.5h内生成
时,1.0~1.5h内生成 的速率是
的速率是___________  。
。
 )是新型多功能水处理剂,其生产工艺如图所示:
)是新型多功能水处理剂,其生产工艺如图所示:
已知:
①
 与NaOH溶液反应的产物与反应温度有关,温度较低时产物为NaCl、NaClO和
与NaOH溶液反应的产物与反应温度有关,温度较低时产物为NaCl、NaClO和 ;温度较高时产物为NaCl、
;温度较高时产物为NaCl、 和
和 。
。②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出
 与NaOH溶液在较高温度下反应的离子方程式:
与NaOH溶液在较高温度下反应的离子方程式:(2)向“溶液Ⅰ”中加入NaOH固体起到的作用有降低NaCl的溶解度
 为阿伏加德罗常数的值,则距离最近的
为阿伏加德罗常数的值,则距离最近的 间的距离为
间的距离为 的表达式)
的表达式) 。
。
(3)配制NaOH溶液时,将44g NaOH固体溶解在100mL水中,所得溶液的密度为1.33
 ,则该溶液的物质的量浓度为
,则该溶液的物质的量浓度为 。
。(4)步骤③发生的反应中氧化剂与还原剂的物质的量之比n(氧化剂)∶n(还原剂)=
A.
 B.
B. C.
C.
(5)从环境保护的角度看,制备
 较好的方法为电解法。维持一定的电流强度和电解温度,KOH起始浓度对
较好的方法为电解法。维持一定的电流强度和电解温度,KOH起始浓度对 浓度的影响如图(电解液体积相同的情况下进行的实验)。
浓度的影响如图(电解液体积相同的情况下进行的实验)。
适宜的电解时间应选用
 时,1.0~1.5h内生成
时,1.0~1.5h内生成 的速率是
的速率是 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)已知A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Cu2+、Na+中的一种,阴离子分别是 、
、 、
、 、Cl-中的一种(离子不能重复),进行如下实验:
、Cl-中的一种(离子不能重复),进行如下实验:
①分别溶于水,只有C溶液呈蓝色;
②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;根据①②的实验事实。可推断它们的化学式为:
a.A___________ ;B ___________ 。
b.写出D的电离方程式:___________ 。
c.以铜为原料,写出能生成C的化学方程式(不限步骤):___________ 。
(2)某校化学兴趣小组同学猜想自来水中可能含有大量Cu2+、Ca2+、Mg2+和某些阴离子,从而进行了三组实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
a.不用做实验就可排除的离子是___________ 。
b.通过实验可初步确定自来水中含有哪些阳离子___________ 。
c.③中产生的白色沉淀是___________ (用化学式表示),理由是___________ 。(用离子方程式表示)。
(1)已知A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Cu2+、Na+中的一种,阴离子分别是
 、
、 、
、 、Cl-中的一种(离子不能重复),进行如下实验:
、Cl-中的一种(离子不能重复),进行如下实验:①分别溶于水,只有C溶液呈蓝色;
②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;根据①②的实验事实。可推断它们的化学式为:
a.A
b.写出D的电离方程式:
c.以铜为原料,写出能生成C的化学方程式(不限步骤):
(2)某校化学兴趣小组同学猜想自来水中可能含有大量Cu2+、Ca2+、Mg2+和某些阴离子,从而进行了三组实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
a.不用做实验就可排除的离子是
b.通过实验可初步确定自来水中含有哪些阳离子
c.③中产生的白色沉淀是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,工业大规模生产前,实验室先按如下流程进行模拟制备少量Mg(ClO3)2·6H2O:
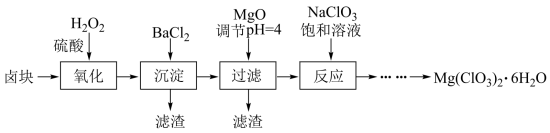
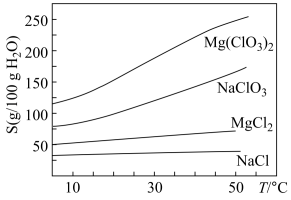
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。②几种化合物的溶解度(S)随温度(T)变化曲线如右图。
(1)卤块中加H2O2的目的是________________ ,写出该反应的离子方程式__________________ 。
(2)加入BaCl2的目的是除去SO ,如何检验SO
,如何检验SO 已沉淀完全?
已沉淀完全?_________________ 。
(3)常温下,加MgO调节pH=4后溶液中c(Fe3+)=___________ (已知Ksp[Fe(OH)3=4×10-38],过滤所得滤渣的主要成分有______________ 。
(4)加入NaClO3饱和溶液公有NaCl晶体析出,写出该反应的化学方程式:___________ ,请利用该反应,结合上图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应;②蒸发结晶;③___________ ;④冷却结晶;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。②几种化合物的溶解度(S)随温度(T)变化曲线如右图。

(1)卤块中加H2O2的目的是
(2)加入BaCl2的目的是除去SO
 ,如何检验SO
,如何检验SO 已沉淀完全?
已沉淀完全?(3)常温下,加MgO调节pH=4后溶液中c(Fe3+)=
(4)加入NaClO3饱和溶液公有NaCl晶体析出,写出该反应的化学方程式:
①取样,加入NaClO3饱和溶液充分反应;②蒸发结晶;③
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】(1)21世纪是钛的世界,纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。工业上二氧化钛的制备是:
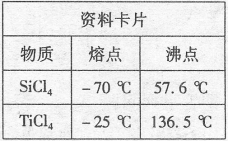
I.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4。
II.将SiCl4分离,得到纯净的TiCl4,所采取的操作名称是_______
III.用TiCl4制备TiO2·xH2O的化学方程式为________________ ,制备时需要________ ,促进水解趋于完全。
IV.TiO2·xH2O高温分解得到TiO2。如在实验室中进行,则需在________ (填仪器名称)中加热。
(2)亚硫酰氯(SOCl2)是一种液态化合物,沸点为77℃,在农药制药等领域用途广泛。SOCl2遇水剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出,该气体可使品红溶液褪色。根据上述实验,写出SOCl2与水反应的化学方程式_________________________________________________ ,AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·6H2O混合共热,可得无水AlCl3,其原因是______________________________

I.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4。
II.将SiCl4分离,得到纯净的TiCl4,所采取的操作名称是
III.用TiCl4制备TiO2·xH2O的化学方程式为
IV.TiO2·xH2O高温分解得到TiO2。如在实验室中进行,则需在
(2)亚硫酰氯(SOCl2)是一种液态化合物,沸点为77℃,在农药制药等领域用途广泛。SOCl2遇水剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出,该气体可使品红溶液褪色。根据上述实验,写出SOCl2与水反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】胆矾( )是一种重要化工原料。某研究小组以生锈的铜屑为原料[主要成分是Cu,含有少量的油污、
)是一种重要化工原料。某研究小组以生锈的铜屑为原料[主要成分是Cu,含有少量的油污、 、
、 、
、 ]制备胆矾,流程如下。
]制备胆矾,流程如下。
回答问题:
(1)进行操作①时,需要用到的玻璃仪器有___________ 。
(2)操作②中,为了加快固体B的溶解速率,可采取的措施有___________ (写出一种合理方法即可)。
(3)操作②中,Cu溶解的化学方程式为___________ 。
(4)经过操作③,能得到胆矾晶体,则操作③的具体操作为___________ 。
(5)经步骤④得到的胆矾附有可溶性杂质,可用___________ 洗涤晶体,减少胆矾晶体的损失。
(6)实验证明,滤液D能将 氧化为
氧化为 。
。
ⅰ.甲同学认为不可能是步骤②中过量 将
将 氧化为
氧化为 ,理由是
,理由是___________ 。
ⅱ.乙同学通过实验证实,只能是 将
将 氧化为
氧化为 ,写出乙同学的实验方案及结果
,写出乙同学的实验方案及结果___________ (不要求写具体操作过程)。
 )是一种重要化工原料。某研究小组以生锈的铜屑为原料[主要成分是Cu,含有少量的油污、
)是一种重要化工原料。某研究小组以生锈的铜屑为原料[主要成分是Cu,含有少量的油污、 、
、 、
、 ]制备胆矾,流程如下。
]制备胆矾,流程如下。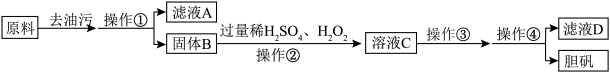
回答问题:
(1)进行操作①时,需要用到的玻璃仪器有
(2)操作②中,为了加快固体B的溶解速率,可采取的措施有
(3)操作②中,Cu溶解的化学方程式为
(4)经过操作③,能得到胆矾晶体,则操作③的具体操作为
(5)经步骤④得到的胆矾附有可溶性杂质,可用
(6)实验证明,滤液D能将
 氧化为
氧化为 。
。ⅰ.甲同学认为不可能是步骤②中过量
 将
将 氧化为
氧化为 ,理由是
,理由是ⅱ.乙同学通过实验证实,只能是
 将
将 氧化为
氧化为 ,写出乙同学的实验方案及结果
,写出乙同学的实验方案及结果
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯化铝融盐电解法是以氯化铝为原料,以碱金属或碱土金属氯化物(含少量MgCl2、KCl、CaCl2)为电解质进行电解制取铝的方法。
(1)氯化铝融盐电解法需要先制纯氧化铝。以铝土矿(主要成分为Al2O3,含有少量Fe2O3、SiO2等杂质)为原料通过以下途径提纯氧化铝:
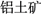
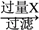
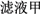


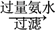
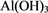
 Al2O3
Al2O3
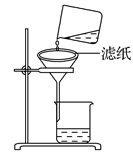
①依次写出X、Y的成分________ ,________ 。
②如右图所示在实验室中进行过滤,操作中的两处错误分别是__________________________ ;____________________________ 。
(2)制备无水氯化铝的反应为:2Al2O3+6Cl2 4AlCl3+3O2
4AlCl3+3O2
③为促进该反应的进行,实际生产中需加入焦炭,其原理是____________________ 。
④加入焦炭后的化学反应可表示为Al2O3+C+Cl2 AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)
AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)________ ,请说明理由_________________________________________________ 。
(3)现在工业上通常用电解熔融氧化铝方式制取铝,理论上生产1吨铝消耗的氧化铝的质量________ (填“大于”、“小于”或“等于”)氯化铝质量。
(1)氯化铝融盐电解法需要先制纯氧化铝。以铝土矿(主要成分为Al2O3,含有少量Fe2O3、SiO2等杂质)为原料通过以下途径提纯氧化铝:


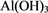
 Al2O3
Al2O3
①依次写出X、Y的成分
②如右图所示在实验室中进行过滤,操作中的两处错误分别是
(2)制备无水氯化铝的反应为:2Al2O3+6Cl2
 4AlCl3+3O2
4AlCl3+3O2③为促进该反应的进行,实际生产中需加入焦炭,其原理是
④加入焦炭后的化学反应可表示为Al2O3+C+Cl2
 AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)
AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)(3)现在工业上通常用电解熔融氧化铝方式制取铝,理论上生产1吨铝消耗的氧化铝的质量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】叶蛇纹石是一种富镁硅酸盐矿物[主要成分为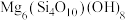 ,还含有
,还含有 、
、 、
、 等杂质],利用该矿物生产铁红(
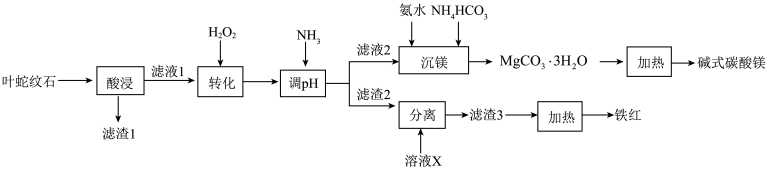
等杂质],利用该矿物生产铁红( )和碱式碳酸镁的工艺流程如图:
)和碱式碳酸镁的工艺流程如图:
常温下部分难溶物的溶度积常数如表:
回答下列问题:
(1)为了加快“酸浸”的速率可采取的措施有_______ (写出两种即可)。
(2)“转化”过程中 参与反应的离子方程式为
参与反应的离子方程式为_______ 。
(3)分离滤渣2时,溶液X通常选用_______ (填化学式);在实验室中加热滤渣3需用到的仪器有_______ 、三脚架和泥三角。
(4)“沉镁”过程中发生反应的离子方程式为_______ 。该过程中加入氨水的量不能太多,否则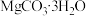 的产率会降低,原因是
的产率会降低,原因是_______ 。
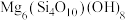 ,还含有
,还含有 、
、 、
、 等杂质],利用该矿物生产铁红(
等杂质],利用该矿物生产铁红( )和碱式碳酸镁的工艺流程如图:
)和碱式碳酸镁的工艺流程如图:
常温下部分难溶物的溶度积常数如表:
| 难溶物 |  |  |  |  |
溶度积常数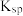 | 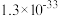 | 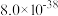 | 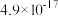 | 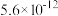 |
(1)为了加快“酸浸”的速率可采取的措施有
(2)“转化”过程中
 参与反应的离子方程式为
参与反应的离子方程式为(3)分离滤渣2时,溶液X通常选用
(4)“沉镁”过程中发生反应的离子方程式为
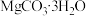 的产率会降低,原因是
的产率会降低,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】CoC2O4是制备金属钴的原料。利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如图:
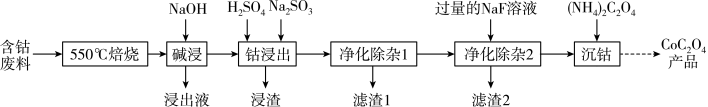
(1)“550℃煅烧”的目的是____ 。
(2)“浸出液”的主要成分是___ 。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为___ 。
(4)“净化除杂1”过程中,如何检验该杂质__ (用离子方程式表示),现象为__ :需在40~50℃加入H2O2溶液,其原因是__ ,目的是__ (用离子方程式表示);再升温至80~85℃,加入Na2CO3溶液,调pH至5,“滤渣I”的主要成分是__ 。
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l0-5 mol/L,则滤液中c(Mg2+)为___ mol/L。[已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10]

(1)“550℃煅烧”的目的是
(2)“浸出液”的主要成分是
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(4)“净化除杂1”过程中,如何检验该杂质
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l0-5 mol/L,则滤液中c(Mg2+)为
您最近一年使用:0次



