现有常温时pH=1的某强酸溶液10 mL,下列操作能使溶液pH变成2的是
| A.加水稀释成100 mL |
| B.加入10 mL水进行稀释 |
| C.加入10 mL 0.01 mol·L-1的NaOH溶液 |
| D.加入10 mL 0.01 mol·L-1的HCI溶液 |
14-15高二上·宁夏银川·期中 查看更多[9]
福建省龙岩市永定区城关中学2023-2024学年高二上学期期中考试化学试题作业(十七) 水溶液的酸碱性与pH贵州省铜仁市贵州铜仁伟才学校2021-2022学年高二上学期期中考试化学试题云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题天津市部分区2021-2022学年高二上学期期末(下学期期初)考试化学试题云南省红河县一中2020-2021学年高二下学期6月份考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第1节 水与水溶液2014-2015学年云南省蒙自市蒙自一中高二上学期期中化学试卷2014-2015学年宁夏回族自治区银川一中高二上学期期中化学试卷
更新时间:2016-12-09 07:02:38
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】常温下,向一定体积0.01mol/L的Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液和NaHSO4溶液体积之和,则Ba(OH)2溶液和NaHSO4溶液体积之比是
| A.1:1 - | B.1:2 | C.1:4 | D.1:9 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】25℃时,某溶液中由水电离出的c(OH-)为1×10-11mol·L-1,则该溶液的pH可能等于
| A.12 | B.8 | C.7 | D.3 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】表1是元素周期表的一部分:
 时,用浓度为
时,用浓度为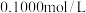 的NaOH溶液分别滴定
的NaOH溶液分别滴定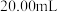 浓度均为
浓度均为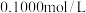 的两种酸HX、
的两种酸HX、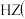 忽略体积变化
忽略体积变化 ,实验数据如表
,实验数据如表
下列判断正确的是
| 氧 | X |
| Y | Z |
 时,用浓度为
时,用浓度为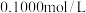 的NaOH溶液分别滴定
的NaOH溶液分别滴定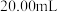 浓度均为
浓度均为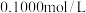 的两种酸HX、
的两种酸HX、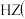 忽略体积变化
忽略体积变化 ,实验数据如表
,实验数据如表| 数据编号 | 滴入NaOH溶液的体积 | 溶液pH | |
| HX | HZ | ||
| ① | 0 | 3 | 1 |
| ② | 20.00 | a | 7 |
A.表格中 |
B.HX和HZ等体积混合后 |
| C.Y和Z两元素的简单氢化物受热分解,前者分解温度高 |
D.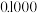  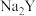 的水溶液中: 的水溶液中: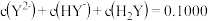  |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】常温常压时,下列叙述正确的是
A.pH相等的 、NaOH和 、NaOH和 三种溶液: 三种溶液: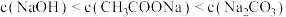 |
B.对于pH为2的盐酸: |
C. 固体在 固体在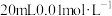 氨水中的 氨水中的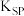 比在 比在 溶液中的 溶液中的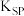 小 小 |
D. 的醋酸的 的醋酸的 , , 的醋酸的 的醋酸的 ,则 ,则 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐3】根据下列图示所得出的结论一定错误的是
A.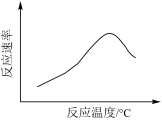 表示酶催化反应的反应速率随反应温度的变化 表示酶催化反应的反应速率随反应温度的变化 |
B.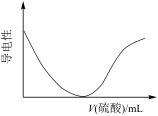 表示向Ba(OH)2溶液中滴加稀硫酸至过量的过程中溶液导电性的变化 表示向Ba(OH)2溶液中滴加稀硫酸至过量的过程中溶液导电性的变化 |
C.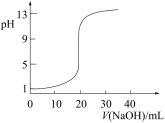 表示用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸的滴定曲线 表示用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸的滴定曲线 |
D.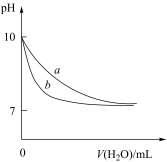 表示相同温度下,向等体积pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线 表示相同温度下,向等体积pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】将pH=12的NaOH与pH=10的NaOH溶液等体积混合后,溶液后c(H+)最接近于( )
| A.0.5(10-12+10-10)mol/L | B.0.5(10-4+10-2) mol/L |
| C.(10-12+10-10)mol/L | D.2×10-12mol/L |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】25 ℃将0.1 mol·L-1的HCl和0.06 mol·L-1 Ba(OH)2溶液以等体积混合后,该混合液的pH是
| A.1.7 | B.12.3 | C.12 | D.2 |
您最近半年使用:0次

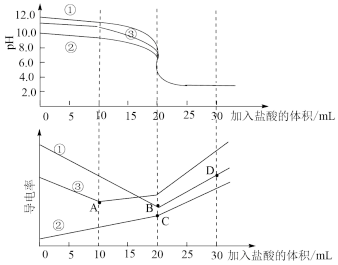
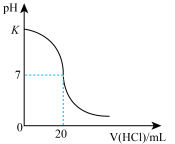
 约为
约为

 的标准盐酸滴定
的标准盐酸滴定 未知浓度的
未知浓度的 溶液,所得滴定曲线如图所示。图中K点代表的pH为
溶液,所得滴定曲线如图所示。图中K点代表的pH为