A、B、C是单质,其中A是金属,各种物质间的转化关系如图:
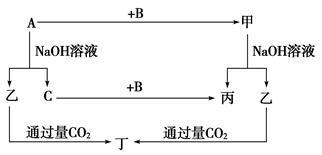
根据图示转化关系回答:
(1)写出下列物质的化学式。
A___________ ,B________ ,乙_________ ,丁______________ 。
(2)写出 ①A与NaOH溶液反应的化学方程式________________________ 。
②乙溶液中通入过量CO2反应的离子方程式_____________________ 。
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为________ ,有_______ mol电子发生转移。

根据图示转化关系回答:
(1)写出下列物质的化学式。
A
(2)写出 ①A与NaOH溶液反应的化学方程式
②乙溶液中通入过量CO2反应的离子方程式
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为
更新时间:2016/12/09 07:03:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
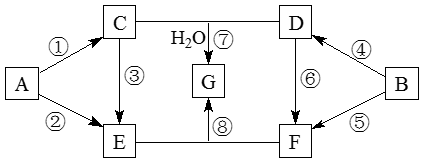
【推荐1】下图所涉及的物质均为中学化学中的常见物质,其中A、C、G是中学化学常见单质,其中A、C是金属,G是气体,B是常见液体,它们存在如下转化关系,反应中部分反应物及次要产物均已略去。
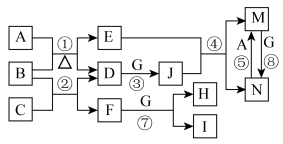
(1)①→⑦中属于氧化还原反应的有______ 个,④的离子方程式是___________________
(2)实验室中常用反应⑦处理多余G,理论上处理标准状况下6.72L气体G,至少需要5mol/LNaOH溶液体积________ ,实验室中制取G的离子方程式______________________
(3)向M的溶液中加过量的氨水,写出对应离子方程式_________________________ ,露置,产物的颜色迅速变化,对应化学方程式是______________________________________
(4)图中有信息能表明A、C的活动性不同,用文字说明_______________________

(1)①→⑦中属于氧化还原反应的有
(2)实验室中常用反应⑦处理多余G,理论上处理标准状况下6.72L气体G,至少需要5mol/LNaOH溶液体积
(3)向M的溶液中加过量的氨水,写出对应离子方程式
(4)图中有信息能表明A、C的活动性不同,用文字说明
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E 五种化合物,均含有某种常见元素,它们的转化关系如图所示,其中 A 为澄清溶液,C 为难溶的白色固体,E 则易溶于水,若取 A 溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃)。

请回答下列问题:
(1)写出化学式:A_____ ,B_____ ,C_____ ,D_____ ,E_____ 。
(2)写出下列反应的离子方程式: A→B:____ B→D:_____ C→E:_____

请回答下列问题:
(1)写出化学式:A
(2)写出下列反应的离子方程式: A→B:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】Ⅰ液氨和二硫化碳在一定条件下反应可以生成甲和乙两种盐。2.55g乙受热会完全分解生成等物质的量的气体丙和丁共2.24L(标准状况),丙能使紫色石蕊试液变蓝,另取少量FeCl3溶液,向其中滴加甲溶液,发现溶液变为红色。试推测回答:
(1)化合物甲的化学式为___________ ,化合物乙的电子式为___________ 。
(2)请写出乙与足量NaOH溶液共热的离子反应方程式___________ 。
(3)请写出液氨与二硫化碳在一定条件下反应的化学方程式___________ 。
Ⅱ焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中,受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
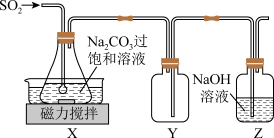
当溶液pH约为4时,停止反应。在20℃静置结晶,生成Na2S2O5的化学方程式为2NaHSO3=Na2S2O5+H2O
(1)温度为40℃时,SO2与Na2CO3过饱和溶液反应的离子方程___________ 。
(2)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是___________ 。
(1)化合物甲的化学式为
(2)请写出乙与足量NaOH溶液共热的离子反应方程式
(3)请写出液氨与二硫化碳在一定条件下反应的化学方程式
Ⅱ焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中,受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。

当溶液pH约为4时,停止反应。在20℃静置结晶,生成Na2S2O5的化学方程式为2NaHSO3=Na2S2O5+H2O
(1)温度为40℃时,SO2与Na2CO3过饱和溶液反应的离子方程
(2)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】铝镁合金已成为轮船制造、化工生产等行业的重要材料。某研究性学习小组的三位同学为测定某含镁3%~5%的铝镁合金(不含其他元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。
探究一
实验方案:铝镁合金 测定剩余固体质量。实验中发生反应的化学方程式是
测定剩余固体质量。实验中发生反应的化学方程式是__ 。
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入体积为V浓度为2.0mol•L-1的NaOH溶液中,充分反应。为保证合金充分反应,NaOH溶液的体积V≥__ 。
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将__ (填“偏大”或“偏小”)。
探究二
实验方案:铝镁合金 测定生成气体的体积(实验装置如图所示)。
测定生成气体的体积(实验装置如图所示)。

(1)某同学提出该实验装置不够完善,应在A、B之间添加一个除酸雾的装置。你的意见是__ (填“需要”或“不需要”)。
(2)为使测定结果尽可能精确,实验中应注意的问题有(写出两点):
①__ ,
②___ 。
探究三
实验方案:称量xg铝镁合金粉末,放入装有足量氧气的容器中使其充分灼烧。
(1)欲计算镁的质量分数,该实验中还需测定的数据是__ 。
(2)若用空气代替O2进行实验,对测定结果是否有影响?__ (填“是”或“否”)。
探究一
实验方案:铝镁合金
 测定剩余固体质量。实验中发生反应的化学方程式是
测定剩余固体质量。实验中发生反应的化学方程式是实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入体积为V浓度为2.0mol•L-1的NaOH溶液中,充分反应。为保证合金充分反应,NaOH溶液的体积V≥
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
探究二
实验方案:铝镁合金
 测定生成气体的体积(实验装置如图所示)。
测定生成气体的体积(实验装置如图所示)。
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个除酸雾的装置。你的意见是
(2)为使测定结果尽可能精确,实验中应注意的问题有(写出两点):
①
②
探究三
实验方案:称量xg铝镁合金粉末,放入装有足量氧气的容器中使其充分灼烧。
(1)欲计算镁的质量分数,该实验中还需测定的数据是
(2)若用空气代替O2进行实验,对测定结果是否有影响?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】向一个铝制易拉罐中充满CO2,然后往罐中注入足量的NaOH溶液,立即用胶布严封罐口,不多会儿听到罐内“咔、咔”作响,发现易拉罐变瘪,再过一会儿易拉罐又鼓起来。
(1)易拉罐变瘪的原因_______ 。反应的离子方程式_______ 。
(2)易拉罐又鼓起来的原因_______ 。反应的离子方程式_______ 。
(1)易拉罐变瘪的原因
(2)易拉罐又鼓起来的原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于18。其中只有C、D为金属元素;A和C的最外层均只有1个电子;B和E的最外层电子数相同,且B的L层电子数是K层电子数的3倍;D常用作易拉罐外壳。完成下列问题:
(1)写出相应元素的元素符号:B___________ ,E___________ 。
(2)A的一种核素中质子数为质量数的 ,则以
,则以 X的形式表示该核素为
X的形式表示该核素为___________ 。
(3)E元素的最高化合价为___________ 。
(4)A2B和C2B2反应的化学方程式___________ 。
(5)D与氢氧化钠溶液反应的化学方程式___________ 。
(1)写出相应元素的元素符号:B
(2)A的一种核素中质子数为质量数的
 ,则以
,则以 X的形式表示该核素为
X的形式表示该核素为(3)E元素的最高化合价为
(4)A2B和C2B2反应的化学方程式
(5)D与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表中的一部分,列出10种元素在元素周期表中的位置。用化学符号回答下列各问题
(1)10种元素中,化学性质最不活泼的是_______ 。
(2)①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是_______ 。
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是_______ 。
(4)元素⑦的氢化物的化学式为_______ ;若该氢化物和元素⑧的单质反应,则化学方程式为_______ 。
(5)①和⑨的最高价氧化物对应水化物的化学式为_______ 和_______ 。①和⑨两元素形成化合物的化学式为_______ ;该化合物的溶液与元素⑧的单质反应的化学方程式为_______ 。
(6)①和⑤最高价氧化物对应水化物相互反应的化学方程式为_______ ;离子方程式为_______ 。
| 主族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是
(4)元素⑦的氢化物的化学式为
(5)①和⑨的最高价氧化物对应水化物的化学式为
(6)①和⑤最高价氧化物对应水化物相互反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】图为元素周期表的一部分,请参照①~⑧在表中的位置,回答下列问题:___________ 。
(2)①~⑧中,化学性质最稳定的是___________ (填元素符号),非金属性最强的是___________ (填元素符号),最高价氧化物对应水化物酸性最强的是___________ (填化学式)。
(3)①~⑦中,原子半径最大的是___________ (填元素符号)。
(4)元素③的非金属性比⑥___________ (填“强”或“弱”),请从原子结构的角度解释:___________ ,列举一个化学事实加以说明___________ 。
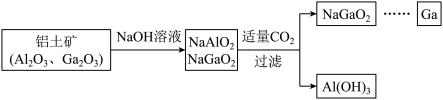
(5)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。
工业制备镓的流程如下图所示:___________ 。酸性:Al(OH)3___________ Ga(OH)3(填“>”或“<”),冶炼金属镓的方法是___________ (填序号)。
A.热还原法 B.热分解法 C.电解法

(2)①~⑧中,化学性质最稳定的是
(3)①~⑦中,原子半径最大的是
(4)元素③的非金属性比⑥
(5)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。
工业制备镓的流程如下图所示:
A.热还原法 B.热分解法 C.电解法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A~G七种物质的转化关系如图所示(部分反应物、产物和反应条件未标出)。其中,A、B为中学化学常见的金属单质,C是淡黄色固体,D既能与强酸溶液反应,又能与强碱溶液反应,F溶液中加入AgNO3溶液产生不溶于稀硝酸的白色沉淀,E和G焰色反应均呈黄色。①、④、⑤均为燃烧反应。
请回答下列问题:
(1)F的化学式___________ ,G的化学式___________ 。
(2)反应①的化学方程式是__________ 。
(3)写出下列反应的离子方程式:
③__________________ ,⑥_______________ 。
(4)将E的溶液逐滴加入到F的溶液中至过量,其现象是____________ ,_____________ 。

请回答下列问题:
(1)F的化学式
(2)反应①的化学方程式是
(3)写出下列反应的离子方程式:
③
(4)将E的溶液逐滴加入到F的溶液中至过量,其现象是
您最近一年使用:0次



