有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。
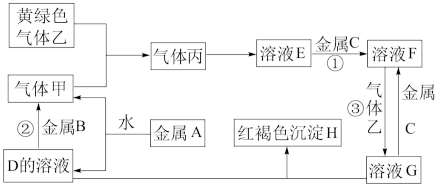
(1)写出下列物质的化学式:F中的溶质_______ ;丙_______ 。
(2)反应③的离子方程式_______
(3)H受热分解后的固体产物与金属B高温下的化学方程式:_______
(4)A与水反应的离子方程式_______

(1)写出下列物质的化学式:F中的溶质
(2)反应③的离子方程式
(3)H受热分解后的固体产物与金属B高温下的化学方程式:
(4)A与水反应的离子方程式
更新时间:2016/12/09 07:37:25
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下气态化合物,C为常温下液态化合物,图中有部分生成物未标出。请填写以下空白:
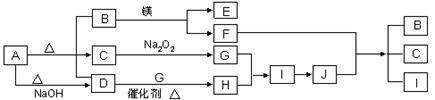
(1)写出下列反应的化学方程式:
D+G→ H__________________________________________________ ,
F+J → B + C + I________________________________________________ 。
(2)写出A+NaOH→D的离子方程式__________________________________ 。
(3)J的浓溶液久置后显黄色,其原因用化学方程式表示为_________________________ 。

(1)写出下列反应的化学方程式:
D+G→ H
F+J → B + C + I
(2)写出A+NaOH→D的离子方程式
(3)J的浓溶液久置后显黄色,其原因用化学方程式表示为
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如图所示(部分产物已略去):
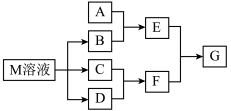
(1)写出用惰性电极电解M溶液的离子方程式 ____________ 。
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是__________________ 。
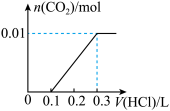
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如下图所示,“则A与B溶液”反应后溶液中的溶质为__________ (填化学式 )。
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所能观察到的实验现象是____________________ 。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚后溶液显紫色,则由A转化成E的离子方程式是_______________ ;
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,请写出足量E与D反应的化学方程式___________________ 。

(1)写出用惰性电极电解M溶液的
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如下图所示,“则A与B溶液”反应后溶液中的溶质为

(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所能观察到的实验现象是
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚后溶液显紫色,则由A转化成E的离子方程式是
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,请写出足量E与D反应的化学方程式
您最近半年使用:0次
【推荐3】某研究小组为探究不溶性固体X的组成和性质,进行了如下实验。已知X是一种仅含有四种元素的具有固定成的盐类物质,H由碘元素和另外一种元素组成,图中所有气体体积均在标准状况下测定。
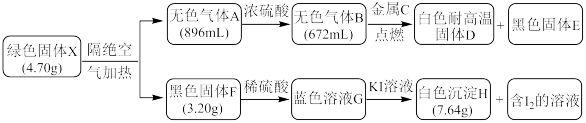
请回答下列问题:
(1)写出X的化学式__________ ;
(2)写出C的原子结构示意图___________ ;组成E元素的某种核素常用于考古断代,该原子核内中子数为8,写出该校素的原子符号___________ 。
(3)C在装有B的集气瓶中燃烧,其实验现象为___________ ;并写出相应的化学方程式___________ 。
(4)已知H能与含NaClO的碱性溶液反应生成NaIO3和蓝色絮状沉淀,试写出该反应的离子方程式____________________________ 。

请回答下列问题:
(1)写出X的化学式
(2)写出C的原子结构示意图
(3)C在装有B的集气瓶中燃烧,其实验现象为
(4)已知H能与含NaClO的碱性溶液反应生成NaIO3和蓝色絮状沉淀,试写出该反应的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间的转化关系如图所示。(图中有些反应的产物和反应条件没有标出)
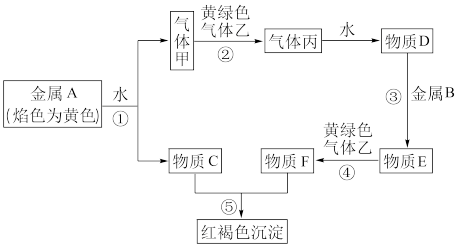
请回答下列问题:
(1)A的化学式为___________ ,丙的化学式为___________ 。
(2)写出下列反应的离子方程式:
①___________ ;
④___________ ;
⑤___________ 。
(3)写出C溶液与Al反应的离子方程式:___________ 。

请回答下列问题:
(1)A的化学式为
(2)写出下列反应的离子方程式:
①
④
⑤
(3)写出C溶液与Al反应的离子方程式:
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
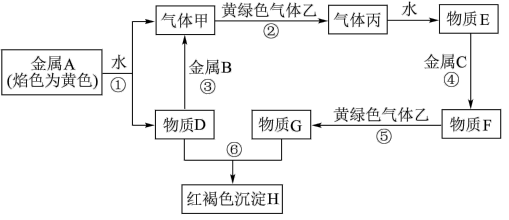
请根据以上信息回答下列问题:
(1)写出下列物质的化学式: C_______________ 、F_____________ 。
(2)写出下列反应化学方程式或离子方程式:
反应①的化学方程式_______________________________________________ 。
反应③的离子方程式_______________________________________________ 。
反应⑤的离子方程式_______________________________________________ 。
(3)通常用___________ 溶液检验物质G中阳离子,其原理是__________________ 。(用离子方程式表示)

请根据以上信息回答下列问题:
(1)写出下列物质的化学式: C
(2)写出下列反应化学方程式或离子方程式:
反应①的化学方程式
反应③的离子方程式
反应⑤的离子方程式
(3)通常用
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】金属钠与水的反应是中学化学中的一个重要反应。高一化学教材中该实验曾出现过几种不同的演示方法。分别如下图中(A)(B)(C)所示:
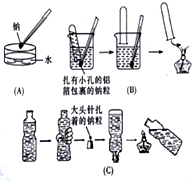
(1)现按图(A)所示的方法,在室温时,向盛有饱和Na2CO3溶液(滴有几滴酚酞)的烧杯中,加入一小块金属钠。
①下列现象描述正确的是_______ (填字母代号)。
A.钠浮在液面上,并四处游动,最后消失 B.反应过程中钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色 D.恢复到室温时,烧杯底部有固体物质析出
②请补充并完成该实验从试剂瓶中取出钠到向烧杯中投入钠的有关操作:
用镊子从试剂瓶中取出一小块钠→_______________ →用镊子夹取切好的金属钠投入到盛有饱和Na2CO3溶液的烧杯中。
(2)按图(C)所示的方法进行该实验,若500mL的矿泉水瓶开始时装有477.6mL水,要使倒置的矿泉水瓶正好恢复原状,假设矿泉水瓶内外均为标准状况,则大头针上扎着的钠粒质量为_______ g。
(3)1998年全国高考试题中的实验题就是根据图(B)的原理设计的。题目及部分答案如下:
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:中学化学实验常用仪器、800毫升烧杯、100毫升量筒、短颈玻璃漏斗、 长颈漏斗、玻璃棒、铜网、铝锌合金样品、 浓盐酸(密度1.19克/毫升)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100毫升)
Ⅰ.补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在800毫升烧杯底部,把短颈漏斗倒扣在样品上面。……
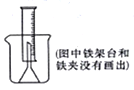
Ⅰ.②往烧杯中注入水,直至水面没过漏斗颈。[评分标准,凡加水改为加酸者,不论其他后续步骤是否正确,本小题一律0分]
③在100毫升量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中。烧杯中水面到杯口至少保留约100毫升空间。
④将“仅器A”插入烧杯并接近烧杯底部,通过它慢慢加入浓盐酸,至有气体产生。
回答下列问题:
a.为什么在“②往烧杯中注入水,直至水面没过调斗颈”这一步中改加水为加酸会
b.“仪器A”可以是________________________ 。
c.合金样品用铜网包裹的目的是____________________________________ 。

(1)现按图(A)所示的方法,在室温时,向盛有饱和Na2CO3溶液(滴有几滴酚酞)的烧杯中,加入一小块金属钠。
①下列现象描述正确的是
A.钠浮在液面上,并四处游动,最后消失 B.反应过程中钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色 D.恢复到室温时,烧杯底部有固体物质析出
②请补充并完成该实验从试剂瓶中取出钠到向烧杯中投入钠的有关操作:
用镊子从试剂瓶中取出一小块钠→
(2)按图(C)所示的方法进行该实验,若500mL的矿泉水瓶开始时装有477.6mL水,要使倒置的矿泉水瓶正好恢复原状,假设矿泉水瓶内外均为标准状况,则大头针上扎着的钠粒质量为
(3)1998年全国高考试题中的实验题就是根据图(B)的原理设计的。题目及部分答案如下:
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:中学化学实验常用仪器、800毫升烧杯、100毫升量筒、短颈玻璃漏斗、 长颈漏斗、玻璃棒、铜网、铝锌合金样品、 浓盐酸(密度1.19克/毫升)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100毫升)
Ⅰ.补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在800毫升烧杯底部,把短颈漏斗倒扣在样品上面。……

Ⅰ.②往烧杯中注入水,直至水面没过漏斗颈。[评分标准,凡加水改为加酸者,不论其他后续步骤是否正确,本小题一律0分]
③在100毫升量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中。烧杯中水面到杯口至少保留约100毫升空间。
④将“仅器A”插入烧杯并接近烧杯底部,通过它慢慢加入浓盐酸,至有气体产生。
回答下列问题:
a.为什么在“②往烧杯中注入水,直至水面没过调斗颈”这一步中改加水为加酸会
b.“仪器A”可以是
c.合金样品用铜网包裹的目的是
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E是中学常见的几种化合物,相关物质间的关系如下图所示:

已知:X、Y是生活中常见的金属单质,A、B都是氧化物且A是红棕色粉末。
回答下列问题:
(1)单质X与A反应的化学方程式是________________________________ ;
(2)若试剂1和试剂2均是强电解质。
①若试剂1和试剂2的酸碱性相同,则C溶液显__________ (填“酸性”、“碱性”或“中性”);
②若试剂1和试剂2的酸碱性不同,试剂1和B的离子方程式是_________________ 。
(3)若试剂2是稀硝酸。
①Y单质与稀硝酸反应生成E时,Y单质必须过量,写出该反应的离子方程式___________ 。如果稀硝酸过量,可以选择试剂_____________ 进行验证。
②D的阳离子能够与强碱、氯气反应,生成一种高效的净水剂YO42-,写出有关反应的离子方程式_________________ 。

已知:X、Y是生活中常见的金属单质,A、B都是氧化物且A是红棕色粉末。
回答下列问题:
(1)单质X与A反应的化学方程式是
(2)若试剂1和试剂2均是强电解质。
①若试剂1和试剂2的酸碱性相同,则C溶液显
②若试剂1和试剂2的酸碱性不同,试剂1和B的离子方程式是
(3)若试剂2是稀硝酸。
①Y单质与稀硝酸反应生成E时,Y单质必须过量,写出该反应的离子方程式
②D的阳离子能够与强碱、氯气反应,生成一种高效的净水剂YO42-,写出有关反应的离子方程式
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】我国古代许多著作在化学学科知识上都体现出了一定水平的认识。其中《管子•地数》中有记载:“上有丹沙者,下有黄金;上有慈石者,下有铜金。”
Ⅰ.“丹沙者丹砂也”,丹砂是古代炼丹的重要原料,也是实验室处理水银洒落后的产物。你认为丹砂主要成分是_____ ;(填化学式)“慈石者磁石也”,请写出磁石溶于盐酸的离子方程式:_____ ;
Ⅱ.“铜金者,斑岩铜矿也。”
安徽宣城茶亭铜金矿床是长江中下游成矿带中新发现的一个大型斑岩型矿床。斑岩铜矿中Cu主要以铜﹣铁硫化物(主要为CuFeS2)的形式存在。以黄铜矿(主要成分为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4•7H2O)。其主要流程如图:
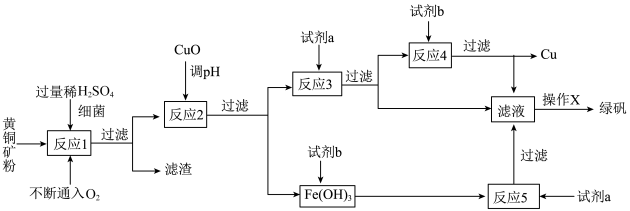
已知:①“反应1”:4CuFeS2 +2H2SO4 +17O2 ═4CuSO4 +2Fe2(SO4)3 +2H2O
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表:
(1)“反应1”中,每生成1 mol CuSO4转移电子数为_____ NA;
(2)“试剂a”是_____ ,“试剂b”是_____ ;
(3)“反应2”中加CuO调pH为3.7~4.7的目的是_____ ;
(4)“操作X”应为_____ 、_____ 、过滤、洗涤;请简述上述“操作X”中如何对所得 FeSO4•7H2O晶体进行洗涤_____ ;
(5)简述如何判断“反应5”已进行完全:_____ 。
Ⅰ.“丹沙者丹砂也”,丹砂是古代炼丹的重要原料,也是实验室处理水银洒落后的产物。你认为丹砂主要成分是
Ⅱ.“铜金者,斑岩铜矿也。”
安徽宣城茶亭铜金矿床是长江中下游成矿带中新发现的一个大型斑岩型矿床。斑岩铜矿中Cu主要以铜﹣铁硫化物(主要为CuFeS2)的形式存在。以黄铜矿(主要成分为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4•7H2O)。其主要流程如图:

已知:①“反应1”:4CuFeS2 +2H2SO4 +17O2 ═4CuSO4 +2Fe2(SO4)3 +2H2O
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表:
沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 4.7 | 2.7 | 7.6 |
完全沉淀pH | 6.7 | 3.7 | 9.6 |
(2)“试剂a”是
(3)“反应2”中加CuO调pH为3.7~4.7的目的是
(4)“操作X”应为
(5)简述如何判断“反应5”已进行完全:
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种多功能水处理剂。K2FeO4具有强氧化性,在碱性溶液中较稳定。实验室中常用KClO在强碱性介质中与Fe(NO3)3反应制备K2FeO4(夹持装置略去)。回答下列问题:

(1)装置A中盛放浓HCl的仪器名称为_____ ,装置D中饱和食盐水的作用是____ 。
(2)选择上述装置制备K2FeO4,按气流从左到右的方向,装置的连接顺序为____ 。(用字母表示)
(3)装置B中生成K2FeO4的离子方程式为____ 。
(4)根据K2FeO4理论合成产率与合成条件相应曲面投影图(如下图,虚线上的数据表示K2FeO4的理论合成产率),制备K2FeO4最佳条件是:温度___ (填序号,下同),反应时间_____ 。

a 0.0~5.0℃ b 5.0~10℃
c 50~60min d 60~70min
(5)高铁酸钾既能杀菌消毒又能絮凝净水,其处理水的原理为_____ 、____ 。
(6)为测定产品的纯度,现取产品10.0g,加入足量稀硫酸(FeO + H+→O2↑+Fe3++H2O),收集到0.672L气体(标准状况下)。则产品中高铁酸钾的质量分数为
+ H+→O2↑+Fe3++H2O),收集到0.672L气体(标准状况下)。则产品中高铁酸钾的质量分数为_____ 。

(1)装置A中盛放浓HCl的仪器名称为
(2)选择上述装置制备K2FeO4,按气流从左到右的方向,装置的连接顺序为
(3)装置B中生成K2FeO4的离子方程式为
(4)根据K2FeO4理论合成产率与合成条件相应曲面投影图(如下图,虚线上的数据表示K2FeO4的理论合成产率),制备K2FeO4最佳条件是:温度

a 0.0~5.0℃ b 5.0~10℃
c 50~60min d 60~70min
(5)高铁酸钾既能杀菌消毒又能絮凝净水,其处理水的原理为
(6)为测定产品的纯度,现取产品10.0g,加入足量稀硫酸(FeO
 + H+→O2↑+Fe3++H2O),收集到0.672L气体(标准状况下)。则产品中高铁酸钾的质量分数为
+ H+→O2↑+Fe3++H2O),收集到0.672L气体(标准状况下)。则产品中高铁酸钾的质量分数为
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】有关物质的转化关系如下图所示(部分物质和条件已略去)。A、C、E、G是中学化学中的常见单质,A为黑色粉末,G为黄绿色气体,E在G 中燃烧时发出苍白色火焰,F的焰色反应显黄色,B是常见的无色液体,K为红褐色沉淀。
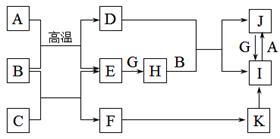
请回答下列问题:
(1)G的化学式为______________ ,F的化学式为______________ 。
(2)D、B、H混和生成J和I的离子方程式:___________________ 。
(3)常温下G与F的溶液反应的离子方程式:___________________
(4)J转变为I的化学方程式:_______________________

请回答下列问题:
(1)G的化学式为
(2)D、B、H混和生成J和I的离子方程式:
(3)常温下G与F的溶液反应的离子方程式:
(4)J转变为I的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍;F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为_________________ ,反应④的化学方程式为________________________ 。
(2)若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是_____________________________________________ 。
(3)若A、D、F都是由短周期非金属元素形成的单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为__________________________________ 。

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍;F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为
(2)若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是
(3)若A、D、F都是由短周期非金属元素形成的单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为液体,C为气体。D、E、F、G、H、X均为化合物,其中X是一种无氧强酸、E为黑色固体,H在常温下为液体。它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去)。
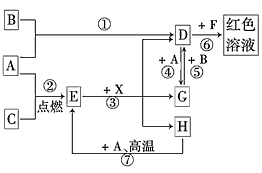
(1)写出化学式:A_________ 、D_________ 、E__________ 、X__________ 。
(2)在反应①~⑦中,不属于氧化还原反应的是________ (填编号)。
(3)反应⑥的离子方程式为_________________________ ;
(4)反应⑦的化学方程式为____________________ ;该反应中每消耗0.3 mol的A,可转移电子________ mol。
(5)分别写出D的溶液与小苏打溶液、D的溶液中通入少量SO2反应的离子方程式___________________ 。

(1)写出化学式:A
(2)在反应①~⑦中,不属于氧化还原反应的是
(3)反应⑥的离子方程式为
(4)反应⑦的化学方程式为
(5)分别写出D的溶液与小苏打溶液、D的溶液中通入少量SO2反应的离子方程式
您最近半年使用:0次



