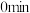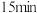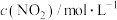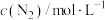Ⅰ.对于4FeS2+11O2═2Fe2O3+8SO2,试回答有关的问题:
(1)常选用哪些物质浓度的变化来表示该反应的速率____________ ;
(2)为了提高生成SO2的速率,可以采取的措施是______________ ;
A.增加FeS2的量 B.增大O2的浓度 C.升高温度 D.减小压强
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0﹣3分钟各物质的量的变化情况如图所示(A,B,C均为气体)

(3)该反应的化学方程式为_________________ ;
(4)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______________
A.气体总质量保持不变
B.A、B、C的浓度都相等
C.A、B、C的浓度不再发生变化
D.A、B、C的分子数之比为2:1:2
E.正反应和逆反应都已停止
F.容器内气体密度不再发生变化.
(1)常选用哪些物质浓度的变化来表示该反应的速率
(2)为了提高生成SO2的速率,可以采取的措施是
A.增加FeS2的量 B.增大O2的浓度 C.升高温度 D.减小压强
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0﹣3分钟各物质的量的变化情况如图所示(A,B,C均为气体)

(3)该反应的化学方程式为
(4)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是
A.气体总质量保持不变
B.A、B、C的浓度都相等
C.A、B、C的浓度不再发生变化
D.A、B、C的分子数之比为2:1:2
E.正反应和逆反应都已停止
F.容器内气体密度不再发生变化.
更新时间:2016-12-09 07:58:44
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.由图中数据分析:

(1)该反应的化学方程式为__________________ .
(2)反应开始至2min,用X表示的平均反应速率为______ mol·L-1·min-1;
平衡时,Y的转化率为__________ ,
平衡时,Z的浓度为_____________ mol·L-1。
(3)下列叙述能说明上述反应达到平衡状态的是_________ (填选项、多选)
E.混合气体的总物质的量不随时间的变化而变化.

(1)该反应的化学方程式为
(2)反应开始至2min,用X表示的平均反应速率为
平衡时,Y的转化率为
平衡时,Z的浓度为
(3)下列叙述能说明上述反应达到平衡状态的是
| A.X、Y、Z的物质的量之比为3:1:2 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗3mol X,同时生成2mol Z |
| D.混合气体的总质量不随时间的变化而变化 |
E.混合气体的总物质的量不随时间的变化而变化.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在有氧条件下,新型催化剂 能催化
能催化 与
与 反应生成
反应生成 ,该反应的方程式为
,该反应的方程式为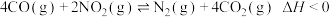
(1)现向某密闭容器中充入等物质的量浓度的 和
和 气体,维持恒温恒容,在倠化剂作用下发生反应。相关数据如下:
气体,维持恒温恒容,在倠化剂作用下发生反应。相关数据如下:
在0~ 内,以
内,以 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为______ ,在 时,
时, 的转化率为
的转化率为______ 。此温度下,该反应的化学平衡常数
______ (保留两位有效数字)。
(2)该反应的正、逆反应的平衡常数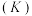 与温度
与温度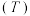 的关系如图所示,其中表示正反应的平衡常数
的关系如图所示,其中表示正反应的平衡常数 的是
的是______ (选“A”或“B”),原因是______ 。

 能催化
能催化 与
与 反应生成
反应生成 ,该反应的方程式为
,该反应的方程式为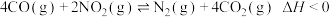
(1)现向某密闭容器中充入等物质的量浓度的
 和
和 气体,维持恒温恒容,在倠化剂作用下发生反应。相关数据如下:
气体,维持恒温恒容,在倠化剂作用下发生反应。相关数据如下:
|
|
|
|
| |
| 2.0 | 1.7 | 0.56 | 1.5 | 1.5 |
| 0 | 0.15 | 0.22 | 0.25 | 0.25 |
 内,以
内,以 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为 时,
时, 的转化率为
的转化率为
(2)该反应的正、逆反应的平衡常数
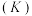 与温度
与温度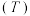 的关系如图所示,其中表示正反应的平衡常数
的关系如图所示,其中表示正反应的平衡常数 的是
的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】25 ℃时,在2 L的恒容密闭容器中,气态A、B、C的物质的量n(mol)随时间t的变化如图所示。

(1)该反应的化学方程式____________________________________________________ 。
(2)在________________ min时反应刚好达到平衡。
(3)在0~3minA物质的平均速率为_____________________ ,此时A物质的转化率为______ ,3min末时A物质的浓度为_____________ 。
(4)5~7 min内B的平均速率___________ 1~3min内B的平均速率(填大于、小于、等于)。
(5)下列措施可加快该反应速率的是__________ 。
A.扩大容器体积 B.使用恰当的催化剂 C.提高反应的温度 D.液化并转移出C物质

(1)该反应的化学方程式
(2)在
(3)在0~3minA物质的平均速率为
(4)5~7 min内B的平均速率
(5)下列措施可加快该反应速率的是
A.扩大容器体积 B.使用恰当的催化剂 C.提高反应的温度 D.液化并转移出C物质
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g) N2O4(g),如图所示。
N2O4(g),如图所示。

(1)曲线__ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)在0到1min中内用X表示该反应的速率是__ ,该反应达限度时,Y的转化率是__ 。
(3)下列能说明该反应已达到化学平衡状态的是__ 。(填标号)。
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.容器内分子总数不再发生变化
D.容器内N2O4与NO2物质的量相同
E.消耗nmolN2O4的同时生成2nmolNO2
 N2O4(g),如图所示。
N2O4(g),如图所示。
(1)曲线
(2)在0到1min中内用X表示该反应的速率是
(3)下列能说明该反应已达到化学平衡状态的是
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.容器内分子总数不再发生变化
D.容器内N2O4与NO2物质的量相同
E.消耗nmolN2O4的同时生成2nmolNO2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氢能是一种非常清洁的能源,氨分解制备氢气是一种技术先进和经济可行的工艺。恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应 ,测得不同起始浓度和催化剂表面积下
,测得不同起始浓度和催化剂表面积下 的浓度随时间的变化如下表所示:
的浓度随时间的变化如下表所示:
回答下列问题:
(1)已知 、
、 、
、 的键能分别为436kJ/mol、946kJ/mol、391kJ/mol。则
的键能分别为436kJ/mol、946kJ/mol、391kJ/mol。则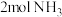 完全分解吸收的能量为
完全分解吸收的能量为___________ kJ。
(2)实验①中20~40min,
___________ 
(3)实验③达到平衡后, 的体积分数约为
的体积分数约为___________ (保留三位有效数字)。
(4)下列能说明该反应达到平衡状态的是___________ (填序号)
a.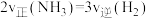 b.
b. 保持不变 c.
保持不变 c. 保持不变 d.容器内混合气体密度保持不变 e.容器内混合气体平均相对分子质量保持不变
保持不变 d.容器内混合气体密度保持不变 e.容器内混合气体平均相对分子质量保持不变
(5)关于上述实验,下列说法正确的是___________ (填序号)
a.实验②,60min时处于平衡状态b.相同条件下,增加氨气的浓度,反应速率增大
c.相同条件下,增加催化剂的表面积,反应速率增大
 ,测得不同起始浓度和催化剂表面积下
,测得不同起始浓度和催化剂表面积下 的浓度随时间的变化如下表所示:
的浓度随时间的变化如下表所示:| 编号 | 时间min 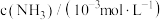 表面积/  | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 2a | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
(1)已知
 、
、 、
、 的键能分别为436kJ/mol、946kJ/mol、391kJ/mol。则
的键能分别为436kJ/mol、946kJ/mol、391kJ/mol。则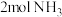 完全分解吸收的能量为
完全分解吸收的能量为(2)实验①中20~40min,


(3)实验③达到平衡后,
 的体积分数约为
的体积分数约为(4)下列能说明该反应达到平衡状态的是
a.
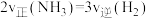 b.
b. 保持不变 c.
保持不变 c. 保持不变 d.容器内混合气体密度保持不变 e.容器内混合气体平均相对分子质量保持不变
保持不变 d.容器内混合气体密度保持不变 e.容器内混合气体平均相对分子质量保持不变(5)关于上述实验,下列说法正确的是
a.实验②,60min时处于平衡状态b.相同条件下,增加氨气的浓度,反应速率增大
c.相同条件下,增加催化剂的表面积,反应速率增大
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式___ 。该反应需要在加压下进行,原因是___ 。
(2)298K时,将20mL3xmol·L-1Na3AsO3、20mL3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq) AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是__ (填标号)。
a.溶液的pH不再变化
b.v(I-)=2v(AsO33-)
c.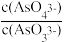 不再变化
不再变化
d.c(I-)=ymol·L-1
②tm时,v正__ v逆(填“大于”“小于”或“等于”)。
③tm时v逆___ tn时v逆(填“大于”“小于”或“等于”),理由是___ 。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___ 。
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
(2)298K时,将20mL3xmol·L-1Na3AsO3、20mL3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq)
 AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化
b.v(I-)=2v(AsO33-)
c.
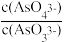 不再变化
不再变化d.c(I-)=ymol·L-1
②tm时,v正
③tm时v逆
④若平衡时溶液的pH=14,则该反应的平衡常数K为
您最近一年使用:0次