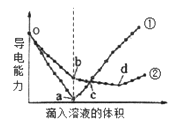
下列化学反应先后顺序判断正确的是( )
| A.含有等物质的量的H+、Al3+的溶液中,逐滴加入NaOH溶液:H+、Al3+、Al(OH)3 |
| B.含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气: I-、Br-、Fe2+ |
| C.含有等物质的量的NaCl、Na2S的溶液中加入AgNO3溶液:NaCl、Na2S |
| D.含有等物质的量的Fe3+、Cu2+的溶液中加入铁粉:Cu2+、Fe3+ |
14-15高三下·湖北·阶段练习 查看更多[6]
(已下线)专题34 分类例析元素化合物综合应用试题中存在的陷阱-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)专题04 离子反应(缺项配平、离子检验、离子推断、共存)-2021年高考化学必做热点专题(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(押题专练)(已下线)二轮复习 专题3 氧化还原反应 押题专练2016届河南省三门峡市陕州中学高三上学期第二次精英对抗赛化学试卷2015届湖北省七市(州)教科研协作体4月高三联合考试理综化学试卷
更新时间:2016-12-09 08:00:18
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某固体可能含有Ba2+、NH4+、Cu2+、Na+、Cl-、CO32-、SO42- 中的几种离子,取等质量的两份该固体,进行如下实验:
(1)一份固体溶于水得到无色透明溶液,加入足量的BaCl2溶液,得到沉淀6.63 g,在沉淀中加入过量的稀盐酸,仍有4.66 g沉淀;
(2)另一份固体与过量的NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672 L(标准状况)。
下列说法正确的是
(1)一份固体溶于水得到无色透明溶液,加入足量的BaCl2溶液,得到沉淀6.63 g,在沉淀中加入过量的稀盐酸,仍有4.66 g沉淀;
(2)另一份固体与过量的NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672 L(标准状况)。
下列说法正确的是
| A.该固体中只含有NH4+、Cl-、CO32-、SO42- |
| B.该固体中一定没有Cu2+、Na+、Ba2+、Cl- |
| C.该固体中一定含有NH4+、Na+、CO32- 、SO42- |
| D.根据以上实验,无法确定该固体中含有Na+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将KCl和CrCl3两种固体混合物共熔,得化合物X。X由K、Cr、Cl三种元素组成。将1.892gX中的Cr全部氧化成Cr2O72-,Cr2O72-可从过量的KI溶液中氧化出2.667g碘单质(Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O)。向溶有1.892gX的溶液中加入过量的AgNO3溶液,可得4.52gAgCl沉淀。则表示X的化学式为
| A.K3Cr2Cl9 | B.K3Cr2Cl5 | C.K3Cr2Cl7 | D.K2CrCl4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-。其中Cl-、Br- 、I-的个数比为2 :3 :4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3 :1,则通入氯气的物质的量与溶液中剩余的Fe2+物质的量之比为
| A.9 :1 | B.6 :2 | C.7 :3 | D.7 :4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】含等物质的量浓度的Na2S和NaBr的溶液中缓慢通入氯气,下列离子方程式不符合实际情况的是
| A.S2-+Cl2═S↓+2Cl- | B.S2-+2Br-+2Cl2═S↓+Br2+4Cl- |
| C.2S2-+2Br-+3Cl2═2S↓+Br2+6Cl- | D.3S2-+2Br-+4Cl2═3S↓+Br2+8Cl- |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将一块用砂纸打磨过的铝条放入试管,再加入98%浓硫酸3mL,铝条表面无明显现象 | 铝与浓硫酸常温下不反应 |
| B | 向试管中加入3mL稀KMnO4酸性溶液,再通入SO2气体,紫红色褪去 | SO2具有漂白性 |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
| D | 将溶液X与稀盐酸反应产生的气体通入品红溶液中,品红溶液褪色 | 溶液X中一定含有SO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】某小组同学探究铁离子与硫离子的反应,实验操作及现象如表:下列有关说法错误的( )
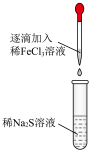 | 滴入FeCl3溶液立刻有黑色沉淀生成继续滴入FeC13溶液,黑色沉淀增多后又逐渐转化为黄色沉淀 |
 | 滴入Na2S溶液立刻生成黑色沉淀,沉淀下沉逐渐转化为黄色。继续滴入Na2S溶液,最后出现黑色的沉淀 |
| A.两次实验中,开始产生的黑色沉淀都为Fe2S3 |
| B.两次实验中,产生的黄色沉淀是因为发生了反应Fe2S3+4FeCl3═6FeCl2+3S |
| C.向稀FeCl3溶液中逐滴加入稀Na2S溶液至过量最后生成的黑色沉淀为FeS |
| D.在Na2S溶液过量的情况下,黑色沉淀中存在较多的Fe(OH)3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列反应的离子方程式正确的是
| A.等物质的量的 MgCl2、Ba(OH)2和 HCl 溶液浪合:Mg2++2OH- = Mg(OH)2↓ |
| B.向NaHSO4溶液中滴加Ba(OH)2溶液至不再产生沉淀: Ba2+ +OH-+H++SO42- = BaSO4↓+ H2O |
| C.向 Fe(NO3)3溶液中加入过量的HI 溶液:2NO3-+8H++6I- = 3I2+ 2NO↑+ 4H2O |
| D.(NH4)2Fe(SO4)2溶液与过量的 NaOH 溶液反应制 Fe(OH)2:Fe:2++2OH- = Fe(OH)2↓ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,用0.100mol/L 的AgNO3溶液滴定50.0mL,0.0500mol/L KCl溶液,以K2CrO4为指示剂,测得溶液中pCl=-lgc(Cl-) 、pAg=-lgc(Ag+)随加入AgNO3的体积变化如图所示,已知溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,Ksp(Ag2CrO4)=2.0×10-12 ,Ksp(Ag2SO4)=1.4×10-5,下列说法错误的是( )


| A.AgCl的沉淀溶解平衡常数Ksp数量级为10-10 |
| B.为防止指示剂失效,溶液应维持中性或弱碱性 |
| C.滴定中指示剂的有效浓度应维持在2.0×10-2 mol/L |
| D.滴定完后加入1mL 0.01mol/L H2SO4会产生新的沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据下列实验操作和现象能得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2支盛有5 mL不同浓度NaHSO3溶液的试管 中同时加入2 mL 5%H2O2溶液,观察实验现象 | 浓度越大,反应速率越快 |
| B | 向NaCl、Nal的混合稀溶液中滴入少量稀AgNO3 溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| C | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的 维生素C溶液,观察颜色变化 | 维生素C具有还原性 |
| D | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再 加入银氨溶液,未出现银镜 | 蔗糖为水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】镁离子是多种酶的活化剂,促进体内糖类转化及代谢,促进脂肪和蛋白质的合成。油料作物施镁可提高其含油量,镁还可以促进作物对硅的吸收。海水中含有丰富的镁资源,某同学设计了从模拟海水中制备MgO的实验方案:
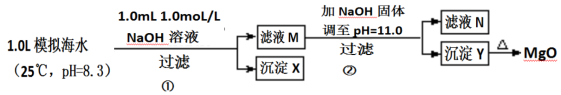
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。
下列说法不正确的是

| 模拟海水中的 离子浓度(mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
下列说法不正确的是
| A.沉淀物X为CaCO3 |
| B.滤液M中存在Mg2+,Ca2+ |
| C.滤液N中存在Ca2+,不存在Mg2+ |
| D.步骤②中若改为加入4.2gNaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物 |
您最近一年使用:0次