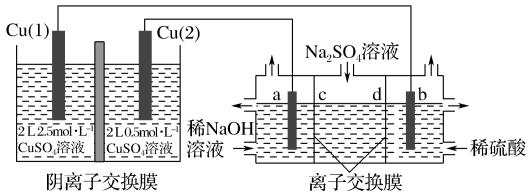
电化学原理在金属腐蚀、能量转换、物质合成等方面应用广泛。
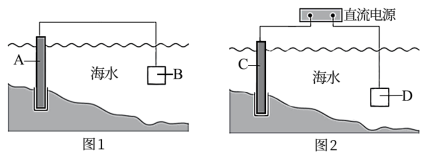
(1)通常可用图l、图2所示的两种方式减缓海水埘钢闸门A的腐蚀,则图l中材料B通常选择_________ (填字母序号),图2 中材料C最好选择_________ (填字母序号)。
a.钠块 b.铜块 c.锌块 d.石墨
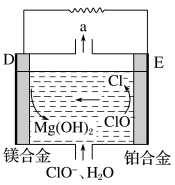
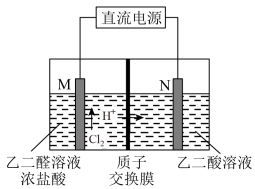
图3 图4
则图2中C上发生的主要电极反应式为___________________ 。
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①D为该燃料电池的________ 极(填“正”或“负”)。E电极上的电极反应式为_______ 。
②镁燃料电池负极容易发生自腐蚀使负极利用率降低,该过程中产生的气体a为_______ (填化学式)。
(3)乙醇酸(HOOC—CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸。
①乙二醛(OHC—CHO)与M电极的气体产物反应生成乙醛酸,则反应的化学方程式为____________ 。
②该电解装置工作中若有0.5molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为____________ mol。

(1)通常可用图l、图2所示的两种方式减缓海水埘钢闸门A的腐蚀,则图l中材料B通常选择
a.钠块 b.铜块 c.锌块 d.石墨


图3 图4
则图2中C上发生的主要电极反应式为
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①D为该燃料电池的
②镁燃料电池负极容易发生自腐蚀使负极利用率降低,该过程中产生的气体a为
(3)乙醇酸(HOOC—CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸。
①乙二醛(OHC—CHO)与M电极的气体产物反应生成乙醛酸,则反应的化学方程式为
②该电解装置工作中若有0.5molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
更新时间:2016-12-09 08:08:59
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求完成下列问题。
(1)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如下图所示:

①HS-在硫氧化菌作用下转化为 的电极反应式是
的电极反应式是_______ 。
②若维持该微生物电池中两种细菌的存在,则电池可以持续供电,原因是_______ 。
(2)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。

①放电过程中,Li+向_______ (填“负极”或“正极”)移动。
②负极反应式为_______ 。
③电路中每转移0.2mol电子,理论上生成_______ gPb。
(3)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如下图所示。

①a电极的电极反应式是_______ ;
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因是_______ 。
(1)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如下图所示:

①HS-在硫氧化菌作用下转化为
 的电极反应式是
的电极反应式是②若维持该微生物电池中两种细菌的存在,则电池可以持续供电,原因是
(2)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。

①放电过程中,Li+向
②负极反应式为
③电路中每转移0.2mol电子,理论上生成
(3)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如下图所示。

①a电极的电极反应式是
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是________ 。
(2)放电时,正极发生________ (填“氧化”或“还原”)反应。
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为______
 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:(1)高铁电池的负极材料是
(2)放电时,正极发生
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为
您最近一年使用:0次
【推荐1】能源是现代文明的原动力,随着常规能源的有限性以及环境问题的日益突出,以环保和可再生为特质的新能源越来越得到各国的重视。新能源包括风能、氢能、沼气、酒精、甲醇等,新能源的使用与研究在一定程度上助力中国实现“碳达峰、碳中和”。通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是_______ 。
(2)如图所示为CH4燃料电池的装置(A、B为多孔碳棒):______ (填A或B)处电极入口通甲烷,其电极反应式为:_______ ;当消耗甲烷的体积为11.2L(标准状况下)时,消耗KOH的质量为_______ g。
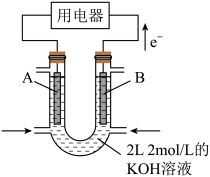
(3)用上述CH4燃料电池连接成如图装置。
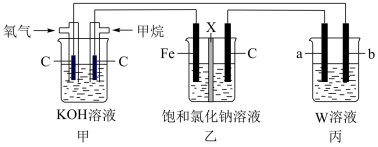
乙池中X为阳离子交换膜,石墨电极(C)作_______ 极,写出乙池总反应的离子方程式_______ 。
(4)若将乙装置中两电极用导线直接相连,则铁发生_______ 腐蚀,写出碳棒的电极反应式:______ 。若将乙装置中两电极连接电源的正负两极,铁连接电源的_______ 极(填“正”或“负”)时,可防止铁腐蚀。
(5)若丙中要实现铁上镀银,b电极材料为_______ 。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是
| A.该电池的电解液可以是稀硫酸 |
| B.放电时,若消耗1.5molCO2时,转移2mol电子 |
| C.放电时,电子从锂电极流出,通过电解液流回锂电极,构成闭合回路 |
| D.放电时,锂电极作正极 |

(3)用上述CH4燃料电池连接成如图装置。

乙池中X为阳离子交换膜,石墨电极(C)作
(4)若将乙装置中两电极用导线直接相连,则铁发生
(5)若丙中要实现铁上镀银,b电极材料为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】生活、生产中随处可见一些化学物质和化学反应现象,请完成下列问题。
(1)已知某温度时,醋酸的电离平衡常数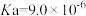 。醋酸的起始浓度为0.010mol/L,平衡时
。醋酸的起始浓度为0.010mol/L,平衡时
___________ mol/L(提示:醋酸的电离平衡常数很小,平衡时的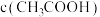 可近似为0.010mol/L)。
可近似为0.010mol/L)。
(2)常温下,等浓度NaOH(aq)和 (aq)按1:2体积比混合后pH<7,离子浓度大小关系为
(aq)按1:2体积比混合后pH<7,离子浓度大小关系为___________ 。
(3)日常生活中常用醋酸除水垢,但工业锅炉的水垢中常含有 ,需先用
,需先用___________ (填化学式)溶液处理,而后用盐酸去除。
(4)炒过菜的铁锅未及时洗净(残液中含有NaCl),不久便会锈蚀,其锈蚀过程属于___________ (填“析氢腐蚀”或“吸氧腐蚀”),正极的电极反应式为___________ 。
(1)已知某温度时,醋酸的电离平衡常数
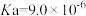 。醋酸的起始浓度为0.010mol/L,平衡时
。醋酸的起始浓度为0.010mol/L,平衡时
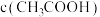 可近似为0.010mol/L)。
可近似为0.010mol/L)。(2)常温下,等浓度NaOH(aq)和
 (aq)按1:2体积比混合后pH<7,离子浓度大小关系为
(aq)按1:2体积比混合后pH<7,离子浓度大小关系为(3)日常生活中常用醋酸除水垢,但工业锅炉的水垢中常含有
 ,需先用
,需先用(4)炒过菜的铁锅未及时洗净(残液中含有NaCl),不久便会锈蚀,其锈蚀过程属于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】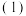 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:

负极区发生的反应有_________  写反应方程式
写反应方程式 。电路中转移
。电路中转移 电子,需消耗氧气
电子,需消耗氧气__________ 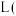 标准状况
标准状况 。
。
 电解法转化
电解法转化 可实现
可实现 资源化利用。电解
资源化利用。电解 制HCOOH的原理示意图如下。
制HCOOH的原理示意图如下。

 写出阴极
写出阴极 还原为
还原为 的电极反应式:
的电极反应式:________ 。
 电解一段时间后,阳极区的
电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是_____ 。
 可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接 或
或 ,可交替得到
,可交替得到 和
和 。
。

 制
制 时,连接
时,连接_______________ 。产生 的电极反应式是
的电极反应式是_________ 。
 改变开关连接方式,可得
改变开关连接方式,可得 。
。
 结合
结合 和
和 中电极3的电极反应式,说明电极3的作用:
中电极3的电极反应式,说明电极3的作用:___________ 。
 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
负极区发生的反应有
 写反应方程式
写反应方程式 。电路中转移
。电路中转移 电子,需消耗氧气
电子,需消耗氧气 标准状况
标准状况 。
。 电解法转化
电解法转化 可实现
可实现 资源化利用。电解
资源化利用。电解 制HCOOH的原理示意图如下。
制HCOOH的原理示意图如下。
 写出阴极
写出阴极 还原为
还原为 的电极反应式:
的电极反应式: 电解一段时间后,阳极区的
电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是 可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接 或
或 ,可交替得到
,可交替得到 和
和 。
。
 制
制 时,连接
时,连接 的电极反应式是
的电极反应式是 改变开关连接方式,可得
改变开关连接方式,可得 。
。 结合
结合 和
和 中电极3的电极反应式,说明电极3的作用:
中电极3的电极反应式,说明电极3的作用:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】图中甲池的总反应式为N2H4+O2=N2+2H2O。

(1)甲池是_____ (填“原电池”或“电解池”),其发生氧化反应的电极上的电极反应式为_____ 。
(2)乙池中石墨电极是_____ (填“正极”或“负极”或“阴极”或“阳极”),其电极反应式为_____ 。
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的_____ 。
(4)若加入9.8g的Cu(OH)2乙池能恢复到电解前的状态,则理论上甲池消耗标况下氧气的体积是_____ L。
(5)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为_____ g。

(1)甲池是
(2)乙池中石墨电极是
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的
| A.CuO | B.Cu(OH)2 | C.CuCO3 | D.CuSO4 |
(5)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】一种新型锂离子电池的工作原理如图所示。作为电池时,M极区为含有 、
、 、
、 等离子的水溶液,电极N是一种固态有机聚合物。回答下列问题:
等离子的水溶液,电极N是一种固态有机聚合物。回答下列问题:

(1)放电时,M极发生还原反应,它是___________ 极,电极反应式是___________ ;当外电路中每转移0.5mol电子时,电极N的质量变化是___________ (填“增大”或“减小”)___________ g。
(2)充电时,N极与外接电源的___________ 极连接,电极反应式是___________ , 通过
通过 透过层由
透过层由___________ 移动(填“左向右”或“右向左”)。
 、
、 、
、 等离子的水溶液,电极N是一种固态有机聚合物。回答下列问题:
等离子的水溶液,电极N是一种固态有机聚合物。回答下列问题:
(1)放电时,M极发生还原反应,它是
(2)充电时,N极与外接电源的
 通过
通过 透过层由
透过层由
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I、依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
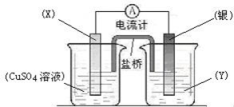
(1)电极X的材料是_______ ;电解质溶液Y是__________ 。
(2)银电极为电池的___ 极,发生的电极反应为____________ ; X电极上发生的电极反应为___________________ 。
(3)外电路中的电子是从_____ 电极流向_______ 电极。
II、如图所示,甲、乙为相互串联的两个电解池。请回答:
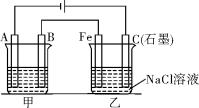
(1)甲池若为用电解原理精炼铜的装置,则A电极为________ 极,电极材料是________ ,电极反应为_______________________________ 电解质溶液可以是________________ 。
(2)乙池中Fe极电极反应为____________________________ 若在乙池中滴入少量酚酞溶液,电解一段时间后,铁极附近呈__________ 色。
(3)若甲池A极增重12.8 g,则乙池C(石墨)极放出气体在标准状况下的体积为___________ 。

(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
II、如图所示,甲、乙为相互串联的两个电解池。请回答:

(1)甲池若为用电解原理精炼铜的装置,则A电极为
(2)乙池中Fe极电极反应为
(3)若甲池A极增重12.8 g,则乙池C(石墨)极放出气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某实验小组依据甲烷燃烧的反应原理,设计如图所示的装置。

(1)甲池中负极的电极反应式为___________ 。
(2)乙池中A(石墨)电极的名称为___________ (填“正极”“负极”“阴极”或“阳极”),乙池中总反应为___________ 。
(3)若乙池中溶液体积为 ,当B电极质量增加
,当B电极质量增加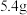 时,其
时,其 为
为___________ (忽略溶液体积变化);甲池中理论上消耗 的体积为
的体积为___________  (标准状况下);假设乙池、丙池中的溶液均足量,丙池中
(标准状况下);假设乙池、丙池中的溶液均足量,丙池中___________ (填“C”或“D”)极析出___________ g铜。

(1)甲池中负极的电极反应式为
(2)乙池中A(石墨)电极的名称为
(3)若乙池中溶液体积为
 ,当B电极质量增加
,当B电极质量增加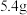 时,其
时,其 为
为 的体积为
的体积为 (标准状况下);假设乙池、丙池中的溶液均足量,丙池中
(标准状况下);假设乙池、丙池中的溶液均足量,丙池中
您最近一年使用:0次


 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导正极生成的
固体,它在高温下能传导正极生成的 (
( )。
)。 甲烷,假设化学能完全转化为电能,则转移电子的数目为
甲烷,假设化学能完全转化为电能,则转移电子的数目为 表示),需要消耗标准状况下氧气的体积为
表示),需要消耗标准状况下氧气的体积为