下列叙述不正确的是
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤沸点:NH3<PH3<AsH3
⑥已知2H2(g)+O2(g)=2H2O(l) △H=﹣571kJ·mol﹣1,则氢气的燃烧热为285.5kJ·mol﹣1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N.
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤沸点:NH3<PH3<AsH3
⑥已知2H2(g)+O2(g)=2H2O(l) △H=﹣571kJ·mol﹣1,则氢气的燃烧热为285.5kJ·mol﹣1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N.
| A.②④⑥ | B.①③⑤⑦ | C.②④⑥⑦ | D.⑤⑥⑦ |
更新时间:2016-12-09 08:43:50
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】25℃、l0lkPa下,煤炭、氢气、天然气和甲醇(CH3OH)四种燃料的热值(指一定条件下,单位质量的物质完全燃烧所放出的热量)依次是33kJ·g-1、143 kJ·g-1、56 kJ·g-1、23 kJ·g-1。则下列热化学方程式正确的是
| A.C(s)+l/2O2(g)=CO(g) △H= -396kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) △H= -286 kJ·mol-1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= -896 kJ·mol-1 |
| D.CH3OH(l)+O2(g)=CO2(g)+2H2O(l) △H= -736 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下述描述中,正确的是
| A.某化学反应其:△H=-122 kJ·mol-1,∆S=231 J·mol-1·K-1,则此反应在任何温度下都能自发进行 |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ·mol-1,则含20.0g NaOH的稀溶液与稀醋酸完全中和,放出大于28.7kJ的热量 |
| C.已知:2CO(g)+O2(g)=2CO2(g); ΔH=-566 kJ·mol-1 ,可知一氧化碳的标准燃烧热为:-283 kJ·mol-1 |
| D.向盛有硫酸铜水溶液的试管里加入过量氨水,可以得到深蓝色的透明溶液。向该溶液加入乙醇后,得到深蓝色的晶体是[Cu(NH3)4]SO4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】C和H2在生产、生活、科技中是非常重要的燃料。已知:
①2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
②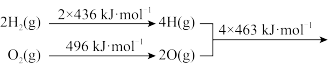 2H2O(g)
2H2O(g)
下列推断正确的是
①2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
②
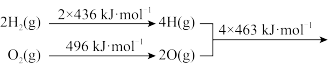 2H2O(g)
2H2O(g)下列推断正确的是
| A.C(s)的燃烧热为110.5kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(g) ΔH>0,ΔS<0,该反应是非自发反应 |
| C.C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.5kJ·mol-1 |
| D.将2molH2O(g)分解成H2(g)和O2(g),至少需要提供4×463kJ的热量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】W、X、Y、Z为元素周期表中的主族元素,且原子序数均不大于20,W的原子序数最大,X位于第二周期且原子的最外层电子数是内层电子数的3倍,Y的单质在空气中易形成一层致密氧化膜,且Y原子的最外层电子数为奇数,Z与Y同周期且相邻,W、Y原子的最外层电子数之和等于Z原子的最外层电子数。下列说法正确的是( )
| A.最简单离子的半径:Y>W>X |
| B.气态氢化物的稳定性:X>Z |
| C.最高价氧化物对应水化物的碱性:Y>W |
| D.Y、Z的氧化物均不能溶解于水中,且均为碱性氧化物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】第二主族元素R的单质及其相应氧化物的混合物12g,加足量水经完全反应后蒸干,得固体16g,试推测该元素可能为
| A.Mg | B.Ca | C.Be | D.Ba |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列说法正确的是
| A.Br的非金属性比I强,HBr比HI的稳定性强 |
| B.P的原子半径比N大,H3PO4 比HNO3 的酸性强 |
| C.Na熔点比K高, NaOH的碱性比KOH强 |
| D.非金属性Cl>Br>I,沸点HCl>HBr>HI |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】2019年诺贝尔化学奖颁给研究锂电池的科学家,一种用作锂电池电解液的锂盐的结构如图所示。其中,X位于第三周期,X原子的电子数为Z原子的两倍,W、Z、Y位于同一周期。下列叙述正确的是
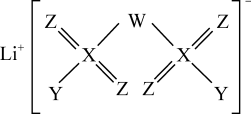

| A.W、X、Y、Z四种元素对应的简单氢化物的分子之间均能形成氢键 |
B.Z、W的非金属性强弱可以通过比较 和 和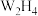 的热稳定性进行判断 的热稳定性进行判断 |
| C.X的氧化物对应的水化物均为强酸 |
D. 中各原子均满足8电子稳定结构 中各原子均满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】X、Y、Z、W、R属于短周期主族元素。X的原子半径是短周期主族元素中最大的;Y元素的原子最外层电子数为m,次外层电子数为n;Z元素的原子L层电子数为m+n,M层电子数为m-n;W与Z同主族;R元素原子与Y元素原子核外电子数之比为2︰1。下列叙述不正确的是( )
| A.X与Y形成的两种化合物中阴、阳离子的个数比均为1︰2 |
| B.Y的氢化物比R的氢化物稳定,且熔沸点高 |
| C.Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z |
| D.ZY2、WY2、RY2均溶于水,且都能与NaOH溶液反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】类推的思维方法在化学学习和研究中常会产生错误的结论,因此类推出的结论最终要经过实践的检验才能决定其正确与否。下列几种类推结论中正确的是
| A.Fe3O4可写成FeO·Fe2O3;Pb3O4也可写成PbO·Pb2O3 |
| B.晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子 |
| C.可电解熔融MgCl2来制取金属镁;也能电解熔融AlCl3来制取金属铝 |
| D.第二周期元素氢化物稳定性顺序是HF>H2O > NH3;则第三周期元素氢化物稳定性顺序也是HCl> H2S > PH3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】锡烯的结构与石墨烯结构相似,其俯视图、侧视图如图所示。已知锡烯的导电性只存在于材料的边缘或表面,随着锡烯层数的增加,显示出超导性。下列说法正确的是


A.SnO2+2C Sn+2CO↑,说明金属性Sn>C Sn+2CO↑,说明金属性Sn>C |
| B.锡烯中的Sn与石墨烯中的C的杂化方式相同 |
| C.锡烯层内存在金属键,层间不存在金属键 |
| D.Sn最外层电子逐级电离能存在关系:I5/I4≫ I4/I3 |
您最近一年使用:0次




