下图是病人输液用的葡萄糖(分子式为C6H12O6,相对分子质量为180)注射液的标签上的部分内容。

(1)该注射液中葡萄糖的质量分数是_____________ 。
(2)该注射液中葡萄糖的物质的量浓度是_______________ (小数点后保留两位)。
(3)实验室配制250 mL该浓度的葡萄糖溶液需要用天平称取葡萄糖粉末__________ g ,需要的主要玻璃仪器有量筒、烧杯、胶头滴管、______________ 、_______________ 等。
(4)下列操作不正确的是_______________ (填序号)。
①使用容量瓶前检查它是否漏水
②定容时仰视刻度线
③定容时加水超过刻度线,把水倒出一些,重新加水至刻度线
④定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀

(1)该注射液中葡萄糖的质量分数是
(2)该注射液中葡萄糖的物质的量浓度是
(3)实验室配制250 mL该浓度的葡萄糖溶液需要用天平称取葡萄糖粉末
(4)下列操作不正确的是
①使用容量瓶前检查它是否漏水
②定容时仰视刻度线
③定容时加水超过刻度线,把水倒出一些,重新加水至刻度线
④定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
更新时间:2016-12-09 01:13:39
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】计算填空
(1)相同物质的量的SO2和SO3,所含分子的数目之比为___________ ,所含原子数目之比为___________ ,所含氧原子的物质的量之比为___________ 。
(2)同温同压条件下,等质量的CO2与O2的体积比为___________ ,分子数之比为___________ ,原子数之比为___________ ,密度之比为___________ 。
(3)在Al2(SO4)3溶液中,若c( )=0.3mol/L,则c(Al3+)=
)=0.3mol/L,则c(Al3+)=___________ mol/L,c[Al2(SO4)3]=___________ mol/L。
(1)相同物质的量的SO2和SO3,所含分子的数目之比为
(2)同温同压条件下,等质量的CO2与O2的体积比为
(3)在Al2(SO4)3溶液中,若c(
 )=0.3mol/L,则c(Al3+)=
)=0.3mol/L,则c(Al3+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。回答下列问题:

(1)该硫酸的物质的量浓度为___________ mol/L。
(2)配制240 mL 4.6 mol/L的稀硫酸,若使用量筒量取,需量取该硫酸___________ mL。
(3)该硫酸与等体积的水混合所得溶液的质量分数___________ 49%(填<、>或=)。
(4)在制备稀硫酸的过程中,需要用到的主要玻璃仪器有容量瓶、玻璃棒、烧杯等,其中容量瓶在使用前需要___________ (填操作名称)。
(5)某溶液中仅含有0.2 mol/L 、0.25 mo/LFe2+、0.4 mol/LCl-及一定量的
、0.25 mo/LFe2+、0.4 mol/LCl-及一定量的 ,则
,则 物质的量浓度为
物质的量浓度为___________ mol/L (忽略水溶液中由水电离生成的H+和OH-)。

(1)该硫酸的物质的量浓度为
(2)配制240 mL 4.6 mol/L的稀硫酸,若使用量筒量取,需量取该硫酸
(3)该硫酸与等体积的水混合所得溶液的质量分数
(4)在制备稀硫酸的过程中,需要用到的主要玻璃仪器有容量瓶、玻璃棒、烧杯等,其中容量瓶在使用前需要
(5)某溶液中仅含有0.2 mol/L
 、0.25 mo/LFe2+、0.4 mol/LCl-及一定量的
、0.25 mo/LFe2+、0.4 mol/LCl-及一定量的 ,则
,则 物质的量浓度为
物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上制取氯酸钾的主要步骤为:
I.将Cl2通入石灰浆,在75℃左右充分反应,然后过滤;
II.向滤液中加入稍过量的KCl固体,进行适当操作可析出KClO3固体。
请回答下列问题:
(1)步骤I中总反应的化学方程式为6Ca(OH)2+ 6Cl2=Ca(ClO3)2+5CaCl2+ 6H2O 。
①标出反应中电子转移的方向和数目______________ 。
②滤液中Ca(ClO3)2与CaC12的物质的量之比n[Ca(ClO3)2]:n [CaCl2]____ l∶5 (填“> ”“< ”、或“=” ) ,理由是____________________________________ 。
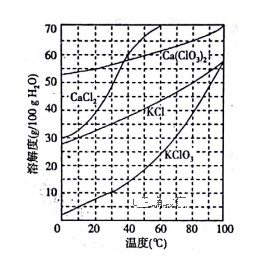
(2)下图是有关物质的溶解度曲线。步骤II中,若溶液中KClO3的含量为147g·L-1,则KClO3得物质的量浓度为_______________ 。从该溶液中尽可能多地析出KClO3 固体的方法是______________ 。
I.将Cl2通入石灰浆,在75℃左右充分反应,然后过滤;
II.向滤液中加入稍过量的KCl固体,进行适当操作可析出KClO3固体。
请回答下列问题:
(1)步骤I中总反应的化学方程式为6Ca(OH)2+ 6Cl2=Ca(ClO3)2+5CaCl2+ 6H2O 。
①标出反应中电子转移的方向和数目
②滤液中Ca(ClO3)2与CaC12的物质的量之比n[Ca(ClO3)2]:n [CaCl2]
(2)下图是有关物质的溶解度曲线。步骤II中,若溶液中KClO3的含量为147g·L-1,则KClO3得物质的量浓度为

您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题
(1)若实验过程中遇到下列情况,则会造成所配溶液的浓度偏低的是_______ (填字母)
a.加水时越过刻度线
b.未洗涤烧杯和玻璃棒
c.容量瓶内壁附有水珠而未干燥处理
d.定容时俯视刻度线
(2)向VmL上述浓度的NaOH溶液中,通入一定量的CO2后,然后向该溶液中逐滴中入1mol•L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如图所示:

①当加入45mL盐酸溶液时,产生二氧化碳的物质的量为_______
②计算所取氢氧化钠溶液的体积V=_______ mL
(3)取上述氢氧化钠溶液100mL,加入足量的铝,该反应的离子方程式为_______ ,反应生成的气体的物质的量为_______
(1)若实验过程中遇到下列情况,则会造成所配溶液的浓度偏低的是
a.加水时越过刻度线
b.未洗涤烧杯和玻璃棒
c.容量瓶内壁附有水珠而未干燥处理
d.定容时俯视刻度线
(2)向VmL上述浓度的NaOH溶液中,通入一定量的CO2后,然后向该溶液中逐滴中入1mol•L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如图所示:

①当加入45mL盐酸溶液时,产生二氧化碳的物质的量为
②计算所取氢氧化钠溶液的体积V=
(3)取上述氢氧化钠溶液100mL,加入足量的铝,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】pH试纸使用前能否用蒸馏水润湿?若用湿润的pH试纸测量溶液的pH对结果有何影响_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某小组开展“海带中碘的含量测定”活动。方案的主要步骤有:称量、灰化、过滤、氧化、滴定等,回答下列问题:
(1)灰化:称a g海带洗净并浸润少量酒精然后装入_______ 中(填标号),置高温炉内,在充足空气氛中燃烧成灰渣。将海带灰化的主要目的是_______ 。
A.不锈钢培养皿 B.烧杯 C.坩埚 D.试管
(2)氧化:向灰渣中滴加25mL蒸馏水浸泡、煮沸、过滤,向滤液中加入稀硫酸调至pH=3再加入过量的H2O2溶液,发生的离子方程为_______ 。若将漏斗直接置于容量瓶上过滤收集滤液(如图所示),存在安全风险,原因是_______ 。
(3)滴定:将(2)所得混合液在250 mL容量瓶中定容,移取25.00 mL于锥形瓶中,加入少许MnO2 ,滴加几滴淀粉溶液。用5 mL微量滴定管盛装b mol/L的Na2S2O3标准溶液进行滴定。三次平行测定的数据如下表。
(已知:I2+ 2Na2S2O3 = 2NaI+ Na2S4O6)
①加入MnO2的作用是_______ ,选用微量滴定管的原因是_______ 。
②滴定终点的现象是_______ 。
③碘元素的百分含量是_______ (列出计算式,用含a、b的字母表示)。
④本实验测定结果偏大,主要原因是_______ 。
(1)灰化:称a g海带洗净并浸润少量酒精然后装入
A.不锈钢培养皿 B.烧杯 C.坩埚 D.试管
(2)氧化:向灰渣中滴加25mL蒸馏水浸泡、煮沸、过滤,向滤液中加入稀硫酸调至pH=3再加入过量的H2O2溶液,发生的离子方程为

(3)滴定:将(2)所得混合液在250 mL容量瓶中定容,移取25.00 mL于锥形瓶中,加入少许MnO2 ,滴加几滴淀粉溶液。用5 mL微量滴定管盛装b mol/L的Na2S2O3标准溶液进行滴定。三次平行测定的数据如下表。
| 序号 | 1 | 2 | 3 |
| 标准溶液用量/mL | 2.715 | 2.905 | 2.725 |
①加入MnO2的作用是
②滴定终点的现象是
③碘元素的百分含量是
④本实验测定结果偏大,主要原因是
您最近一年使用:0次



