24. 铜是过渡元素。化合物中,铜常呈现+1价或+2价。
(1)铜原子的原子结构示意图:
_________________;
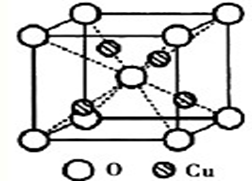
(2)右图为某铜矿晶体结构单元,该铜矿的化学式为
____________________。
(3)已知,铜的第一电离能为746kJ·mol
-1,第二电离能为1958kJ·mol
-1。请结合核外电子排布相关知识解释,铜第二电离能远远大于第一电离能的原因:
___________________。
(4)对于CuX(X为卤素)而言,铜与X形成的化学键极性越强,对应的CuX的溶解度越大。据此可知,CuCl的溶解度比CuI的溶解度
__________(填“更大”或“更小”);
(5)CO、NH
3都能提供孤电子对与Cu
+形成配合物。Cu
+与NH
3形成的配合物可表示为[Cu(NH
3)n]
+。该配合物中,Cu
+的4s轨道及4p轨道通过sp杂化接受NH
3提供的孤电子对。
①[Cu(NH
3)n]
+中n =
______________________;
②[Cu(NH
3)n]
+中Cu
+与n个氮原子构成的空间结构呈
________________型;
③[Cu(NH
3)n]
+溶液可用于吸收合成氨原料气中的CO,加热吸收CO后的溶液又将放出CO。加热分解放出CO的过程中,必须克服微粒间的作用力是
______________。
(6)+2价铜的氢氧化物难溶于水,但可溶于浓氨水形成配位数为4的配合物。写出氢氧化铜溶解于浓氨水的离子方程式
_____________________。