某班学生对BeCl2是离子化合物还是共价化合物进行集体探究,从经验看铍是金属元素,易失去电子,氯元素易得到电子,请回答以下问题:
(1)Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为_________ 化合物。
(2)工业上制取BeCl2方法是:将得到的BeCl2溶液在HCl气流中蒸干灼烧,防止BeCl2水解,请写出BeCl2水解的化学方程式__________________ 。
(3)经实验验证,熔融的BeCl2不能导电,说明它是_______ 化合物;BeCl2能溶于水,水溶液能导电,因它在溶液中能电离,写出它的电离方程式_________ 。
(4)在周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,判断BeCl2应与_____ (填MgCl2或AlCl3)化学性质更相似。
(5)0.1mol氢氧化铍恰好能和100mL0.2mol/L的氢氧化钠溶液发生反应,写出反应的化学方程式_________________ 。
(1)Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为
(2)工业上制取BeCl2方法是:将得到的BeCl2溶液在HCl气流中蒸干灼烧,防止BeCl2水解,请写出BeCl2水解的化学方程式
(3)经实验验证,熔融的BeCl2不能导电,说明它是
(4)在周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,判断BeCl2应与
(5)0.1mol氢氧化铍恰好能和100mL0.2mol/L的氢氧化钠溶液发生反应,写出反应的化学方程式
更新时间:2016-12-09 01:13:39
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:④_______ ;⑫________ 。
(2)画出原子的结构示意图:⑤_________ ;⑪________ 。
(3)在①~⑫元素中,金属性最强的元素是_________ ,非金属性最强的元素是_______ ,最不活泼的元素是________ (均填元素符号)。
(4)元素⑦与元素⑧相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是___________ (填序号)。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)元素⑥是构成地壳的主要元素之一,其氧化物是现代光学及光纤制品的基本原料,该氧化物的化学式为_____ 。且该氧化物可溶解在强碱NaOH中其离子方程式_______ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)写出下列元素符号:④
(2)画出原子的结构示意图:⑤
(3)在①~⑫元素中,金属性最强的元素是
(4)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)元素⑥是构成地壳的主要元素之一,其氧化物是现代光学及光纤制品的基本原料,该氧化物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑩九种元素在周期表中的位置。
请回答:
(1)在表里所列元素中,最高价氧化物对应的水化物中,酸性最强的是________ (填化学式 )。
(2)在②③④三种元素的最高价氧化物对应的水化物中,碱性最强 的是_______ (填化学式 )。电子式:________ 。
(3)⑦⑧⑨形成的气态氢化物中,最稳定的是________ (填化学式 )。
(4)元素⑥的氢化物的化学式是________ ,电子式:________
(5)⑧元素与②元素形成的化合物的电子式:________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ⑩ | ||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑤ | ⑨ |
请回答:
(1)在表里所列元素中,最高价氧化物对应的水化物中,酸性最强的是
(2)在②③④三种元素的最高价氧化物对应的水化物中,
(3)⑦⑧⑨形成的气态氢化物中,最稳定的是
(4)元素⑥的氢化物的化学式是
(5)⑧元素与②元素形成的化合物的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表给出14~17号元素的一些性质,请回答:
(1)它们所形成的氢化物中稳定性最差的是________ ,还原性最差的是_____ 。
(2)四种元素的非金属性随着元素原子序数的递增而逐渐_____________________ ,试从原子结构的角度加以解释____________ 。
(3)一定条件下,反应H2S+Cl2=2HCl+S能否发生?简述理由___________ 。
| 14Si | 15P | 16S | 17Cl | |
| 单质与H2反应的条件 | 高温 | 磷蒸气与H2能反应 | 加热 | 光照或点燃时发生爆炸 |
| 最高价氧化物的水化物 | H4SiO4弱酸 | H3PO4中强酸 | H2SO4强酸 | HClO4最强含氧酸 |
(1)它们所形成的氢化物中稳定性最差的是
(2)四种元素的非金属性随着元素原子序数的递增而逐渐
(3)一定条件下,反应H2S+Cl2=2HCl+S能否发生?简述理由
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,其中的编号代表对应的元素。
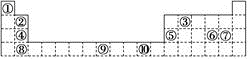
请回答下列问题:
(1)表中属于ds区的元素是________ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状物结构简式为________ 。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子数为________ 。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_______________________ 。
(5)画出⑨的外围电子排布图____________________________ .

请回答下列问题:
(1)表中属于ds区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状物结构简式为
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子数为
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
(5)画出⑨的外围电子排布图
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图是部分元素的第一电离能随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。
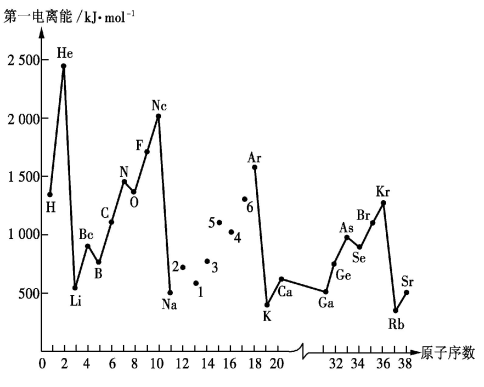
请回答下列问题:
(1)请写出ds区铜原子基态电子排布式_______
(2)同主族元素的第一电离能的变化规律是_______ 。
(3)图中第一电离能最小的元素在周期表中的位置是_______ 。
(4)根据对角线规则,Be、Al的最高价氧化物对应水化物的性质相似,它们都具有_______ 性,能证明 该性质的实验结论是
该性质的实验结论是______________ 。
(5)Na~Ar元素中,某元素M电离能如表所示:
①由此判断该元素是_______ ;
②分析图中同周期元素第一电离能的变化规律,推断:I1(Mg)_______ I1(M),其原因是_______ 。

请回答下列问题:
(1)请写出ds区铜原子基态电子排布式
(2)同主族元素的第一电离能的变化规律是
(3)图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,Be、Al的最高价氧化物对应水化物的性质相似,它们都具有
 该性质的实验结论是
该性质的实验结论是(5)Na~Ar元素中,某元素M电离能如表所示:
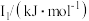 |  | 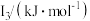 | 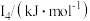 | 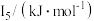 |
| 578 | 1817 | 2745 | 11575 | 14830 |
①由此判断该元素是
②分析图中同周期元素第一电离能的变化规律,推断:I1(Mg)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分。
请完成下列填空
(1) 的结构示意图为
的结构示意图为___________ 。
(2)第三周期中,最高价氧化物水化物酸性最强的是___________ (填化学式)。
(3)Mg、Cl和Ca中,离子半径由大到小的顺序是___________ (用离子符号表示)。
(4) 的电子式为
的电子式为___________ ; 结构式为
结构式为___________ 。
(5)写出一个能证明Cl的非金属性强于Br的离子方程式___________ 。
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在S的下方,下列推断正确的是___________(填字母序号)
(7)元素周期表中,某些主族元素与右下方的主族元素的性质具有相似性,如Be与Al,这种规律称为“对角线原则”。 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为___________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | Be | C | O | F | ||||
| 3 | Na | Mg | Al | S | Cl | |||
| 4 | Ca | Se | Br |
(1)
 的结构示意图为
的结构示意图为(2)第三周期中,最高价氧化物水化物酸性最强的是
(3)Mg、Cl和Ca中,离子半径由大到小的顺序是
(4)
 的电子式为
的电子式为 结构式为
结构式为(5)写出一个能证明Cl的非金属性强于Br的离子方程式
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在S的下方,下列推断正确的是___________(填字母序号)
A. 具有还原性 具有还原性 |
B. 的稳定性比 的稳定性比 强 强 |
C. 的酸性强于 的酸性强于 |
D. 在一定条件下可与NaOH溶液反应 在一定条件下可与NaOH溶液反应 |
 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为
您最近一年使用:0次



