如图是部分元素的第一电离能随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。
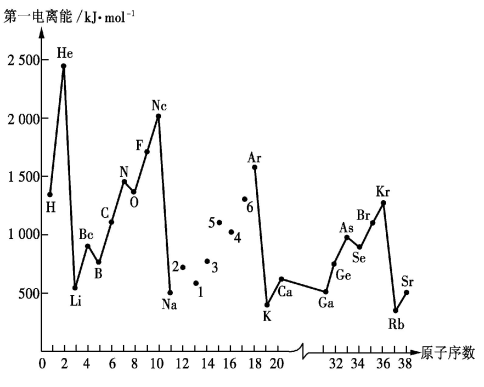
请回答下列问题:
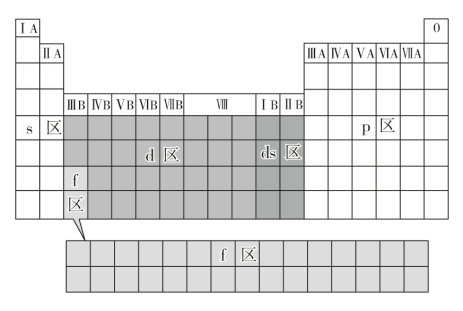
(1)请写出ds区铜原子基态电子排布式_______
(2)同主族元素的第一电离能的变化规律是_______ 。
(3)图中第一电离能最小的元素在周期表中的位置是_______ 。
(4)根据对角线规则,Be、Al的最高价氧化物对应水化物的性质相似,它们都具有_______ 性,能证明 该性质的实验结论是
该性质的实验结论是______________ 。
(5)Na~Ar元素中,某元素M电离能如表所示:
①由此判断该元素是_______ ;
②分析图中同周期元素第一电离能的变化规律,推断:I1(Mg)_______ I1(M),其原因是_______ 。

请回答下列问题:
(1)请写出ds区铜原子基态电子排布式
(2)同主族元素的第一电离能的变化规律是
(3)图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,Be、Al的最高价氧化物对应水化物的性质相似,它们都具有
 该性质的实验结论是
该性质的实验结论是(5)Na~Ar元素中,某元素M电离能如表所示:
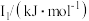 |  | 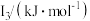 | 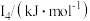 | 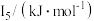 |
| 578 | 1817 | 2745 | 11575 | 14830 |
①由此判断该元素是
②分析图中同周期元素第一电离能的变化规律,推断:I1(Mg)
更新时间:2021-01-15 23:46:34
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】据南方日报报道,广东省珠江第二大水系北江流域因当地矿业的开发,造成附近河底沉积物中铊含量严重超标,致使当地人“靠江不饮北江水”。铊(Tl)是某超导体材料的组成元素之一,Tl3+与Ag在酸性介质中发生反应Tl3++2Ag=Tl++2Ag+。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第____ 周期第______ 族。
(2)铊与下列某种元素位于同一主族,该元素是________ 。
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是______ (填序号)。
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是________ 。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第
(2)铊与下列某种元素位于同一主族,该元素是
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(1)铍的最高价氧化物对应水化物的化学式是______ ,属于两性化合物,证明这一结论的有关离子方程式为______ 、______ 。
(2)若已知反应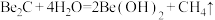 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为______ 。
(3)科学家证实, 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是______ 。用电子式表示 的形成过程:
的形成过程:______ 。
(1)铍的最高价氧化物对应水化物的化学式是
(2)若已知反应
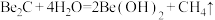 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为(3)科学家证实,
 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是 的形成过程:
的形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下列8种化学符号: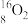 、
、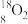 、
、 、
、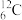 、
、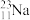 、
、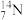 、
、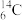 、
、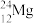 。
。
(1)表示核素的符号共______ 种。
(2)互为同位素的是________________ 。
(3)质量相同的H216O和D216O所含中子数之比为________ 。
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:__________________ 。
(5)Be(OH)2与Mg(OH)2可用____________________ 试剂鉴别。
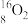 、
、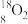 、
、 、
、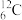 、
、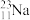 、
、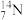 、
、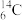 、
、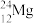 。
。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:
(5)Be(OH)2与Mg(OH)2可用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列填空。
(1)某元素气态氢化物溶于水后溶液显碱性,其元素符号为______ ;其轨道表示式为______ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为______ ,C+的结构示意图为______ 。
(3)某元素的原子最外层电子排布式为nsnnpn+2,则n=______ ;该元素符号为______ 。
(4)某元素的正三价离子的3d能级为半充满,D的元素符号为______ ,其基态原子的电子排布式为______ 。
(5)某元素基态原子的M层全充满,N层没有成对电子且只有一个未成对电子,其元素符号为______ ,该元素分布在______ 区。
(1)某元素气态氢化物溶于水后溶液显碱性,其元素符号为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为
(3)某元素的原子最外层电子排布式为nsnnpn+2,则n=
(4)某元素的正三价离子的3d能级为半充满,D的元素符号为
(5)某元素基态原子的M层全充满,N层没有成对电子且只有一个未成对电子,其元素符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】天然气广泛用于民用燃气和化工生产,主要成分是CH4,还含有少量H2S和水蒸气。
(1)碳、氢、氧、硫四种元素中,最外层电子数是电子层数两倍的是______ (填元素符号),非金属性最强元素的原子核外电子排布式为__________________ 。
(2) 天然气的用途之一是利用甲烷高温分解制炭黑。若分解16g甲烷,需要吸收258kJ的热量,写出该反应的热化学方程式:____________________________________________ 。
(3)天然气在使用前,需进行脱硫处理。用纯碱溶液吸收其中的H2S,过程中会生成两种酸式盐,该反应的离子方程式为____________________________________________ 。若改用NaOH溶液吸收H2S,从通入气体至过量,溶液中c(S2-)的变化趋势是______________________ 。
(4)微波加热技术的原理是:利用极性分子内部正负电荷分布不均匀的特点,在电磁场作用下会频繁运动摩擦,使温度升高。用甲烷制炭黑的工业生产中,是否适合使用该技术加热,原因是_____________ 。硫化氢分子结构与水分子相似,加热时硫化氢较水更易分解得到氢气,从元素周期律角度分析其原因___________________ 。
(1)碳、氢、氧、硫四种元素中,最外层电子数是电子层数两倍的是
(2) 天然气的用途之一是利用甲烷高温分解制炭黑。若分解16g甲烷,需要吸收258kJ的热量,写出该反应的热化学方程式:
(3)天然气在使用前,需进行脱硫处理。用纯碱溶液吸收其中的H2S,过程中会生成两种酸式盐,该反应的离子方程式为
(4)微波加热技术的原理是:利用极性分子内部正负电荷分布不均匀的特点,在电磁场作用下会频繁运动摩擦,使温度升高。用甲烷制炭黑的工业生产中,是否适合使用该技术加热,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据要求填空
(1)选择下列物质填空(填写序号):①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤CaBr2 ⑥NaH ⑦ K3C60 ⑧石墨 ⑨氯化铵 ⑩铜晶体 熔化时不破坏化学键的有_______ ;含有非极性共价键的有_______ 。
(2)性质比较:(填“>”、“=”或“<”,下同)
①第一电离能Mg_______ Al,解释原因_______
②酸性强弱HClO4_______ HClO3,解释原因_______
(3)下图为几种晶体或晶胞的示意图(用名称填写)
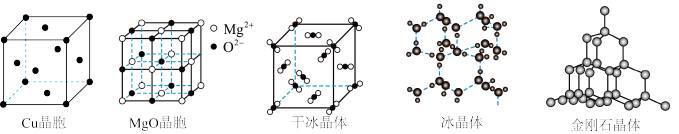
①上述晶体中,粒子之间以共价键结合形成的晶体是_______ 。
②冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为_______ 。
(1)选择下列物质填空(填写序号):①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤CaBr2 ⑥NaH ⑦ K3C60 ⑧石墨 ⑨氯化铵 ⑩铜晶体 熔化时不破坏化学键的有
(2)性质比较:(填“>”、“=”或“<”,下同)
①第一电离能Mg
②酸性强弱HClO4
(3)下图为几种晶体或晶胞的示意图(用名称填写)

①上述晶体中,粒子之间以共价键结合形成的晶体是
②冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据已学知识,回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是____ ,占据该能层电子的电子云轮廓图形状为____ 。
(2)写出3p轨道上有2个未成对电子的元素的符号____ 或____ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是____ 。
(4)已知铁是26号元素,写出Fe的价层电子排布式____ ;在元素周期表中,该元素在____ (填“s”“p”“d”“f”或“ds”)区。
(5)写出与N同主族的As的基态原子的核外电子排布式____ 。
(6)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为____ 。
(7)写出Fe2+的核外电子排布式:____ 。
(8)Zn2+的核外电子排布式为____ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出Fe的价层电子排布式
(5)写出与N同主族的As的基态原子的核外电子排布式
(6)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(7)写出Fe2+的核外电子排布式:
(8)Zn2+的核外电子排布式为
您最近一年使用:0次
【推荐1】Mn、Fe均为第4周期过渡金属元素,两元素的部分电离能数据如下表:
回答下列问题:
(1)Mn元素基态原子价电子层的电子排布式为__ ;比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是__ 。
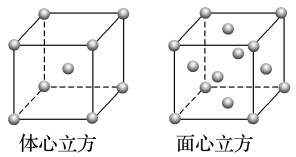
(2)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为__ ,Fe原子配位数之比为__ 。
| 元素 | Mn | Fe | |
| 电离能/(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(1)Mn元素基态原子价电子层的电子排布式为
(2)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据下列五种元素的电离能数据(单位∶ kJ/mol),回答下列问题。
(1)在周期表中,最可能处于同一族的是_______ 。
A.Q和 R B.S和T C. T和U D.R和T E.R和U
(2)电解它们的熔融氯化物,以下过程最可能正确的是_________ 。
A.Q2++2e-→Q B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→T
(3)它们的氯化物的化学式,最可能正确的是________
A. QCl2 B. RCl C. SCl3 D.TCl
(4)S 元素最可能是________ 素
A.S区元素 B.稀有气体元素 C.p 区元素 D .准金属
(5)下列元素中,化学性质和物理性质最像Q元素的是_____ 。
A.氦(1s2) B.铍(1s12s2) C.锂(1s22s1) D.氢(1s1)
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
A.Q和 R B.S和T C. T和U D.R和T E.R和U
(2)电解它们的熔融氯化物,以下过程最可能正确的是
A.Q2++2e-→Q B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→T
(3)它们的氯化物的化学式,最可能正确的是
A. QCl2 B. RCl C. SCl3 D.TCl
(4)S 元素最可能是
A.S区元素 B.稀有气体元素 C.p 区元素 D .准金属
(5)下列元素中,化学性质和物理性质最像Q元素的是
A.氦(1s2) B.铍(1s12s2) C.锂(1s22s1) D.氢(1s1)
您最近一年使用:0次