A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
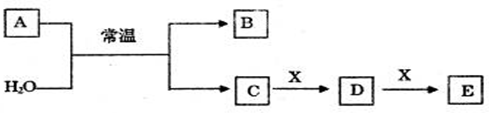
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:____________________________________________________________ 。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为_____________________________________ 。
②X可能为__________________ (填代号)。
A.NaHCO3b.Na2CO3 C.Na2SO3 D.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的氧化产物为_____________ 。
②若X为非金属单质,通常为黑色粉末,写出E的化学式______________ 。
③若X为一种造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为______ (填代号)。
A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。
①A与H2O反应的化学反应方程式为__________________________________ 。
②检验溶液D中还可能存在Fe2+的方法是_________________________________ (注明试剂、现象)。

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为
②X可能为
A.NaHCO3b.Na2CO3 C.Na2SO3 D.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的氧化产物为
②若X为非金属单质,通常为黑色粉末,写出E的化学式
③若X为一种造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为
A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。
①A与H2O反应的化学反应方程式为
②检验溶液D中还可能存在Fe2+的方法是
更新时间:2016-12-09 09:34:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有关物质的转化关系如下图所示(反应中部分物质已略去)。A、C、G、K、M 为单质,其中G、K、L、M 为气体,其中M能使带火星的木条复燃,D可用作耐高温材料,B为黑色磁性氧化物, E为常见的强碱。
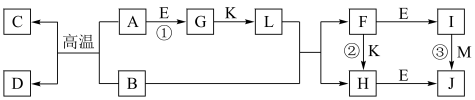
(1)D的化学式为__ 。
(2)写出反应①的离子方程式:__ 。
(3)写出反应②的离子方程式:__ 。
(4)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目:__ 。

(1)D的化学式为
(2)写出反应①的离子方程式:
(3)写出反应②的离子方程式:
(4)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某单质A经如图所示的过程,A、B、C、D均含有同一种元素,请回答下列问题:
A B
B C
C D
D
(1)若A为淡黄色固体,B是有刺激性气味的无色气体。D的化学式_________
(2)若C为淡黄色固体。
①C的电子式为________
②D中化学键类型________ (填标号 )
A.离子键 B.极性键 C.非极性键
③写出C→D反应的离子方程式:________
(3)若C为红棕色气体。
写出C→D反应的化学方程式:___________________________________
A
 B
B C
C D
D(1)若A为淡黄色固体,B是有刺激性气味的无色气体。D的化学式
(2)若C为淡黄色固体。
①C的电子式为
②D中化学键类型
A.离子键 B.极性键 C.非极性键
③写出C→D反应的离子方程式:
(3)若C为红棕色气体。
写出C→D反应的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】物质A~M在一定条件下的转化关系如图(部分产物及反应条件未列出).其中,I是既能与强酸反应生成氢气又能与强碱反应生成氢气的金属,K是一种红棕色气体,D的俗名叫铁红,A是形成酸雨的主要气体.
请填写下列空白:
(1)推导出下列物质的化学式:C:_____ E:_____
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_______________ (填写序号).
(3)反应④的离子方程式是:______________________ .
(4)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是:_______________________ .
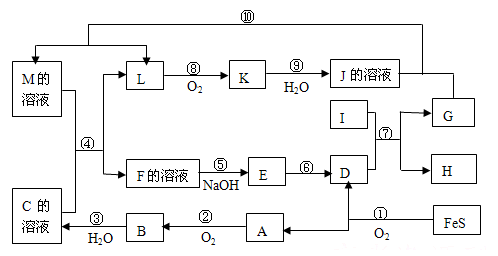
请填写下列空白:
(1)推导出下列物质的化学式:C:
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是
(3)反应④的离子方程式是:
(4)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是:
您最近半年使用:0次
【推荐1】Ⅰ.用覆铜板制作印刷电路板时,常用FeCl3溶液作腐蚀液。某兴趣小组在实验室进行了模拟。
(模拟实验Ⅰ)
向盛有4mL 0.2mol/L FeCl3溶液的试管中,加入一块铜片(Cu过量),反应一段时间后,溶液黄色褪去。
(分析解释)
(1)FeCl3与Cu反应的离子方程式是_______ 。
(2)为检验反应生成的Fe2+,最宜选择的试剂是_______ (填字母)。
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液
(继续实验Ⅱ)
为验证上述实验中Fe3+是否完全反应,该小组同学取上层清液于另一支试管中,滴入3滴0.1mol/L KSCN溶液。结果发现,上层清液中立即产生白色沉淀,同时滴入处局部出现红色,振荡后红色立即消失。
(查阅资料)
为解释该异常现象产生的原因,同学们查阅资料得知:
①2CuCl2+4KSCN=2CuSCN↓+(SCN)2+4KCl
②CuSCN为白色固体,几乎不溶于水;
③(SCN)2与Cl2的性质相似。
(继续实验Ⅲ)
(分析解释)
(3)实验Ⅱ中白色沉淀的成分是_______ (填化学式)。
(4)请结合资料,用离子方程式解释实验Ⅱ中“滴入KSCN溶液处局部出现红色”的原因_______ 。
Ⅱ.水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O +O2+xOH-=Fe3O4↓+S4O
+O2+xOH-=Fe3O4↓+S4O +2H2O。请回答下列问题:
+2H2O。请回答下列问题:
(5)水热法制备Fe3O4纳米颗粒的反应中,被氧化的元素为_______ (填元素符号)。
(6)该反应的化学方程式中,x=_______ 。
(7)每生成1mol Fe3O4,反应转移的电子为_______ mol。
(模拟实验Ⅰ)
向盛有4mL 0.2mol/L FeCl3溶液的试管中,加入一块铜片(Cu过量),反应一段时间后,溶液黄色褪去。
(分析解释)
(1)FeCl3与Cu反应的离子方程式是
(2)为检验反应生成的Fe2+,最宜选择的试剂是
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液
(继续实验Ⅱ)
为验证上述实验中Fe3+是否完全反应,该小组同学取上层清液于另一支试管中,滴入3滴0.1mol/L KSCN溶液。结果发现,上层清液中立即产生白色沉淀,同时滴入处局部出现红色,振荡后红色立即消失。
(查阅资料)
为解释该异常现象产生的原因,同学们查阅资料得知:
①2CuCl2+4KSCN=2CuSCN↓+(SCN)2+4KCl
②CuSCN为白色固体,几乎不溶于水;
③(SCN)2与Cl2的性质相似。
(继续实验Ⅲ)
| 实验方案 | 现象 | |
| 步骤Ⅰ | 取4mL 0.2mol/L FeCl2溶液,向其中滴加3滴0.1mol/L KSCN溶液 | 无明显现象 |
| 步骤Ⅱ | 取4mL 0.2mol/L CuCl2溶液,向其中滴加3滴0.1mol/L KSCN溶液 | 产生白色沉淀 |
(3)实验Ⅱ中白色沉淀的成分是
(4)请结合资料,用离子方程式解释实验Ⅱ中“滴入KSCN溶液处局部出现红色”的原因
Ⅱ.水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O
 +O2+xOH-=Fe3O4↓+S4O
+O2+xOH-=Fe3O4↓+S4O +2H2O。请回答下列问题:
+2H2O。请回答下列问题:(5)水热法制备Fe3O4纳米颗粒的反应中,被氧化的元素为
(6)该反应的化学方程式中,x=
(7)每生成1mol Fe3O4,反应转移的电子为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】工业上用黄铁矿为原料制备硫酸的流程如图所示:
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为___________ 。
(2)已知: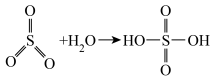 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式___________ 。
(3)写出步骤①的化学方程式___________ 。
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因___________ 。
(5)下列说法正确的是___________ 。
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象___________ 。(供选择的试剂:KSCN溶液、稀硫酸、稀盐酸、KMnO4溶液、品红溶液、NaOH溶液)
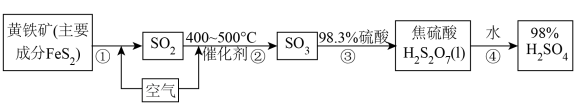
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为
(2)已知:
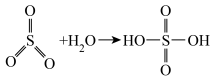 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式(3)写出步骤①的化学方程式
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因
(5)下列说法正确的是
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以柠檬酸、硫酸亚铁、氨水等为原料制备食品添加剂—柠檬酸铁铵[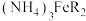 ,M=488g·mol-1]的流程如下所示:
,M=488g·mol-1]的流程如下所示:_______ 。
(2)欲检验FeSO4溶液是否被完全氧化,选用的试剂为_______。
(3)上述流程中,以13.90g绿矾(FeSO4·7H2O)配制FeSO4溶液,经各步骤后,最终制取得19.52g柠檬酸铁铵,则柠檬酸铁铵的产率为_______ 。
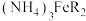 ,M=488g·mol-1]的流程如下所示:
,M=488g·mol-1]的流程如下所示: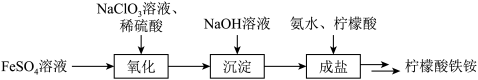
(2)欲检验FeSO4溶液是否被完全氧化,选用的试剂为_______。
| A.NaOH溶液 | B.KSCN溶液 | C.酸性KMnO4溶液 | D.新制氯水 |
(3)上述流程中,以13.90g绿矾(FeSO4·7H2O)配制FeSO4溶液,经各步骤后,最终制取得19.52g柠檬酸铁铵,则柠檬酸铁铵的产率为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知有A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,B、C组成的某一种化合物能引起温室效应,常温下,金属D单质投入水中能与水剧烈反应,常温下E单质是常见的气体。请按要求回答下列几个问题:
(1)D的元素名称为:___ 。
(2)E在周期表中的位置为:___ 。
(3)C原子的结构示意图为:___ 。
(4)C、D、E三种元素的离子半径从大到小的顺序为(用元素符号表示)___ 。
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为___ (用对应的化学式表示)。
(6)B、C组成的能引起温室效应的化合物的电子式为___ 。
(1)D的元素名称为:
(2)E在周期表中的位置为:
(3)C原子的结构示意图为:
(4)C、D、E三种元素的离子半径从大到小的顺序为(用元素符号表示)
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为
(6)B、C组成的能引起温室效应的化合物的电子式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】元素在周期表中的位置、原子结构、元素的性质三者之间关系密切。根据下列短周期主族元素的原子结构特点,回答下列问题:
(1)最外层电子数是核外电子总数的 的非金属元素是
的非金属元素是_______ (填元素符号或化学式,下同)。
(2)周期序数与主族序数相等的金属元素有_______ 。
(3)最外层电子数是电子层数3倍的元素形成的双原子分子为_______ 。
(4)主族序数是电子层数的2倍且具有8个中子的核素为_______ 。
(5)K层和M层电子数相等的元素与氮元素形成的化合物为_______ 。
(1)最外层电子数是核外电子总数的
 的非金属元素是
的非金属元素是(2)周期序数与主族序数相等的金属元素有
(3)最外层电子数是电子层数3倍的元素形成的双原子分子为
(4)主族序数是电子层数的2倍且具有8个中子的核素为
(5)K层和M层电子数相等的元素与氮元素形成的化合物为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
(1)①与⑦组成的化合物的电子式_______ ,该化合物是由_______ (填“极性”“非极性”)键形成的。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______ ,碱性最强的化合物的电子式 是_______ 。
(3)用电子式表示元素⑥与⑨的化合物的形成过程_______ 。
(4)最高价氧化物是两性氧化物的元素原子结构示意图是_______ ;写出该元素单质与氢氧化钠溶液反应的离子方程式_______ 。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是_______ (要求用离子符号表示)。
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为_______ 。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)用电子式表示元素⑥与⑨的化合物的形成过程
(4)最高价氧化物是两性氧化物的元素原子结构示意图是
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂,常见制备方法如下。
(1)氯酸钾氧化法:化学反应方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KC1+3C12,每生成3mol KH(IO3)2,反应中转移的电子数为________ ,向反应后溶液中加_________ 溶液得到KIO3。
(2)一种由含碘废水制取碘酸钾的工艺如下:
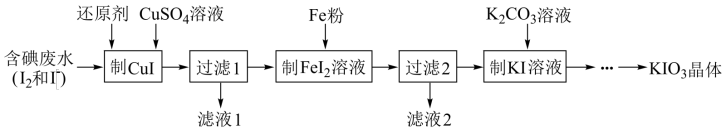
①进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤液中可通过滴加______ 盐溶液来检验其是否已洗涤干净。
②“制FeI2”时,发生反应的化学方程式为________________ 。
③在KIO3、KHSO3的酸性混合溶液中加入少量KI(催化剂)和淀粉,不停地搅拌,反应机理为:第一步IO +5I-+6H+=3I2+3H2O 第二步反应的离子方程式为
+5I-+6H+=3I2+3H2O 第二步反应的离子方程式为________________ 。
(3)山东省已下调食用盐碘含量标准每千克盐含碘25毫克(波动范围为18~33mg·kg-1)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL 6.000×10-4mol· L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O = 2I-+S4O
= 2I-+S4O 。计算该食盐试样中碘元素的含量
。计算该食盐试样中碘元素的含量________ mg·kg-1。
(1)氯酸钾氧化法:化学反应方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KC1+3C12,每生成3mol KH(IO3)2,反应中转移的电子数为
(2)一种由含碘废水制取碘酸钾的工艺如下:

①进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤液中可通过滴加
②“制FeI2”时,发生反应的化学方程式为
③在KIO3、KHSO3的酸性混合溶液中加入少量KI(催化剂)和淀粉,不停地搅拌,反应机理为:第一步IO
 +5I-+6H+=3I2+3H2O 第二步反应的离子方程式为
+5I-+6H+=3I2+3H2O 第二步反应的离子方程式为(3)山东省已下调食用盐碘含量标准每千克盐含碘25毫克(波动范围为18~33mg·kg-1)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL 6.000×10-4mol· L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O
 = 2I-+S4O
= 2I-+S4O 。计算该食盐试样中碘元素的含量
。计算该食盐试样中碘元素的含量
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。

回答下列问题:
(1)黄铁矿中硫元素的化合价为________________ 。
(2)欲得到更纯的NaHSO3,反应①应通入_____________ (填 “过量”或“不足量”)的SO2气体。
(3)加热NaHSO3制备Na2S2O5的化学方程式为__________________________________________ 。
(4)商品Na2S2O5中可能存在Na2SO4,检验其中含有 的方法是
的方法是_________________________ 。
(5)一般用 K2Cr2O7滴定分析法测定还原铁粉纯度。
①配制K2Cr2O7溶液:如图所示是配制0.03mol/L 250ml标准溶液的过程示意图。
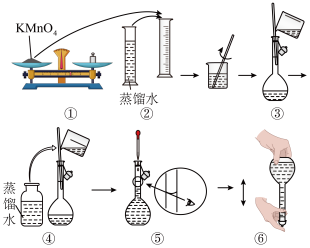
请你观察图示判断,其中不正确的操作有____ (填序号)。
②下列操作会导致所配溶液浓度偏大的是_____ (填标号)。
A.K2Cr2O7溶解后,未冷却就立即转移至容量瓶中
B.容量瓶洗涤后未干燥
C.定容时仰视容量瓶刻度线
D.称量时使用了生锈的砝码
③称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的Fe2+。反应式: +6Fe2+ +14H+ = 2Cr3+ +6Fe3+ +7H2O,某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为
+6Fe2+ +14H+ = 2Cr3+ +6Fe3+ +7H2O,某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为____________________ %。

回答下列问题:
(1)黄铁矿中硫元素的化合价为
(2)欲得到更纯的NaHSO3,反应①应通入
(3)加热NaHSO3制备Na2S2O5的化学方程式为
(4)商品Na2S2O5中可能存在Na2SO4,检验其中含有
 的方法是
的方法是(5)一般用 K2Cr2O7滴定分析法测定还原铁粉纯度。
①配制K2Cr2O7溶液:如图所示是配制0.03mol/L 250ml标准溶液的过程示意图。

请你观察图示判断,其中不正确的操作有
②下列操作会导致所配溶液浓度偏大的是
A.K2Cr2O7溶解后,未冷却就立即转移至容量瓶中
B.容量瓶洗涤后未干燥
C.定容时仰视容量瓶刻度线
D.称量时使用了生锈的砝码
③称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的Fe2+。反应式:
 +6Fe2+ +14H+ = 2Cr3+ +6Fe3+ +7H2O,某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为
+6Fe2+ +14H+ = 2Cr3+ +6Fe3+ +7H2O,某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】CoCl2可用于电镀,是一种性能优越的电池前驱材料,由含钴矿(Co 元素主要以Co2O3、 CoO 的形式存在,还含有Fe、Si、Cu、Zn、Mn、Ni、Mg、Ca 元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图:

已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2 难溶于水。
②CoCl2∙6H2O 的熔点为 86℃,易溶于水、乙醚等;常温下稳定无毒,加热至 110~120℃时, 失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的 pH 见表:
回答下列问题:
(1)“550℃焙烧”的目的是_______ 。
(2)“浸取”的过程中,用离子方程式表示 Na2S2O5的主要作用是_______ 。
(3)滤液 1 中加入 NaClO3溶液的作用是_______ 。
(4)加入Na2CO3 溶液生成滤渣 2 的主要离子方程式为_______ 。
滤液 3 经过多次萃取与反萃取制备CoCl2 晶体:
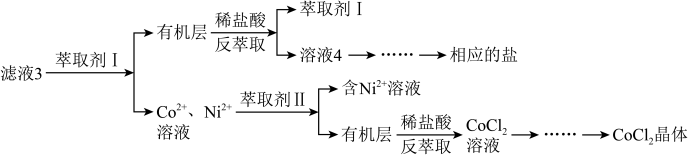
(5)滤液 3 中加入萃取剂 I,然后用稀盐酸反萃取的目的是_______ 。
(6)制备晶体CoCl2∙6H2O,需在减压环境下烘干的原因是_______ 。
(7)测定产品的纯度:称取 CoCl2∙6H2O 样品,将其用适当试剂转化为 CoC2O4,再转化为(NH4)2C2O4溶液,稀硫酸酸化后用高锰酸钾标准溶液滴定,滴定终点的判定_______ 。

已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2 难溶于水。
②CoCl2∙6H2O 的熔点为 86℃,易溶于水、乙醚等;常温下稳定无毒,加热至 110~120℃时, 失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的 pH 见表:
| Co3+ | Fe3+ | Cu2+ | Co2+ | Fe2+ | Zn2+ | Mn2+ | Mg2+ | |
| 开始沉淀 pH | 0.3 | 2.7 | 5.5 | 7.2 | 7.6 | 7.6 | 8.3 | 9.6 |
| 完全沉淀 pH | 1.1 | 3.2 | 6.6 | 9.2 | 9.6 | 9.2 | 9.3 | 11.1 |
(1)“550℃焙烧”的目的是
(2)“浸取”的过程中,用离子方程式表示 Na2S2O5的主要作用是
(3)滤液 1 中加入 NaClO3溶液的作用是
(4)加入Na2CO3 溶液生成滤渣 2 的主要离子方程式为
滤液 3 经过多次萃取与反萃取制备CoCl2 晶体:

(5)滤液 3 中加入萃取剂 I,然后用稀盐酸反萃取的目的是
(6)制备晶体CoCl2∙6H2O,需在减压环境下烘干的原因是
(7)测定产品的纯度:称取 CoCl2∙6H2O 样品,将其用适当试剂转化为 CoC2O4,再转化为(NH4)2C2O4溶液,稀硫酸酸化后用高锰酸钾标准溶液滴定,滴定终点的判定
您最近半年使用:0次



