已知有A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,B、C组成的某一种化合物能引起温室效应,常温下,金属D单质投入水中能与水剧烈反应,常温下E单质是常见的气体。请按要求回答下列几个问题:
(1)D的元素名称为:___ 。
(2)E在周期表中的位置为:___ 。
(3)C原子的结构示意图为:___ 。
(4)C、D、E三种元素的离子半径从大到小的顺序为(用元素符号表示)___ 。
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为___ (用对应的化学式表示)。
(6)B、C组成的能引起温室效应的化合物的电子式为___ 。
(1)D的元素名称为:
(2)E在周期表中的位置为:
(3)C原子的结构示意图为:
(4)C、D、E三种元素的离子半径从大到小的顺序为(用元素符号表示)
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为
(6)B、C组成的能引起温室效应的化合物的电子式为
更新时间:2021-01-29 13:44:20
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表列出了①~⑧8种元素在周期表中的位置。请回答:
(1)写出⑤元素下一周期同主族的元素的符号_______ ,⑥位于元素周期表的位置_______ 。
(2)在这些元素中,最高价氧化物对应的水化物呈两性化合物的是_______ (用化学式表示)。金属性最强的元素是_______ (填元素符号)。离子半径最大的元素的离子符号是_______ 。
(3)⑥元素与②元素形成的X2Y2型化合物的电子式_______ 。
(4)①元素与④元素形成的最简单化合物分子构型为_______ 。它与氯气反应在光照条件下发生反应(装置如图),实验现象及解释均正确的是_______ 。

族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 3 | ② | ③ | ⑧ |
(2)在这些元素中,最高价氧化物对应的水化物呈两性化合物的是
(3)⑥元素与②元素形成的X2Y2型化合物的电子式
(4)①元素与④元素形成的最简单化合物分子构型为

| 现象 | 解释 | |
| A | 量筒内气体颜色逐渐变浅 | 甲烷被氯气还原 |
| B | 量筒内出现少量白雾 | 生成HCl气体 |
| C | 量筒内壁产生油状液滴 | 油状液体是纯净物CCl4 |
| D | 量筒中液面降低 | 生成产物全部是液态 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大,D、G同主族,A与B、C、D能形成电子数相同的二种常见分子,E、F的原子序数之和是D的原子序数的3倍,D、E、F的简单离子具有相同电子层结构。
(1)三种元素的名称:B______ ,D______ ,F______ 。
(2)A与D、A与G均可形成18e-的化合物。两种化合物在水溶液中反应的化学方程式为:________________________________
(3)A、D、E三种元素中的两种或三种形成的物质中,含有非极性键的离子化合物的电子式为:____________ ;只含离子键的化合物的电子式为:______________ 。
(4)E离子的半径_____________ (填“大于” “小于”或“等于”)F离子的半径;E 和F元素最高价氧化物对应的水化物之间反应的离子方程式为:______________ 。
(5)写出由上述各种元素形成的粒子中与BC-电子数相等的三种分子的化学式______ 、________ 、_______ 。
(1)三种元素的名称:B
(2)A与D、A与G均可形成18e-的化合物。两种化合物在水溶液中反应的化学方程式为:
(3)A、D、E三种元素中的两种或三种形成的物质中,含有非极性键的离子化合物的电子式为:
(4)E离子的半径
(5)写出由上述各种元素形成的粒子中与BC-电子数相等的三种分子的化学式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】锂离子电池是目前广泛应用的二次电池。由于锂资源储量有限,科学家将目光转向钾离子电池。
(1) 用作钾离子电池的电解液溶剂,可由
用作钾离子电池的电解液溶剂,可由 与有机物X经加成反应得到。
与有机物X经加成反应得到。
① 中碳原子杂化方式为
中碳原子杂化方式为_______ 。
②X的结构简式为_______ 。
(2)由于离子半径:
_______  (填“>”或“<”),在充、放电过程中,
(填“>”或“<”),在充、放电过程中, 的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。
的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。
(3)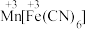 可用作钾离子电池的正极材料,其晶胞结构如下图所示。
可用作钾离子电池的正极材料,其晶胞结构如下图所示。

①距离 最近的
最近的 有
有_______ 个。
②第三电离能 :
: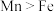 ,结合原子结构解释原因:
,结合原子结构解释原因:_______ 。
③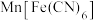 放电后转化为
放电后转化为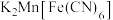 ,充电时物质的变化如下:
,充电时物质的变化如下: 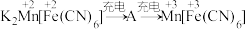 。充电时生成A的电极反应式:
。充电时生成A的电极反应式:_______ (请标注A中 和
和 的化合价)。
的化合价)。
(1)
 用作钾离子电池的电解液溶剂,可由
用作钾离子电池的电解液溶剂,可由 与有机物X经加成反应得到。
与有机物X经加成反应得到。①
 中碳原子杂化方式为
中碳原子杂化方式为②X的结构简式为
(2)由于离子半径:

 (填“>”或“<”),在充、放电过程中,
(填“>”或“<”),在充、放电过程中, 的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。
的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。(3)
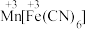 可用作钾离子电池的正极材料,其晶胞结构如下图所示。
可用作钾离子电池的正极材料,其晶胞结构如下图所示。
①距离
 最近的
最近的 有
有②第三电离能
 :
: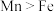 ,结合原子结构解释原因:
,结合原子结构解释原因:③
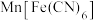 放电后转化为
放电后转化为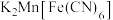 ,充电时物质的变化如下:
,充电时物质的变化如下: 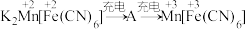 。充电时生成A的电极反应式:
。充电时生成A的电极反应式: 和
和 的化合价)。
的化合价)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、M四种短周期元素,原子半径M>Z>X>Y,其中X、Y处在同一周期,X、Z处在同一主族。Z原子核内质子数等于X、Y原子核内质子数之和,原子核外最外层上的电子数是M原子核外最外层电子数的4倍。请回答:
(1)这两种元素名称分别是X_______ ,M_______ 。
(2)Y的简单离子结构示意图是_______ ;Z在周期表中的位置是_______ 。
(3)X、Y、Z这三种元素的气态氢化物的稳定性由大而小的顺序是_______ 。
(4)X与Y形成的三原子分子甲的结构式是_______ ,Y与M形成的原子个数比为1∶1的化合物乙的电子式是_______ ,甲与乙反应的化学方程式是_______ 。
(1)这两种元素名称分别是X
(2)Y的简单离子结构示意图是
(3)X、Y、Z这三种元素的气态氢化物的稳定性由大而小的顺序是
(4)X与Y形成的三原子分子甲的结构式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)B的轨道排布式是_____________________________________ ,A、B、C、D的第一电离能由小到大的顺序为___________________________________________ 。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________________ ;
(3)A的最高价含氧酸根离子中,其中心原子采取____________ 杂化,D的低价氧化物分子的空间构型是___________________________ 。
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为________________ ;(每个球均表示1个原子) 若相邻A原子和E原子间的距离为a nm,阿伏伽德罗常数为NA,则该晶体的密度为_____________ g/cm3(用含a、NA的符号表示)。

(1)B的轨道排布式是
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是
(3)A的最高价含氧酸根离子中,其中心原子采取
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期元素A、B、C、D、E的原子序数依次增大。已知:
①C的简单气态氢化物遇湿润的红色石蕊试纸变蓝色;
②A与D可以形成原子个数比分别为2∶1、1∶1的两种液态化合物X和Y,A、E同主族,C与B、D相邻;
③A、B、C、D四种元素组成一种化合物F,其组成原子数之比为5∶1∶1∶3。
请回答下列问题:
(1)C原子在周期表的位置为_____________ ;D的原子结构示意图为_____________ ;写出化合物EDA的电子式__________ 。
(2)C的最高价氧化物对应的水化物与其气态氢化物反应可生成盐,写出其化学式___________ ;写出Y的结构式_____________ 。
(3)F溶液与足量EDA的稀溶液混合,其离子方程式为_______________________ 。
(4)氯气与C的简单气态氢化物相遇有白烟及C2生成,写出反应方程式______________ 。
(5)用CH4可以消除汽车尾气中氮氧化物的污染。
已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1
N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1
2NO2(g) N2O4(g) ΔH=-56.9 kJ·mol-1
N2O4(g) ΔH=-56.9 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:____________________ 。
①C的简单气态氢化物遇湿润的红色石蕊试纸变蓝色;
②A与D可以形成原子个数比分别为2∶1、1∶1的两种液态化合物X和Y,A、E同主族,C与B、D相邻;
③A、B、C、D四种元素组成一种化合物F,其组成原子数之比为5∶1∶1∶3。
请回答下列问题:
(1)C原子在周期表的位置为
(2)C的最高价氧化物对应的水化物与其气态氢化物反应可生成盐,写出其化学式
(3)F溶液与足量EDA的稀溶液混合,其离子方程式为
(4)氯气与C的简单气态氢化物相遇有白烟及C2生成,写出反应方程式
(5)用CH4可以消除汽车尾气中氮氧化物的污染。
已知:CH4(g)+2NO2(g)
 N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1
N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-12NO2(g)
 N2O4(g) ΔH=-56.9 kJ·mol-1
N2O4(g) ΔH=-56.9 kJ·mol-1写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
请回答下列问题:
(1)若元素E的某种核素中中子数比质子数多3个,表示这种核素的符号为___________ ;
(2)把D的单质放到NaOH溶液中,反应的离子方程式为:______________________ ;
(3)甲的电子式:____________________________________________ ;
(4)有100mL MgCl2和丙的混合溶液,其中c(Mg2+)=0.2mol·L-1,c(Cl-)=1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4mol·L-1NaOH溶液的体积是:________ mL;
(5)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的质量比为__________ 。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
(1)若元素E的某种核素中中子数比质子数多3个,表示这种核素的符号为
(2)把D的单质放到NaOH溶液中,反应的离子方程式为:
(3)甲的电子式:
(4)有100mL MgCl2和丙的混合溶液,其中c(Mg2+)=0.2mol·L-1,c(Cl-)=1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4mol·L-1NaOH溶液的体积是:
(5)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的质量比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,W的最简单氢化物甲是一种能使湿润的红色石蕊试纸变蓝的无色气体,常用作制冷剂,Y的金属性是所有短周期主族元素中最强的,Z与X属于同一主族,Z与Y属于同一周期。
(1)元素W在周期表位置___________ ;
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为___________ ;
(3)若X的未成对电子数为2,则其与H元素以原子个数比1:1形成的化合物电子式为___________ ;
(4)X、Y、Z的原子半径由小到大为___________ ;(填对应字母)
(5)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为___________ ,该产物化肥中含有的化学键有___________ 。
(1)元素W在周期表位置
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为
(3)若X的未成对电子数为2,则其与H元素以原子个数比1:1形成的化合物电子式为
(4)X、Y、Z的原子半径由小到大为
(5)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐3】W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为____________________ 。
(2)W与Y 可形成化合物W2Y,该化合物的电子式为______________ 。
(3)X的硝酸盐水溶液显______ 性,用离子方程式解释原因___________________________________________ 。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为____________________________ 。
(5)比较Y、Z气态氢化物的稳定性_____ >_______ (用分子式表示)。
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:_____ >_____ >______ >______ 。
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量,写出该反应的热化学方程式:_______________________ 。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(2)W与Y 可形成化合物W2Y,该化合物的电子式为
(3)X的硝酸盐水溶液显
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
(5)比较Y、Z气态氢化物的稳定性
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量,写出该反应的热化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的原子核内无中子,B、F在元素周期表中的相对位置 如图,B与氧元素能形成两种无色气体,D是地壳中含量最多的元素,E是地壳中含量最多的金属元素。
(1)BF2的结构式为____________ 。
(2)D和 F氢化物中沸点较高的___________________ 填化学式)。
(3)工业制取E单质的化学方程式为______________ 。
(4)在微电子工业中,C的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______________ 。
(5)火箭使用B2A8C2作燃料,N2O4为氧化剂,燃烧放出的巨大能量能把火箭送入 太空,并且产生三种无污染的气体,其化学方程式为____________ 。
| B | ||
| F |
(1)BF2的结构式为
(2)D和 F氢化物中沸点较高的
(3)工业制取E单质的化学方程式为
(4)在微电子工业中,C的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
(5)火箭使用B2A8C2作燃料,N2O4为氧化剂,燃烧放出的巨大能量能把火箭送入 太空,并且产生三种无污染的气体,其化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】四种常见的短周期非金属元素在周期表中的相对位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的三倍。
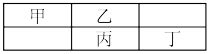
请用化学用语回答:
(1)丙在元素周期表中的位置___________________________
(2)丁单质的电子式___________________________________
(3)乙的两种常见单质分别是__________ ,_______________
(4)甲乙丙丁的气态氢化物水溶液显酸性的是(写化学式)________ ,________
(5)氢元素和乙组成的化合物中,既含有极性共价键又含有非极性共价键的是(写化学式)__________ 。此化合物可将碱性工业废水中CN-氧化为可溶性碳酸盐和氨,相应的离子方程式_________________
(6)电解丁的钠盐饱和溶液的离子方程式________________________________
(7)若甲的元素符号为X。已知①X2(g)+2O2(g)=X2O4(l) △H=-19.5kJ/mol
②X2H4(l)+O2(g)=X2(g)+2H2O(g) △H=-534.2kJ/mol则液态X2H4和液态的X2O4反应生成气态X2和气态H2O的热化学方程式为____________________

请用化学用语回答:
(1)丙在元素周期表中的位置
(2)丁单质的电子式
(3)乙的两种常见单质分别是
(4)甲乙丙丁的气态氢化物水溶液显酸性的是(写化学式)
(5)氢元素和乙组成的化合物中,既含有极性共价键又含有非极性共价键的是(写化学式)
(6)电解丁的钠盐饱和溶液的离子方程式
(7)若甲的元素符号为X。已知①X2(g)+2O2(g)=X2O4(l) △H=-19.5kJ/mol
②X2H4(l)+O2(g)=X2(g)+2H2O(g) △H=-534.2kJ/mol则液态X2H4和液态的X2O4反应生成气态X2和气态H2O的热化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有部分短周期元素的性质或原子结构如下表:
(1)元素X位于周期表中的位置___ ,它的一种核素可测定文物的年代,这种核素的符号___
(2)元素Y的原子结构示意图为____ ,写出YH3和Y的最高价氧化物对应的水化物反应的化学方程式___ 。
(3)元素Z与元素T相比,非金属性较强的是__ (填元素符号),下列表述能证明这一事实的是__ 。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与NaOH溶液反应
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中酸性最强的是__ (填酸的化学式,下同),酸性最弱的是___ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7 |
(2)元素Y的原子结构示意图为
(3)元素Z与元素T相比,非金属性较强的是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与NaOH溶液反应
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中酸性最强的是
您最近一年使用:0次



