已知X、Y是两种性质相似的短周期元素。
Ⅰ.若X、Y是相邻相似 ,它们的单质都必须采用电解法制备,但都无需密封保存,
,它们的单质都必须采用电解法制备,但都无需密封保存,
(1)X离子的结构示意图_____________ 。(2)Y元素在周期表中位置__________ 。
Ⅱ.若X、Y是同族相似 ,X是形成化合物种类最多的元素。
,X是形成化合物种类最多的元素。
(3)I2O3以氧化XO,常用于测定XO含量,已知:①2I2(s)+5O2(g)=2I2O5(s)△H=-75.66kJ·mol-1
②2XO(g)+O2(g)=2XO2(g) △H=-566.0kJ·mol-1。请写出XO(g)与I2O5(s)和XO2(g)的热化学方程式:______ 。
(4)工业上用X单质与Y的氧化物反应制取Y单质的过程中,YO是反应中间产物,隔绝空气时YO和NaOH溶液反应(产物之一是Na2YO3)的离子方程式是_________________________ 。
Ⅲ.若X、Y是对角相似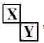 ,X、Y的最高价含氧酸的浓溶液都有强氧化性。
,X、Y的最高价含氧酸的浓溶液都有强氧化性。
(5)下列试剂都可以证明X、Y的最高价含氧酸的浓溶液都有强氧化性的是_________ 。
(6)HA是含有X元素的一元酸,常温下,将0.2mol/L的HA溶液与等体积、等浓度的NaOH溶液混合,所得溶液(假设溶液体积可以相加)中部分微粒组成及浓度如右图所示,图中N表示______ (填微粒符号)。


(7)某化工厂设计要求:空气中YO2含量不得超过0.02mg/L。某同学用右图所示简易装置测定空气中的YO2含量:准确移取10mL5×10-4mol/L的标准碘水溶液,注入试管中,加2-3滴淀粉指示剂,此时溶液呈蓝色,在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,假设该同学的测量是准确的,则他抽气的次数至少为_______ 次时方可说明该厂空气中的YO2含量达标。
Ⅰ.若X、Y是相邻相似
 ,它们的单质都必须采用电解法制备,但都无需密封保存,
,它们的单质都必须采用电解法制备,但都无需密封保存,(1)X离子的结构示意图
Ⅱ.若X、Y是同族相似
 ,X是形成化合物种类最多的元素。
,X是形成化合物种类最多的元素。(3)I2O3以氧化XO,常用于测定XO含量,已知:①2I2(s)+5O2(g)=2I2O5(s)△H=-75.66kJ·mol-1
②2XO(g)+O2(g)=2XO2(g) △H=-566.0kJ·mol-1。请写出XO(g)与I2O5(s)和XO2(g)的热化学方程式:
(4)工业上用X单质与Y的氧化物反应制取Y单质的过程中,YO是反应中间产物,隔绝空气时YO和NaOH溶液反应(产物之一是Na2YO3)的离子方程式是
Ⅲ.若X、Y是对角相似
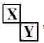 ,X、Y的最高价含氧酸的浓溶液都有强氧化性。
,X、Y的最高价含氧酸的浓溶液都有强氧化性。(5)下列试剂都可以证明X、Y的最高价含氧酸的浓溶液都有强氧化性的是
| A.铁片 | B.铜片 | C.二氧化硫 | D.木炭 |
(6)HA是含有X元素的一元酸,常温下,将0.2mol/L的HA溶液与等体积、等浓度的NaOH溶液混合,所得溶液(假设溶液体积可以相加)中部分微粒组成及浓度如右图所示,图中N表示


(7)某化工厂设计要求:空气中YO2含量不得超过0.02mg/L。某同学用右图所示简易装置测定空气中的YO2含量:准确移取10mL5×10-4mol/L的标准碘水溶液,注入试管中,加2-3滴淀粉指示剂,此时溶液呈蓝色,在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,假设该同学的测量是准确的,则他抽气的次数至少为
更新时间:2019-01-30 18:14:09
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】雾霾天气严重影响人们的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染。
请回答下列问题:
(1)将一定量的某利M2.5样品用蒸馏水溶解制成待测试样(忽略OH-)。常温下测得该训试样的组成及其浓度如下表:根据表中数据判断该试样的pH=___________ 。
(2)汽车尾气中NOx和CO的生成:①已知汽缸中生成NO的反应为:N2(g)+O2(g) 2NO(g)△H>0恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是____。
2NO(g)△H>0恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是____。
(3)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ·mol-1
C(s)+1/2O2(g)=CO(g)△H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:_____________ 。
②洗涤含SO2的烟气。下列可作为洗涤含SO2的烟气的洗涤剂的是___________ 。
A.浓氨水B.碳酸氢钠饱和溶液C.FeCl2饱和溶液D.酸性CaCl2饱和溶液
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为______ ,在n(NO)/n(CO)=1的条件下,为更好的除去NOx物质,应控制的最佳温度在_____ K左右。
(5)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
①写出NO与活性炭反应的化学方程式_____ ,②若T1<T2,则该反应的△H______ O(填”>”、“<”或“=”)。
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为__________ 。
请回答下列问题:
(1)将一定量的某利M2.5样品用蒸馏水溶解制成待测试样(忽略OH-)。常温下测得该训试样的组成及其浓度如下表:根据表中数据判断该试样的pH=
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度mol/L |  |  |  |  |  |  |
 2NO(g)△H>0恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是____。
2NO(g)△H>0恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是____。| A.混合气体的密度不再变化 |
| B.混合气体的压强不再变化 |
| C.N2、O2、NO的物质的量之比为1∶1∶2 |
| D.氧气的转化率不再变化 |
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ·mol-1
C(s)+1/2O2(g)=CO(g)△H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:
②洗涤含SO2的烟气。下列可作为洗涤含SO2的烟气的洗涤剂的是
A.浓氨水B.碳酸氢钠饱和溶液C.FeCl2饱和溶液D.酸性CaCl2饱和溶液
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为

(5)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
物质  | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】氨气是重要的化工原料
(1)已知:N2(g)+O2(g)= 2NO(g) △H= +180.5kJ·mol-1
4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H= - 905kJ·mol-1
2H2(g)+O2(g)= H2O(g) △H= - 483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式:_____________________ ,
(2)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:______________________ ,科学家利用此原理,设计成氨气和氧气燃料电池, 则通入氨气的电极是_________ (填“正极”或“负极”);碱 性条件下,该电极发生反应的电极反应式为_______________________ 。
(3)一定条件下,某密闭容器中发生反应 4NH3(g)+5O2(g) 4NO(g )+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g )+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是___________ (填字母代号)。
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(4)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为_______ {已知Ksp[Mg(OH)2]=4.0×10-12]}
(1)已知:N2(g)+O2(g)= 2NO(g) △H= +180.5kJ·mol-1
4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H= - 905kJ·mol-1
2H2(g)+O2(g)= H2O(g) △H= - 483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式:
(2)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:
(3)一定条件下,某密闭容器中发生反应 4NH3(g)+5O2(g)
 4NO(g )+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g )+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(4)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】高铁酸钠(Na2FeO4)是一种新型、高效的水处理剂,与水反应的化学方程式为:4Na2FeO4+10H2O=4Fe(OH)3+3O2↑+8NaOH。电解制备 Na2FeO4装置示意图如下。
(1)a是电源的______________ 极(填“正”或“负”)。电解时,石墨电极附近溶液的碱性____________ (填“增强”、“减弱”或“不变”)。
(2)铁电极的反应式为__________________________ 。
(3)维持一定的电流强度和电解温度,NaOH起始浓度对Na2FeO4浓度影响如下图(电解液体积相同情况下进行实验)。
①电解3.0h内,随NaOH起始浓度增大,Na2FeO4浓度变化趋势是______________ (填“增大”、“不变”或“减小”)。
②当NaOH起始浓度为16mol·L-1,1.0~2.0h内生成Na2FeO4的速率是_____________ mol·L-1·h-1。
③A 点与B 点相比,n[Fe(OH)3]: A_____________ B (填“>”、 “=”或“<” )
(4)提纯电解所得Na2FeO4,采用重结晶、过滤、洗涤、低温烘干的方法,则洗涤剂最好选用______________ 溶液(填标号)和异丙醇。
A.Fe(NO3)3B.NH4ClC.CH3COONa
(5)次氯酸钠氧化法也可以制得Na2FeO4。
已知 2H2(g)+O2(g)=2H2O (1) △H=akJ·mol-1
NaCl(aq)+ H2O(1)=NaClO(aq)+H2(g) △H=bkJ·mol-1
4Na2FeO4(aq)+10H2O(1)=4Fe(OH)3(s)+3O2(g)+8NaOH(aq) △H=c kJ·mol-1
反应 2Fe(OH)3(s)+3NaClO(aq)+4NaOH(aq)=2Na2FeO4(aq)+3NaCl(aq)+5H2O(1)的△H=______________ kJ·mol-1。

(1)a是电源的
(2)铁电极的反应式为
(3)维持一定的电流强度和电解温度,NaOH起始浓度对Na2FeO4浓度影响如下图(电解液体积相同情况下进行实验)。

①电解3.0h内,随NaOH起始浓度增大,Na2FeO4浓度变化趋势是
②当NaOH起始浓度为16mol·L-1,1.0~2.0h内生成Na2FeO4的速率是
③A 点与B 点相比,n[Fe(OH)3]: A
(4)提纯电解所得Na2FeO4,采用重结晶、过滤、洗涤、低温烘干的方法,则洗涤剂最好选用
A.Fe(NO3)3B.NH4ClC.CH3COONa
(5)次氯酸钠氧化法也可以制得Na2FeO4。
已知 2H2(g)+O2(g)=2H2O (1) △H=akJ·mol-1
NaCl(aq)+ H2O(1)=NaClO(aq)+H2(g) △H=bkJ·mol-1
4Na2FeO4(aq)+10H2O(1)=4Fe(OH)3(s)+3O2(g)+8NaOH(aq) △H=c kJ·mol-1
反应 2Fe(OH)3(s)+3NaClO(aq)+4NaOH(aq)=2Na2FeO4(aq)+3NaCl(aq)+5H2O(1)的△H=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为______ (填元素符号);
②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______ (填化学式)。
(2)①、④、⑤、⑧四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___________ 。
(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)___________ 。
a.MnO2 b.FeCl3 c.Na2SO3 d.CaCO3
(4)由表中元素形成的物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为________________ 。
| IA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑥的原子半径由大到小的顺序为
②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(2)①、④、⑤、⑧四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 c.Na2SO3 d.CaCO3
(4)由表中元素形成的物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)元素D在周期表中的位置__________ 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)______ 。
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有________________________________________________________________________ 。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:________________________________________________________________________ 。
若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:_______________________________________________________________ 。
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方程式______________________________________________________________________ 。
(1)元素D在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】按要求填空
(1)X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的一种单质具有特殊臭味,Z与X原子最外层电子数相同。回答下列问题:
①由上述元素组成的化合物中,既有共价键又有离子键的化合物有(写2种)___________ ,
②X和Y组成的化合物可将碱性工业废水中的CNˉ氧化为碳酸盐和氨,相应的离子方程式为___________ 。
(2)在一定条件下,NanRO3和NaI在硫酸介质中反应,发生反应生成NaR、I2和Na2SO4.已知该变化过程中,0.1mol的NanRO3参加反应时共转移0.6mol电子:
①NanRO3中R元素的化合价是___________ ,
②R元素的最外层电子数为___________ 。
(3)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1︰16,则x值是___________ 。
(4)已知M2O 可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O
可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O 的还原产物中,M为+3价,又知c(M2O
的还原产物中,M为+3价,又知c(M2O )=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为
)=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为___________ 。
(1)X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的一种单质具有特殊臭味,Z与X原子最外层电子数相同。回答下列问题:
①由上述元素组成的化合物中,既有共价键又有离子键的化合物有(写2种)
②X和Y组成的化合物可将碱性工业废水中的CNˉ氧化为碳酸盐和氨,相应的离子方程式为
(2)在一定条件下,NanRO3和NaI在硫酸介质中反应,发生反应生成NaR、I2和Na2SO4.已知该变化过程中,0.1mol的NanRO3参加反应时共转移0.6mol电子:
①NanRO3中R元素的化合价是
②R元素的最外层电子数为
(3)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1︰16,则x值是
(4)已知M2O
 可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O
可与R2ˉ作用,R2ˉ被氧化为R的单质,M2O 的还原产物中,M为+3价,又知c(M2O
的还原产物中,M为+3价,又知c(M2O )=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为
)=0.3mol/L的溶液100mL可与c(R2ˉ)=0.6mol/L的溶液150mL恰好完全反应,则n值为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为________ ,W、D、E三种元素的简单离子的离子半径由大到小顺序为__________ (用离子符号表示)。
(2)由A、B、W三种元素组成的18电子微粒的电子式为_______________ 。
(3)经测定A2W2为二元弱酸,其酸性比碳酸弱,写出其第一步电离的电离方程式_________________ ,实验室常用稀硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_____________________________________ 。
(4)元素D的单质在一定条件下与元素A的单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,该反应的化学方程式为____________ 。
(5)元素D的某化合物呈淡黄色,可与氯化亚铁溶液反应,生成红褐色沉淀,且无气体生成.则该反应的离子方程式为___________________________ 。
(1)E元素在周期表中的位置为
(2)由A、B、W三种元素组成的18电子微粒的电子式为
(3)经测定A2W2为二元弱酸,其酸性比碳酸弱,写出其第一步电离的电离方程式
(4)元素D的单质在一定条件下与元素A的单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,该反应的化学方程式为
(5)元素D的某化合物呈淡黄色,可与氯化亚铁溶液反应,生成红褐色沉淀,且无气体生成.则该反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。

请回答下列问题:
(1)f在周期表中的位置为______________ ;x形成的阴离子的结构示意图为_____________________ 。
(2)比较d、e常见离子的半径大小:__________________ (填化学式,下同);比较g、h的最高价氧化物对应水化物的酸性强弱:_______________________ 。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶2∶1 ∶4,其化学式为__________________________ 。
②能形成共价化合物,写出其中一种的结构简式____________________________ 。

请回答下列问题:
(1)f在周期表中的位置为
(2)比较d、e常见离子的半径大小:
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶2∶1 ∶4,其化学式为
②能形成共价化合物,写出其中一种的结构简式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】下表为部分短周期元素化合价及相应氢化物沸点的数据:
已知:①A与D可形成化合物AD2、AD3,可用于制备强酸甲;
②B与D可形成化合物BD、BD2,可用于制备强酸乙。
请回答:
(1)表中属于第三周期元素的是_________________________ (用表中元素编号填写)。
(2)写出H的最高价氧化物的电子式:__________________________ ;
比较A、D、G三种简单阴离子的半径大小:r( ) >r( ) >r( ) (均用实际的元素符号表示)。
(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________________ 。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是:______________________ 。
元素性质 | 元素编号 | |||||||
A | B | C | D | E | F | G | H | |
氢化物的沸点(℃) | -60.7 | -33.4 | -111.5 | 100 | -87.7 | 19.54 | -84.9 | -161.5 |
最高化合价 | +6 | +5 | +4 | +5 | +7 | +4 | ||
最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
已知:①A与D可形成化合物AD2、AD3,可用于制备强酸甲;
②B与D可形成化合物BD、BD2,可用于制备强酸乙。
请回答:
(1)表中属于第三周期元素的是
(2)写出H的最高价氧化物的电子式:
比较A、D、G三种简单阴离子的半径大小:r
(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】下图是100 mgCaC2O4·H2O受热分解时,所得固体产物的质量随温度变化的曲线。试利用图中信息结合所学的知识,回答下列各问题:

(1)温度分别为t 1 和t 2 时,固体产物的化学式A是______________,B是______________。
(2)由CaC2O4·H2O得到A的化学方程式为__________________________________。
(3)由A得到B的化学方程式为____________________________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。

(1)温度分别为t 1 和t 2 时,固体产物的化学式A是______________,B是______________。
(2)由CaC2O4·H2O得到A的化学方程式为__________________________________。
(3)由A得到B的化学方程式为____________________________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量的铝铁合金与100mL很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4 mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:

(1)结合OH-的能力最弱的是________ (填离子符号)
(2)B与A的差值为________ mol.
(3)原混合物中铝粉与铁粉的物质的量之比为______ .
(4)B点对应的沉淀量为________ mol,C点对应的溶液体积为________ mL.
(5)硝酸溶液的物质的量浓度为_________ mol·L-1
(6)写出铝与该浓度硝酸反应的离子方程式_____________________ 。

(1)结合OH-的能力最弱的是
(2)B与A的差值为
(3)原混合物中铝粉与铁粉的物质的量之比为
(4)B点对应的沉淀量为
(5)硝酸溶液的物质的量浓度为
(6)写出铝与该浓度硝酸反应的离子方程式
您最近一年使用:0次

 )随温度的变化如图所示(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物)。
)随温度的变化如图所示(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物)。
 )=
)=

