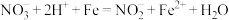黄铜矿(CuFeS2)是提取铜的主要原料,其煅烧产物Cu2S在1200℃高温下继续反应:2Cu2S + 3O2→2Cu2O + 2SO2……① 2Cu2O + Cu2S →6Cu + SO2……②。则下列说法正确的是
| A.反应②中Cu2S只发生了氧化反应 |
| B.反应①中氧化产物只有SO2 |
| C.若1molCu2S完全转化为2molCu,则转移电子数为2NA |
| D.将1molCu2S冶炼成2molCu,需要O2 1mol |
2015·上海普陀·二模 查看更多[5]
更新时间:2016-12-09 10:24:31
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
⑴4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
⑵2Na2CrO4+H2SO4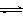 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法中正确的是
⑴4FeO·Cr2O3+8Na2CO3+7O2
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2⑵2Na2CrO4+H2SO4
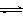 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O下列说法中正确的是
| A.反应⑴和⑵均为氧化还原反应 |
| B.反应⑴的氧化剂是O2,还原剂是FeO·Cr2O3 |
| C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4 |
| D.生成1mol的Na2Cr2O7时共转移7mol电子 |
您最近半年使用:0次
多选题
|
适中
(0.65)
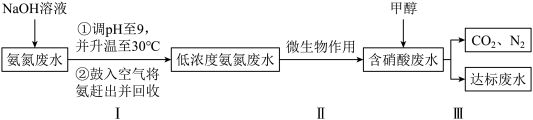
【推荐2】氨氮废水是造成河流及湖泊富营养化的主要因素,现处理某氮肥厂产生的氨氮废水(其中氮元素多以NH 和NH3·H2O的形式存在)的一种设计流程如下。下列相关叙述错误的是
和NH3·H2O的形式存在)的一种设计流程如下。下列相关叙述错误的是
 和NH3·H2O的形式存在)的一种设计流程如下。下列相关叙述错误的是
和NH3·H2O的形式存在)的一种设计流程如下。下列相关叙述错误的是
| A.过程Ⅰ、Ⅱ、Ⅲ发生的化学反应都属于氧化还原反应 |
B.过程Ⅰ中调pH至9的目的是将NH 转化为NH3·H2O 转化为NH3·H2O |
C.过程Ⅱ中NH →NO →NO ,每转化1 mol NH ,每转化1 mol NH 转移2NA个电子 转移2NA个电子 |
| D.过程Ⅲ中甲醇作还原剂,将硝酸还原为N2 |
您最近半年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】亚氯酸钠( )是一种高效的漂白剂和氧化剂,制备亚氯酸钠的流程如下。
)是一种高效的漂白剂和氧化剂,制备亚氯酸钠的流程如下。
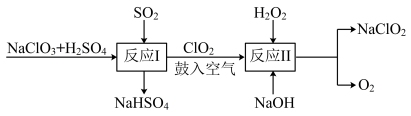
已知:纯 易分解爆炸,一般稀释到10%以下安全;“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。
易分解爆炸,一般稀释到10%以下安全;“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。
下列说法正确的是
 )是一种高效的漂白剂和氧化剂,制备亚氯酸钠的流程如下。
)是一种高效的漂白剂和氧化剂,制备亚氯酸钠的流程如下。
已知:纯
 易分解爆炸,一般稀释到10%以下安全;“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。
易分解爆炸,一般稀释到10%以下安全;“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。下列说法正确的是
A. 的“有效氯含量”约为1.27g 的“有效氯含量”约为1.27g |
B.鼓入空气的主要目的是稀释 以防爆炸 以防爆炸 |
| C.反应I中氧化产物与还原产物的物质的量之比为2:1 |
D.反应II条件下, 的氧化性大于 的氧化性大于 |
您最近半年使用:0次
【推荐2】NaClO2 是一种重要的杀菌消毒剂,工业上制备 NaClO2 的原理为 ClO2+H2O2+NaOH→NaClO2+H2O+O2(未配平)。下列说法正确的是( )
| A.该制备反应中,O2 是氧化产物 |
| B.氧化剂与还原剂的物质的量之比为 1:2 |
| C.生成标准状况下的 11.2L 气体,转移 2mol 电子 |
| D.制备过程中,混合液的 pH 降低 |
您最近半年使用:0次

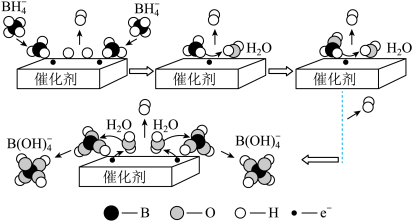
 +4H2O= B(OH)
+4H2O= B(OH)  和
和 )是废水处理的重要环节。一种利用还原铁粉和微生物进行脱硝的过程如图所示:
)是废水处理的重要环节。一种利用还原铁粉和微生物进行脱硝的过程如图所示: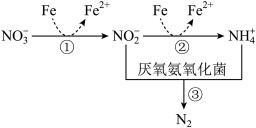
 的浓度几乎为零。下列说法正确的是
的浓度几乎为零。下列说法正确的是