29. 硝酸在有机合成、医药化工、化纤等行业应用非常广泛。工业上用氨催化氧化法可生产硝酸,其生产过程可表示为:
4NH
3+5O
2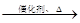
4NO+6H
2O ----①
4NO+3O
2+2H
2O→4HNO
3----②
完成下列计算:
52、如果以一定量的氨气在一密闭容器中与足量氧气发生上述反应,冷却后所得溶液中溶质的质量分数是
_________________(保留2位小数,下同)。
53、现以1.70吨液氨为原料生产硝酸,然后加入4.50吨水,得到密度为1.31g/cm
3的硝酸,该硝酸的物质的量浓度是
_______mol/L(假设生产过程中反应物和生成物均无损耗)。
54、把22.40 g铁完全溶解于某浓度的硝酸中,反应只收集到 0.30 mol NO
2 和0.20 mol NO。通过计算推断反应后溶液中溶质的成分及其物质的量
__________(写出计算过程)。
55、硝酸工业尾气中的NO、NO
2属于大气的主要污染物。已知1m
3硝酸工业的尾气中含3160mg NO
x,其中n(NO) : n(NO
2) = 9:1。
(1)如果用NaOH溶液完全吸收NO
x,至少需要补充标准状况下的富氧空气多少升?
_________________________(富氧空气中O
2的体积分数为0.25)(写出计算过程)
(2)如果用氨催化还原法,即用氨作催化剂,将NO、NO
2转化为氮气直接排入空气中,需要氨气的质量为多少克?
__________________________(写出计算过程)