对于CH3COOH、HCl、H2SO4三种溶液,下列判断正确的是
| A.pH相同的三种溶液,物质的量浓度最小的是HCl |
| B.物质的量浓度相同的三种溶液,pH最小的是H2SO4 |
| C.含溶质的物质的量相同的三种溶液与过量镁粉反应,CH3COOH产生的H2最多 |
| D.相同pH、相同体积的三种溶液用NaOH溶液完全中和时,消耗NaOH溶液一样多 |
11-12高二上·甘肃兰州·期末 查看更多[5]
浙江省金华市云富高级中学2020-2021学年高二10月月考化学试题浙江省磐安县第二中学2020-2021学年高二上学期期中考试化学试题(已下线)2010—2011学年甘肃省兰州一中高二上学期期末考试化学试卷2015-2016学年陕西省宝鸡市岐山县高二上学期期末理化学试卷2014-2015四川省雅安中学高二上学期期末模拟化学试卷
更新时间:2016-12-09 10:54:51
|
【知识点】 弱电解质的电离平衡
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是常温下用 的
的 溶液滴定
溶液滴定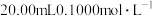 的
的 溶液所得到的滴定曲线。下列说法错误的是(忽略反应前后溶液体积的变化)
溶液所得到的滴定曲线。下列说法错误的是(忽略反应前后溶液体积的变化)
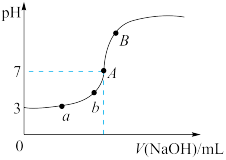
 的
的 溶液滴定
溶液滴定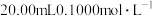 的
的 溶液所得到的滴定曲线。下列说法错误的是(忽略反应前后溶液体积的变化)
溶液所得到的滴定曲线。下列说法错误的是(忽略反应前后溶液体积的变化)
A.由图可知, 是一种弱酸,且 是一种弱酸,且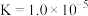 |
B.由水电离出的氢离子浓度: |
C.若 溶液为 溶液为 的 的 溶液或 溶液或 溶液,则A点时消耗 溶液,则A点时消耗 溶液的体积相同 溶液的体积相同 |
D.B点溶液中的离子浓度关系为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,浓度均为0.10 mol·L-1、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随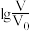 的变化如图所示。下列叙述错误的是
的变化如图所示。下列叙述错误的是

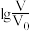 的变化如图所示。下列叙述错误的是
的变化如图所示。下列叙述错误的是
| A.HA的酸性强于HB的酸性 | B.HB溶液中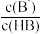 的值:b点大于a点 的值:b点大于a点 |
| C.此温度下,Ka(HB)=1×10-5 mol·L-1 | D.HA的电离程度:d点大于c点 |
您最近一年使用:0次

 :CO2+H2O
:CO2+H2O H2CO3
H2CO3 =Ag2SO4↓
=Ag2SO4↓

