下列电离或离子方程式正确的是
A.亚硫酸的电离:H2SO3 2H++ SO32- 2H++ SO32- |
B.氯化铵水解的离子方程式为: NH4+ +H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.NaHCO3水解的离子方程式为:HCO3-+H2O  CO32-+H3O+ CO32-+H3O+ |
D.向氯化铝溶液中加入过量的氨水:A13++3NH3·H2O Al(OH)3+3NH4+ Al(OH)3+3NH4+ |
更新时间:2016-12-09 10:54:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式书写正确的是( )
A.NaHS的水解:HS-+ H2O S2-+ H3O+ S2-+ H3O+ |
B.NaHCO3在水溶液中的电离:HCO3−+ H2O H2 CO3+ OH− H2 CO3+ OH− |
| C.NH4Cl的水解:NH4+ + H2O = NH3·H2O + OH− |
| D.硫酸铝溶液和碳酸氢钠溶液混合: Al3+ + 3HCO3− = Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验方案不能 达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向2mL1mol∙L-1NaHCO3溶液中滴加1mol∙L-1CH3COOH溶液,观察现象 | 比较Ka(CH3COOH)和Ka1(H2CO3)的大小 |
| B | 向NaCl固体中加入适量的酒精,充分振荡形成透明液体,用激光笔照射,观察现象 | 探究该分散系是否为胶体 |
| C | 将生锈铁片置于稀盐酸中,充分反应一段时间后,向溶液中滴加KSCN溶液,观察现象 | 生锈的铁片表面含有Fe2O3 |
| D | 取少量的Na2SO3粉末于试管中,先向其中滴加稍过量的盐酸,再向其中滴加BaCl2溶液,观察现象 | Na2SO3粉末是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用如图1所示装置,分别向25mL0.3mol/LNa2CO3溶液和25mL0.3mol/LNaHCO3溶液中逐滴滴加0.3mol/L稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示,下列说法正确的是


| A.X曲线为Na2CO3溶液的滴定曲线 |
| B.b点溶液的pH大于c点溶液的pH |
C.a点溶液中: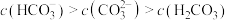 |
| D.c、d两点水的电离程度相等 |
您最近一年使用:0次
【推荐2】常温下,将0.025 mol BaSO4粉末置于盛有蒸馏水的烧杯中形成1 L悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌。加入Na2CO3固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法正确的是

| A.常温下,Ksp(BaSO4)=1.0×10-10 |
| B.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
| C.若要使BaSO4全部转化为BaCO3至少要加入0.625 mol Na2CO3 |
D.BaSO4恰好全部转化为BaCO3时,离子浓度大小关系为c(SO )>c(CO )>c(CO )>c(Ba2+)>c(OH-) )>c(Ba2+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知短周期主族元素R、W、X、Y、Z,其中R元素所在的周期数是其族序数的一半,且对应的两种常见氧化物均为酸性氧化物,W元素与Z元素在同一主族,X与其同主族另一元素单质构成原子反应堆导热剂,Y元素原子最外层电子数为m,次外层电子数为n,Z元素原子L层电子数为m+n,M层电子数为m-n,下列叙述中错误的是
| A.R、X、Y对应的简单离子半径:r(X)<r(Y)<r(R) |
| B.相同温度相同浓度的W、R的最高价含氧酸的正盐溶液的碱性:W>R |
| C.将WY2与RY2分别通入Ba(NO3)2溶液中,现象不同 |
| D.因氢化物的稳定性:Y>R,故氢化物的沸点:Y>R |
您最近一年使用:0次



