下表是不同温度下水的离子积的数据。试回答以下问题:
(1)若25<t1<t2,则a________ 1×10-14(填“>”、“<”或“=”),做此判断的理由是______________ 。
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=___________ 。
(3)在t2温度下测得某溶液pH=7,该溶液显__________ (填“酸”、“碱”或“中”)性,将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合:
①若所得混合液为中性,则a∶b=____________ ;
②若所得混合液pH=2,则a∶b=____________ 。
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
(1)若25<t1<t2,则a
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
(3)在t2温度下测得某溶液pH=7,该溶液显
①若所得混合液为中性,则a∶b=
②若所得混合液pH=2,则a∶b=
10-11高二上·江西新余·阶段练习 查看更多[6]
河北省石家庄市藁城区第一中学2019-2020学年高二上学期第二次月考化学试题陕西省西安市第一中学2019-2020学年学高二上学期期末考试化学试题(已下线)2010年江西省新余一中 宜春中学 高安中学高二上学期第三次段考化学试卷2015-2016学年陕西省宝鸡市岐山县高二上学期期末理化学试卷(已下线)2012-2013学年江西省赣州市十一县(市)高二上学期期中联考化学试卷(已下线)2012-2013学年陕西省西安市第一中学高二上学期期末考试理科化学卷
更新时间:2016-12-09 10:54:51
|
【知识点】 水的电离
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是不同温度下水的离子积的数据。试回答以下问题:
(1)若 ,则a
,则a_______  (填“>”、“<”或“=”),做此判断的理由是
(填“>”、“<”或“=”),做此判断的理由是_______ 。
(2) 时,某
时,某 溶液中
溶液中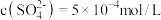 ,取该溶液
,取该溶液 加水稀释至
加水稀释至 ,则稀释后溶液中
,则稀释后溶液中
_______ 。
(3)在 温度下,测得某溶液
温度下,测得某溶液 ,①则该溶液显
,①则该溶液显_______ (填“酸”、“碱”或“中)性;
同样在 温度下
温度下 的
的 溶液
溶液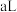 与
与 的
的 溶液
溶液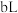 混合:
混合:
②若所得混合液为中性,则
_______ ;
③若所得混合液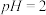 ,则
,则
_______ 。
(4)加热蒸干 溶液并灼烧所得固体,最终得到的产物是
溶液并灼烧所得固体,最终得到的产物是_______ 。
(5)常温下,已知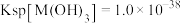 ,要使溶液中的
,要使溶液中的 降至
降至 ,则应调节溶液
,则应调节溶液
_______ 。
(6)已知:a.常温下,醋酸和 的电离平衡常数均为
的电离平衡常数均为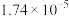 ;
;
b.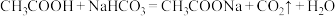 。
。
则 溶液呈
溶液呈_______ 性(填“酸”“碱”或“中”,下同), 溶液呈
溶液呈_______ 性, 溶液中物质的量浓度最大的离子是
溶液中物质的量浓度最大的离子是_______ (填化学式)。
温度/ | 25 |  |  |
| 水的离子积 |  | a |  |
 ,则a
,则a (填“>”、“<”或“=”),做此判断的理由是
(填“>”、“<”或“=”),做此判断的理由是(2)
 时,某
时,某 溶液中
溶液中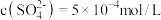 ,取该溶液
,取该溶液 加水稀释至
加水稀释至 ,则稀释后溶液中
,则稀释后溶液中
(3)在
 温度下,测得某溶液
温度下,测得某溶液 ,①则该溶液显
,①则该溶液显同样在
 温度下
温度下 的
的 溶液
溶液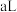 与
与 的
的 溶液
溶液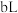 混合:
混合:②若所得混合液为中性,则

③若所得混合液
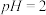 ,则
,则
(4)加热蒸干
 溶液并灼烧所得固体,最终得到的产物是
溶液并灼烧所得固体,最终得到的产物是(5)常温下,已知
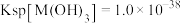 ,要使溶液中的
,要使溶液中的 降至
降至 ,则应调节溶液
,则应调节溶液
(6)已知:a.常温下,醋酸和
 的电离平衡常数均为
的电离平衡常数均为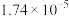 ;
;b.
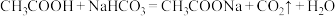 。
。则
 溶液呈
溶液呈 溶液呈
溶液呈 溶液中物质的量浓度最大的离子是
溶液中物质的量浓度最大的离子是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】⑴常温下将0.2 mol/L HCl溶液与0.2 mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+)_______ 0.2 mol/L的HCl溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=_____ mol/L;
c(H+)-c(MOH)=__________ mol/L
⑵常温下若将0.2 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下HA的电离程度______ NaA的水解程度。(填“>”、“<”、或“=”)
⑶已知:难溶电解质Cu(OH)2在常温下的Ksp = 2×10−20,则常温下:某CuSO4溶液中c(Cu2+) = 0.02 mol·L−1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为_________ 。
⑷已知:温度和浓度相等时,氨水的电离程度与醋酸相等。常温下,下列4种溶液:
①0.1mol/L CH3COONa ②0.1mol/L CH3COONH4 ③0.1mol/L CH3COOH
④0.1mol/LCH3COONa和0.1mol/LNaOH的混合溶液
按pH由大到小顺序排列___________ (填序号)
①混合溶液中由水电离出的c(H+)
②求出混合溶液中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=
c(H+)-c(MOH)=
⑵常温下若将0.2 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下HA的电离程度
⑶已知:难溶电解质Cu(OH)2在常温下的Ksp = 2×10−20,则常温下:某CuSO4溶液中c(Cu2+) = 0.02 mol·L−1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为
⑷已知:温度和浓度相等时,氨水的电离程度与醋酸相等。常温下,下列4种溶液:
①0.1mol/L CH3COONa ②0.1mol/L CH3COONH4 ③0.1mol/L CH3COOH
④0.1mol/LCH3COONa和0.1mol/LNaOH的混合溶液
按pH由大到小顺序排列
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)联氨(又称肼,N2H4,无色液体)为二元弱碱,在水中的电离方式与氨相似。写出在水中联氨第一步电离反应的方程式_______________ 。氯化镁溶液在某条件下可生Mg(OH)Cl沉淀,请写出相关离子方程式_________
(2)实验室可通过向盛装有碱石灰的锥形瓶中滴加浓氨水来制取氨气,请利用相关化学反应原理来解释______________________________
(3)室温下向10mL0.1 mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示

则HA为_______ 电解质(填“强”或“弱”),a点所示溶液c(Na)_____ c(A)(填“>”、“<”或“”=),a、b两点所示溶液中水的电离程度a_______ b(填“>”、“<”或“"=)。
(4)25℃时0.05mol/L的醋酸溶液,pH=______ 该溶液中水电离出的c(H+)=____ (已知室温下醋酸电离平衡常数为2.0×10-5)
(5)常温下,0.01mol/L的HCN溶液加水稀释1000倍的过程中,下列选项增大的是_____
A.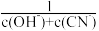 B.Kac(HCN) C.
B.Kac(HCN) C. D.
D.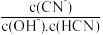
(2)实验室可通过向盛装有碱石灰的锥形瓶中滴加浓氨水来制取氨气,请利用相关化学反应原理来解释
(3)室温下向10mL0.1 mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示

则HA为
(4)25℃时0.05mol/L的醋酸溶液,pH=
(5)常温下,0.01mol/L的HCN溶液加水稀释1000倍的过程中,下列选项增大的是
A.
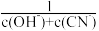 B.Kac(HCN) C.
B.Kac(HCN) C. D.
D.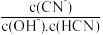
您最近一年使用:0次



