现有下列4种物质:①NH3②NaHCO3③浓H2SO4④Al(OH)3,有强氧化性的是_____ (填序号,下同);遇氯化氢气体产生白烟的是_____ ;焰色反应呈黄色的是_____ ;能与强酸和强碱反应且均不产生气体的是_____ .
更新时间:2016-03-14 17:40:34
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:
(1)氮气的电子式_______ 。
(2) 与焦炭制备粗硅的化学方程式
与焦炭制备粗硅的化学方程式_______ 。
(3)Cu和浓硫酸反应的化学方程式_______ 。
(4)硝酸放在棕色试剂瓶的原因(用化学方程式解释)_______ 。
(5)蘸有浓盐酸和浓氨水的玻璃棒相互靠近时产生白烟的化学方程式_______ 。
(1)氮气的电子式
(2)
 与焦炭制备粗硅的化学方程式
与焦炭制备粗硅的化学方程式(3)Cu和浓硫酸反应的化学方程式
(4)硝酸放在棕色试剂瓶的原因(用化学方程式解释)
(5)蘸有浓盐酸和浓氨水的玻璃棒相互靠近时产生白烟的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氨气电子式:_______ ,其分子空间构型是_______ ,氨气溶于水,溶液呈____ 性,原因是______ (用化学方程式解释)。用玻璃棒蘸浓盐酸接触氨气时,观察到的现象为_____ ,发生的反应是(用化学方程式表示)________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知A、B、C、D、E、F、G是七种原子序数依次增大的短周期元素,它们的原子结构特征或有关物质的性质等如下表所示。
元素B能与氢元素形成化合物BH3,在通常状况下,BH3的水溶液呈_______ (填“酸”、“碱”或“中”)性,原因为_______ (用方程式表示)。B和G的气态氢化物相互反应的化学方程式为_______ 。
| 元素 | 原子结构特征或有关物质的性质 |
| A | 原子的最外层电子数是其内层电子数的2倍 |
| B | 其单质是空气中含量最多的物质 |
| C | 原子的最外层电子数是其电子层数的4倍 |
| D | 位于第ⅡA族,其原子半径比E的大 |
| E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
| F | 原子序数16,其单质在通常状况下为固体 |
| G | 原子的最外层电子数比其次外层电子数少1个 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下图是自然界中不同价态硫元素之间的转化关系图。回答下列问题:

(1)硫元素在自然界中的存在形态有___________ 和化合态,单质硫矿主要存在于___________ ; 硫单质有多种,正交硫和单斜硫,它们均为硫元素的___________ 。
(2)H2SO4 的电离方程式为___________ 。
(3)硫酸是重要的化工原料,接触法制硫酸主要分三步:
①煅烧黄铁矿(FeS2);_____FeS2 + _____O2 _____Fe2O3 + _____SO2
_____Fe2O3 + _____SO2 ___________ ;
②SO2 的接触氧化;___________ ;
③98.3% H2SO4 吸收:SO3 + H2O=H2SO4。
(4)Fe2O3 可用于焊接钢轨,写出反应的化学方程式___________ 。
(5)写出铜与浓硫酸反应的的化学方程式为___________ ,若反应产生672mL(标准状况)还原性气体,转移电子的数目为___________ 。

(1)硫元素在自然界中的存在形态有
(2)H2SO4 的电离方程式为
(3)硫酸是重要的化工原料,接触法制硫酸主要分三步:
①煅烧黄铁矿(FeS2);_____FeS2 + _____O2
 _____Fe2O3 + _____SO2
_____Fe2O3 + _____SO2 ②SO2 的接触氧化;
③98.3% H2SO4 吸收:SO3 + H2O=H2SO4。
(4)Fe2O3 可用于焊接钢轨,写出反应的化学方程式
(5)写出铜与浓硫酸反应的的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】硫酸是当今世界上最重要的化工产品之一、
(1)早在1000多年前,我国就已采用加热CuSO4·5H2O或FeSO4·7H2O的方法来制取硫酸。CuSO4·5H2O的俗称是_______ 。
(2)目前工业制备硫酸主要采用接触法,以黄铁矿(FeS2)为原料制备硫酸的主要设备和流程如图。

①设备甲的名称是_______ ,原料黄铁矿(FeS2)中S的化合价是_______ 。
②接触室中反应的化学方程式是_______ 。
③吸收塔中用于吸收SO3的试剂X是_______ 。
(3)尾气中的SO2可用氨水吸收,反应的化学方程式为_______ 。
(4)钢材进行电镀之前,可用浓硫酸洗净其表面的铁锈,相比于稀硫酸和盐酸,浓硫酸的优点是_ 。
(1)早在1000多年前,我国就已采用加热CuSO4·5H2O或FeSO4·7H2O的方法来制取硫酸。CuSO4·5H2O的俗称是
(2)目前工业制备硫酸主要采用接触法,以黄铁矿(FeS2)为原料制备硫酸的主要设备和流程如图。

①设备甲的名称是
②接触室中反应的化学方程式是
③吸收塔中用于吸收SO3的试剂X是
(3)尾气中的SO2可用氨水吸收,反应的化学方程式为
(4)钢材进行电镀之前,可用浓硫酸洗净其表面的铁锈,相比于稀硫酸和盐酸,浓硫酸的优点是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
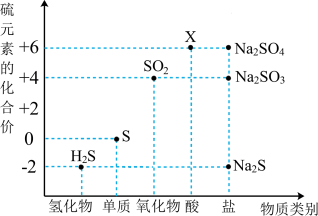
【推荐3】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:_______ ,反应体现出X具有_______ 性。
(2)从硫元素化合价变化的角度分析,图中只有还原性的物质有_______ (填化学式)。
(3)将H2S与SO2混合可生成淡黄色沉淀,该反应方程式为_______ ,该现象说明SO2具有_______ 性(选填“氧化性”、“还原性”、“漂白性”)
(2)从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将H2S与SO2混合可生成淡黄色沉淀,该反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】因在航空、核能、电池等高技术领域的重要作用——锂被称为“21世纪的能源金属”。
(1)氢化锂(LiH)中阴离子半径大于阳离子半径,其原因是___________ 。
(2)下列关于碱金属元素及其单质的叙述中,正确的是___________ (填字母)。
(3)宁德时代推出的钠离子电池,比磷酸亚铁锂电池成本更低,请画出钠离子(Na+)结构示意图___________ 。
(4)磷酸亚铁锂(LiFePO4)是新型锂离子电池的电极材料,P位于元素周期表的___________ 周期,第___________ 族,LiFePO4含有锂、铁两种金属元素,它们焰色试验的颜色分别是___________ (填序号)。
A.紫红色、无焰色现象 B.黄色、无焰色现象
C.黄色、紫色 D.洋红色、黄绿色
(1)氢化锂(LiH)中阴离子半径大于阳离子半径,其原因是
(2)下列关于碱金属元素及其单质的叙述中,正确的是___________ (填字母)。
| A.金属钠着火,要用泡沫灭火剂扑灭 |
| B.水溶液中阳离子氧化性:Li+>Na+>K+>Rb+ |
| C.单质熔点:Li<Na<K<Rb |
| D.与水反应的能力:Na<K |
(4)磷酸亚铁锂(LiFePO4)是新型锂离子电池的电极材料,P位于元素周期表的
A.紫红色、无焰色现象 B.黄色、无焰色现象
C.黄色、紫色 D.洋红色、黄绿色
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表列出了A~R9种元素在周期表中的位置:
请回答下列问题。
(1)这些元素分别为:A___________ ,B___________ ,C___________ ,D___________ ,E___________ ,F___________ ,G___________ ,R___________ ,其中化学性质最不活泼的是___________ (用元素符号表示)。
(2)画出G的原子结构示意图___________ 。
(3)元素周期表共有___________ 个周期___________ 个族,18纵行元素化合价通常表现为___________ 价所以称为0族元素,又叫惰性气体元素。A位于___________ 周期___________ 族
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(1)这些元素分别为:A
(2)画出G的原子结构示意图
(3)元素周期表共有
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】抗酸药物的种类很多,其有效成分一般是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氧氧化镁等化学物质。
(1)抗酸药物具有抗酸作用的原因是_______________________________________ 。
(2)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉。写出该抗酸药发挥功效时的化学方程式:___________________________ 、____________________________ 。
(3)淀粉在抗酸药中作填充剂、黏合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化产物为____________ (写分子式)。
(1)抗酸药物具有抗酸作用的原因是
(2)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉。写出该抗酸药发挥功效时的化学方程式:
(3)淀粉在抗酸药中作填充剂、黏合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化产物为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】人类生活离不开化学,如:①硫酸亚铁片用于治疗贫血(图是其说明书);②复方氢氧化铝用于治疗胃酸过多;③明矾用作净水剂等。

阅读“硫酸亚铁片”的标签说明,请回答:
(1)硫酸亚铁易被氧化而变质,为检验某补血剂中硫酸亚铁是否变质,可向该补血剂配成的溶液中加入
(2)氢氧化铝是典型的两性物质,它的电离方程式为_______ ;复方氢氧化铝在治疗胃酸过多时,氢氧化铝作为_______ (填“酸”或“碱”)中和过多胃酸;当然氢氧化铝也能与烧碱反应,反应的化学方程式_______ 。
(3)明矾能净水是因为①Al3+能水解,②水解产物氢氧化铝胶体具有_______ 能力。

阅读“硫酸亚铁片”的标签说明,请回答:
(1)硫酸亚铁易被氧化而变质,为检验某补血剂中硫酸亚铁是否变质,可向该补血剂配成的溶液中加入
| A.AgNO3溶液 | B.KSCN溶液 |
| C.盐酸酸化的BaCl2溶液 | D.HNO3酸化的Ba(NO3)2溶液 |
(3)明矾能净水是因为①Al3+能水解,②水解产物氢氧化铝胶体具有
您最近一年使用:0次



