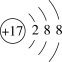
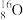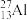元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑧七种元素在周期表中的位置。
请回答:
(1)画出③的原子结构示意图_______________
(2)在①、②、③三种元素的最高价氧化物对应水化物中,碱性最强的是_______
(填碱的化学式)。
(3)⑦、⑧两元素对应形成的氢化物中,最稳定的是_____________ (填氢化物化学式)。
(4)写出⑤和⑥形成的三原子化合物的化学式____________________
(5)写出①、④元素的最高价氧化物对应水化物之间反应生成的盐的化学式为:______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑧ | |||||
| 3 | ① | ③ | ④ | ⑦ | ||||
| 4 | ② |
请回答:
(1)画出③的原子结构示意图
(2)在①、②、③三种元素的最高价氧化物对应水化物中,碱性最强的是
(填碱的化学式)。
(3)⑦、⑧两元素对应形成的氢化物中,最稳定的是
(4)写出⑤和⑥形成的三原子化合物的化学式
(5)写出①、④元素的最高价氧化物对应水化物之间反应生成的盐的化学式为:
9-10高二下·湖南长沙·阶段练习 查看更多[2]
更新时间:2010/05/11 10:46:21
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】原子结构示意图为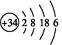 的原子,在周期表中的位置是
的原子,在周期表中的位置是___ ,根据其在周期表中的位置推测,该元素的最高正价是__ ,其最高价氧化物对应水化物的化学式为____ (该元素用X代替),其酸性比硫酸_____ 。
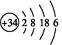 的原子,在周期表中的位置是
的原子,在周期表中的位置是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】某研究小组对下列元素周期表(部分)进行研究,回答下列问题。
(1)钙元素位于周期表第___________ 期___________ 族。
(2)组成化合物最多的元素是___________ 。地壳中含量最多的金属元素是___________ 。
(3)原子半径最小的元素是___________ 。非金属性最强的元素是___________ 。
(4)锂、硫、硅三种单质中,适合作半导体材料的是___________ 。
(5)钠、镁、铝三种单质中,与冷水反应最剧烈的是___________ 。
(6) 和
和 中,酸性较强的是
中,酸性较强的是___________ 。
(7) 和
和 中,热稳定性较强的是
中,热稳定性较强的是___________ 。
(8)KOH和 中,碱性较弱的是
中,碱性较弱的是___________ 。
(9)原子核外电子排布中,最外层电子数是内层电子数3倍的元素是___________ 。
(10)能证明Cl元素比S元素非金属性更强的化学反应,其化学方程式为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | H | ||||||
| 2 | Li | C | N | O | F | ||
| 3 | Na | Mg | Al | Si | S | Cl | |
| 4 | K | Ca |
(2)组成化合物最多的元素是
(3)原子半径最小的元素是
(4)锂、硫、硅三种单质中,适合作半导体材料的是
(5)钠、镁、铝三种单质中,与冷水反应最剧烈的是
(6)
 和
和 中,酸性较强的是
中,酸性较强的是(7)
 和
和 中,热稳定性较强的是
中,热稳定性较强的是(8)KOH和
 中,碱性较弱的是
中,碱性较弱的是(9)原子核外电子排布中,最外层电子数是内层电子数3倍的元素是
(10)能证明Cl元素比S元素非金属性更强的化学反应,其化学方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
真题
【推荐3】V、W、X、Y、Z是由周期表中1~20号部分元素组成的5种化合物,其中V、W、X、Z均为两种元素组成,上述5种化合物涉及的所有元素的原子序数之和等于35。它们之间的反应关系如下图:

(1)5种化合物分别是V____ 、W____ 、X____ 、Y____ 、Z____ :(填化学式)
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是___________ :
(3)V的电子式是___________ 。

(1)5种化合物分别是V
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是
(3)V的电子式是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】已知某主族元素的原子结构示意图如下,请写出它们在周期表中的位置。
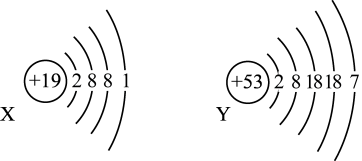
X:_______ ,Y:_______ 。

X:
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】下表为元素周期表的一部分,请回答下列有关问题:
(1)元素②的一种核素可测定文物年代,这种核素的符号为___________ ,已知元素⑩的一种核素,其中子数为45,这种核素的符号为___________ 。
(2)由元素①和④可形成18电子的化合物,该化合物的化学式为___________ 。
(3)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是___________ (用化学式回答),写出该水化物与⑥的最高价氧化物的水化物反应的离子方程式___________ 。
(4)将⑤、⑥、⑨单质各1mol分别投入到足量的同浓度的盐酸中,预测实验结果:___________ 与盐酸反应最剧烈,___________ 与盐酸反应的速度最慢;___________ 与盐酸反应产生的气体最多。(用元素符号回答)
(5)元素的非金属性⑧___________ ⑩(填“>”或“<”);下列事实不能证明上述结论的是___________ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(1)元素②的一种核素可测定文物年代,这种核素的符号为
(2)由元素①和④可形成18电子的化合物,该化合物的化学式为
(3)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是
(4)将⑤、⑥、⑨单质各1mol分别投入到足量的同浓度的盐酸中,预测实验结果:
(5)元素的非金属性⑧
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
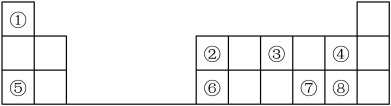
【推荐1】下表是元素周期表的一部分,①~⑧代表对应的元素,回答下列问题:___________ 。
(2)⑦在元素周期表中的位置是___________ ;⑧的原子结构示意图为___________ 。
(3)②③⑧的最高价氧化物对应水化物酸性由强到弱为___________ (填化学式),③的单质的结构式为___________ 。
(4)④⑤⑧的简单离子半径大小顺序是___________ (填离子),④的单质和 发生置换反应的化学方程式为
发生置换反应的化学方程式为___________ 。
(5)写出⑥的单质与⑤最高价氧化物水化物反应的离子方程式:___________ 。
(6)下列方法能比较⑤和⑥的金属性强弱的是___________(填标号)。
(2)⑦在元素周期表中的位置是
(3)②③⑧的最高价氧化物对应水化物酸性由强到弱为
(4)④⑤⑧的简单离子半径大小顺序是
 发生置换反应的化学方程式为
发生置换反应的化学方程式为(5)写出⑥的单质与⑤最高价氧化物水化物反应的离子方程式:
(6)下列方法能比较⑤和⑥的金属性强弱的是___________(填标号)。
| A.相同条件下,比较⑤、⑥的单质与水反应的剧烈程度 |
| B.比较⑤、⑥最高价氧化物水化物的碱性强弱 |
| C.比较⑤、⑥简单离子所带电荷的多少 |
| D.将⑤的单质投入⑥的盐溶液中,观察实验现象 |
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。河南焦作的山药富含硒( ),有抗癌、抗衰老等重要功能。请回答下列问题。
),有抗癌、抗衰老等重要功能。请回答下列问题。
(1) 的原子结构示意图为
的原子结构示意图为___ 。
(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。下列说法正确的是_____(填标号)。
(3)某混合物中硒主要以 和
和 的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
ⅰ.将该混合物与浓硫酸混合焙烧,产生 、
、 的烟气
的烟气
ⅱ.用水吸收ⅰ中烟气,可得 固体
固体
已知: 的熔点为315℃,沸点为684.9℃。
的熔点为315℃,沸点为684.9℃。
可用足量 溶液吸收烟气中的
溶液吸收烟气中的 ,二者反应生成一种盐,该盐的化学式为
,二者反应生成一种盐,该盐的化学式为____ 。
 ),有抗癌、抗衰老等重要功能。请回答下列问题。
),有抗癌、抗衰老等重要功能。请回答下列问题。(1)
 的原子结构示意图为
的原子结构示意图为(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。下列说法正确的是_____(填标号)。
A.还原性: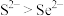 | B.浓硒酸可能具有强氧化性、吸水性 |
C.稳定性: | D.氧化性: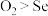 |
 和
和 的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:ⅰ.将该混合物与浓硫酸混合焙烧,产生
 、
、 的烟气
的烟气ⅱ.用水吸收ⅰ中烟气,可得
 固体
固体已知:
 的熔点为315℃,沸点为684.9℃。
的熔点为315℃,沸点为684.9℃。可用足量
 溶液吸收烟气中的
溶液吸收烟气中的 ,二者反应生成一种盐,该盐的化学式为
,二者反应生成一种盐,该盐的化学式为
您最近一年使用:0次

 ②
②