电解原理和原电池原理是电化学的两个重要内容。某兴趣小组做如下探究实验:
Ⅰ.(1)如左下图1为某实验小组依据氧化还原反应设计的原电池装置,该反应的离子方程式为___________ 。反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________ mol电子。
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式__________ ,这是由于NH4Cl溶液显________ (填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的原因____________________ 。
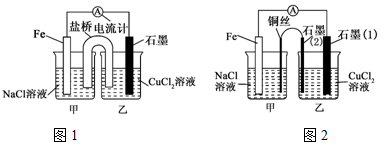
(3)如上图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则乙装置中石墨(1)为________ 极(填正、负、阴、阳),乙装置中与铜线相连的石墨(2)电极上发生的反应式为___________________ 。
(4)在图2乙装置中改为加入400 mL CuSO4溶液,一段时间后,若电极质量增重 1.28 g,则此时溶液的pH为_________
Ⅰ.(1)如左下图1为某实验小组依据氧化还原反应设计的原电池装置,该反应的离子方程式为
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式

(3)如上图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则乙装置中石墨(1)为
(4)在图2乙装置中改为加入400 mL CuSO4溶液,一段时间后,若电极质量增重 1.28 g,则此时溶液的pH为
15-16高二上·山东菏泽·期末 查看更多[3]
2015-2016学年山东省菏泽市高二上学期期末考试化学试卷(已下线)第20讲 原电池 化学电源(精练)-2021年高考化学一轮复习讲练测(已下线)第16讲 原电池 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)
更新时间:2016-12-09 14:43:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】图1为铁在一定条件下的转化关系图。

请回答:
(1)“曾青得铁则化为铜”的反应有:Fe + CuSO4 = FeSO4 + Cu,该反应的还原剂是_____________ (填化学式);
(2)工业上,向500-600℃的铁屑中通入Cl2生产FeCl3,向FeCl3溶液中滴加KSCN溶液,观察到的现象是溶液变成____________ 色;
(3)图2为原电池装置示意图,此装置可以把化学能转化为_________ 能,其中铁作_____ 极;

(4)Fe3O4中Fe既有+2价又有+3价,则+2价和+3价Fe的个数比为__________ 。

请回答:
(1)“曾青得铁则化为铜”的反应有:Fe + CuSO4 = FeSO4 + Cu,该反应的还原剂是
(2)工业上,向500-600℃的铁屑中通入Cl2生产FeCl3,向FeCl3溶液中滴加KSCN溶液,观察到的现象是溶液变成
(3)图2为原电池装置示意图,此装置可以把化学能转化为

(4)Fe3O4中Fe既有+2价又有+3价,则+2价和+3价Fe的个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次正式踏上飞向浩渺星辰的征途。
(1)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的___________ 极, 向
向___________ (填“正”或“负”)极作定向移动,Y极的电极反应式为___________ 。
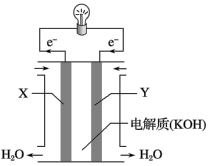
(2)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲制得常温下180g水,则电池内电子转移的物质的量约为___________ mol
(3)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
①飞船在光照区运行时,太阳能电池帆板将___________ 转化为___________ ,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为: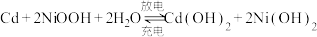 ,充电时,阳极的电极反应式为
,充电时,阳极的电极反应式为___________ ;
②当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性___________ (填“增大”“减小”或“不变”)。
(1)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的
 向
向
(2)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲制得常温下180g水,则电池内电子转移的物质的量约为
(3)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
①飞船在光照区运行时,太阳能电池帆板将
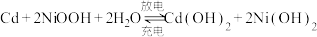 ,充电时,阳极的电极反应式为
,充电时,阳极的电极反应式为②当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.填空。
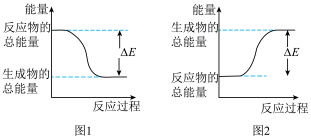
(1)下列反应中,能量变化符合图1的有___________ (填序号,下同),符合图2的有___________ 。
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤碳与二氧化碳高温反应
II.如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。已知: 的溶解度随温度升高而降低。试回答下列问题:
的溶解度随温度升高而降低。试回答下列问题:
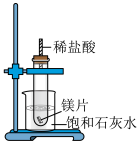
(2)实验中观察到的现象是___________ 。
(3)若将镁和稀盐酸的反应设计成原电池,用稀盐酸作电解质溶液,铜为原电池的某一电极材料,则铜为原电池的___________ (填“正”或“负”,下同)极。电解质溶液中 向
向___________ 极移动。
(4)将铁棒和锌片连接后浸入 溶液里,当电池中有0.2mol电子通过时,正极电极反应式:
溶液里,当电池中有0.2mol电子通过时,正极电极反应式:___________ ,负极质量的变化是减少___________ g。
(1)下列反应中,能量变化符合图1的有
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤碳与二氧化碳高温反应

II.如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。已知:
 的溶解度随温度升高而降低。试回答下列问题:
的溶解度随温度升高而降低。试回答下列问题:
(2)实验中观察到的现象是
(3)若将镁和稀盐酸的反应设计成原电池,用稀盐酸作电解质溶液,铜为原电池的某一电极材料,则铜为原电池的
 向
向(4)将铁棒和锌片连接后浸入
 溶液里,当电池中有0.2mol电子通过时,正极电极反应式:
溶液里,当电池中有0.2mol电子通过时,正极电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
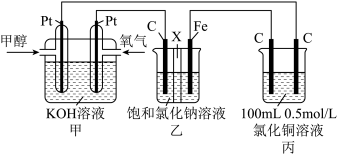
【推荐1】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。
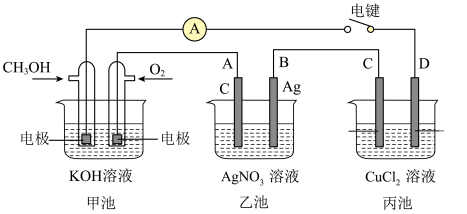
请回答下列问题:
(1)甲池中,通入CH3OH电极的电极反应式为___________ 。
(2)设乙池的体积为200mL,反应一段时间后,乙池中A、B两极都产生22.4mL(已换算成标准状况)的气体时,乙池中pH约为___________ ,反应开始前乙池中的AgNO3的浓度为___________ ,甲池中理论上消耗O2的体积为___________ mL(标准状况)。
(3)若要电解精炼铜,丙池中,粗铜应为___________ (填C或D)电极。
(4)若丙池中C、D两电极都为惰性电极,将其溶液换成NaCl溶液,总电池反应方程式为___________ ,为了获得氢气和氯气,该装置中需使用___________ (填阳离子、阴离子或质子)交换膜。

请回答下列问题:
(1)甲池中,通入CH3OH电极的电极反应式为
(2)设乙池的体积为200mL,反应一段时间后,乙池中A、B两极都产生22.4mL(已换算成标准状况)的气体时,乙池中pH约为
(3)若要电解精炼铜,丙池中,粗铜应为
(4)若丙池中C、D两电极都为惰性电极,将其溶液换成NaCl溶液,总电池反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐2】请回答氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______ (要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________ (填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
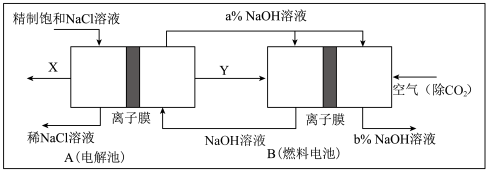
①图中X、Y分别是_____ 、_______ (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________ ;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______ ;负极:_____ ;
③这样设计的主要节(电)能之处在于(写出2处)____________ 、____________ 。
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X、Y分别是
②分别写出燃料电池B中正极、负极上发生的电极反应正极:
③这样设计的主要节(电)能之处在于(写出2处)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.回答下列问题
(1)写出铅酸蓄电池放电时负极电极反应:___________
Ⅱ.如图所示的装置中,若通入直流电5min时,铜电极质量增加21.6g,试回答:
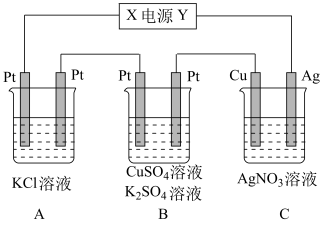
(2)电源为碱性氢氧燃料电池,则电源电极X的电极反应式为___________
(3)若A中KCl足量且溶液的体积也是200mL,电解后,溶液的OH-的物质的量浓度为___________ mol/L(假设电解前后溶液的体积无变化);
(4)通电5min后,B中共收集2240mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为___________ (设电解前后溶液体积无变化),若要使 装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是
装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是___________ 。
A.0.05molCuO B.0.05molCuO和0.025molH2O
C.0.05molCu(OH)2 D.0.05molCuCO3和0.05molH2O
(1)写出铅酸蓄电池放电时负极电极反应:
Ⅱ.如图所示的装置中,若通入直流电5min时,铜电极质量增加21.6g,试回答:

(2)电源为碱性氢氧燃料电池,则电源电极X的电极反应式为
(3)若A中KCl足量且溶液的体积也是200mL,电解后,溶液的OH-的物质的量浓度为
(4)通电5min后,B中共收集2240mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为
 装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是
装置溶液要恢复到电解前的状态,需要加入的物质以及相应的物质的量正确的是A.0.05molCuO B.0.05molCuO和0.025molH2O
C.0.05molCu(OH)2 D.0.05molCuCO3和0.05molH2O
您最近一年使用:0次
【推荐2】按要求填空:
(1)某元素的最外层电子排布式是4s24p5,则其元素符号为___________ 。
(2)写出以惰性电极为材料电解饱和MgCl2溶液的离子方程式___________ 。
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出H3BO3在水中的电离方程式:___________ 。
(4)50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液充分反应,测得此过程放出akJ的热量,写出该过程表示中和热(数值要求化简)的热化学方程式:___________ 。
(5)将AlCl3溶液蒸干并灼烧得不到无水AlCl3,但将SOCl2(亚硫酰氯)与AlCl3·6H2O混合并加热,可获得无水AlCl3,试写出此混合加热过程的化学方程式___________ 。
(1)某元素的最外层电子排布式是4s24p5,则其元素符号为
(2)写出以惰性电极为材料电解饱和MgCl2溶液的离子方程式
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出H3BO3在水中的电离方程式:
(4)50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液充分反应,测得此过程放出akJ的热量,写出该过程表示中和热(数值要求化简)的热化学方程式:
(5)将AlCl3溶液蒸干并灼烧得不到无水AlCl3,但将SOCl2(亚硫酰氯)与AlCl3·6H2O混合并加热,可获得无水AlCl3,试写出此混合加热过程的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是___________ 。
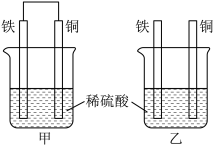
A.甲、乙均为化学能转变为电能的装置
B.甲、乙中铜片上均没有明显现象
C.甲、乙中铁片质量均减少
D.甲、乙两烧杯中 均减小
均减小
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”、“<”或“=”、“无法判断”)。
③请写出甲、乙中构成原电池的正极电极反应式:___________ 。电池工作时,溶液中 向
向___________ 极(填“铜极”或“铁极”)移动。当构成原电池的溶液质量增重27g时,电极上转移电子数目为___________ 。
④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为___________ 。
(2)燃料电池是目前电池研究的热点之一,某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①正极是___________ (填“a”或“b”),a极发生的电极反应式是___________ 。
②将上图 改成甲烷,电解质溶液改成
改成甲烷,电解质溶液改成 溶液。通甲烷电极反应式为
溶液。通甲烷电极反应式为___________ 。
(3)用燃料电池做电源,用惰性电极电解饱和食盐水,电解总反应方程式为___________ 。
(1)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是

A.甲、乙均为化学能转变为电能的装置
B.甲、乙中铜片上均没有明显现象
C.甲、乙中铁片质量均减少
D.甲、乙两烧杯中
 均减小
均减小②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出甲、乙中构成原电池的正极电极反应式:
 向
向④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为
(2)燃料电池是目前电池研究的热点之一,某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①正极是
②将上图
 改成甲烷,电解质溶液改成
改成甲烷,电解质溶液改成 溶液。通甲烷电极反应式为
溶液。通甲烷电极反应式为(3)用燃料电池做电源,用惰性电极电解饱和食盐水,电解总反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】应用电化学原理,回答下列问题:
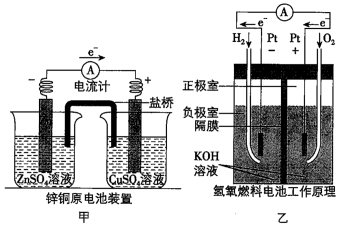
(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是:K+移向_______ ,Cl-移向_______ 。一段时间后,当电路中通过电子为0.5mol时,锌电极质量_______ (填“增加”或“减少”,下同),铜电极质量_______ 了_______ g。
(2)乙中正极反应式为_______ ;若将H2换成CH4,则负极反应式为_______ 。
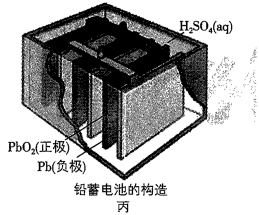
(3)丙中铅蓄电池放电时正极的电极反应式为:_______ ,放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池 _______ 极相连接。


(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是:K+移向
(2)乙中正极反应式为
(3)丙中铅蓄电池放电时正极的电极反应式为:
您最近一年使用:0次
【推荐2】氨氮的生成与消除都具有重要意义。
(1)电催化氮气还原合成氨是一种常温常压条件下利用水作为氢源的低碳环保路线,电催化合成氨装置如图:

①a接电源的_______ 极。
②该装置总反应化学方程式为_______ 。
(2)微生物燃料电池(MFC)是一种现代化氨氮去除技术,MFC碳氮联合同时去除的氮转化系统原理如图。

①A极的电极反应式为_______ 。
② 通过质子交换膜向
通过质子交换膜向_______ (填“A”或“B”)电极区溶液移动。
③在好氧微生物反应器中,转化
 ,转移的电子数目为
,转移的电子数目为_______ 。
(1)电催化氮气还原合成氨是一种常温常压条件下利用水作为氢源的低碳环保路线,电催化合成氨装置如图:

①a接电源的
②该装置总反应化学方程式为
(2)微生物燃料电池(MFC)是一种现代化氨氮去除技术,MFC碳氮联合同时去除的氮转化系统原理如图。

①A极的电极反应式为
②
 通过质子交换膜向
通过质子交换膜向③在好氧微生物反应器中,转化

 ,转移的电子数目为
,转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)氢气是一种热值高、环境友好型燃料。等物质的量的氢气完全燃烧生成液态水与生成气态水相比,生成液态水时放出热量_______ (填“多”“少”或“相等”)。
(2)拆开1mol共价键所吸收的能量或形成1mol共价键所释放的能量称为键能。已知H-H键能为436kJ/mol,H─N键能为391 kJ/mol,N≡N键能为946 kJ/mol。根据键能计算工业合成氨时消耗1molN2能_______ (填“吸收”或“放出”)_______ kJ热量。

(3)若电极a为Zn、电极b为Cu、电解质溶液为稀硫酸,该装置工作时,Cu电极上的可以看到的现象_______ ,SO 向
向_______ 极(填a或b)移动,正极的电极反应式为_______ 。
(4)若电极a为Fe、电极b为Ag、电解质溶液为硝酸银,该原电池工作时,原电池的负极材料为_______ ,电子沿导线向_______ (填a/b)移动。
(5)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,并在下面方框内画出原电池实验装置图,注明电极材料和电解质溶液等_______ 。当线路中转移0.4mol电子时,则被腐蚀铜的质量为_______ g。

(1)氢气是一种热值高、环境友好型燃料。等物质的量的氢气完全燃烧生成液态水与生成气态水相比,生成液态水时放出热量
(2)拆开1mol共价键所吸收的能量或形成1mol共价键所释放的能量称为键能。已知H-H键能为436kJ/mol,H─N键能为391 kJ/mol,N≡N键能为946 kJ/mol。根据键能计算工业合成氨时消耗1molN2能

(3)若电极a为Zn、电极b为Cu、电解质溶液为稀硫酸,该装置工作时,Cu电极上的可以看到的现象
 向
向(4)若电极a为Fe、电极b为Ag、电解质溶液为硝酸银,该原电池工作时,原电池的负极材料为
(5)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,并在下面方框内画出原电池实验装置图,注明电极材料和电解质溶液等

您最近一年使用:0次