已知25℃、101kpa时,一些物质的燃烧热为:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:_____________ 。
(2)根据盖斯定律完成下列热化学方程式CO(g)+ 2H2(g)= CH3OH(l) △H=__________ 。
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/(kJ/mol) | -283.0 | -285.8 | -726.5 |
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:
(2)根据盖斯定律完成下列热化学方程式CO(g)+ 2H2(g)= CH3OH(l) △H=
9-10高二下·福建·期末 查看更多[1]
(已下线)2010年福建省季延中学高二下学期期末考试化学试题
更新时间:2010-08-31 16:57:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求书写方程式:
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为______ 。
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为______ 。
(3)燃烧1.3g乙炔( )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为______ 。已知: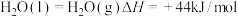 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是______ kJ。
(4)2.3g的 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为______ 。
(5) 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为______ 。
(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为______ 。
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色______ 。
(8)检验 的方法,其离子方程式为
的方法,其离子方程式为______ 。
(9)工业制漂白粉,其化学方程式为______ 。
(10)氨水与稀硫酸反应生成1mol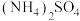 放热24.2kJ;已知
放热24.2kJ;已知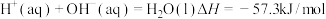 ,
, 电离的热化学方程式为
电离的热化学方程式为______ 。
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为
(3)燃烧1.3g乙炔(
 )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为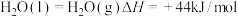 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是(4)2.3g的
 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为(5)
 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色
(8)检验
 的方法,其离子方程式为
的方法,其离子方程式为(9)工业制漂白粉,其化学方程式为
(10)氨水与稀硫酸反应生成1mol
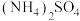 放热24.2kJ;已知
放热24.2kJ;已知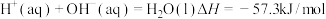 ,
, 电离的热化学方程式为
电离的热化学方程式为
您最近一年使用:0次
【推荐2】煤的气化过程中发生反应:CO(g)+H2O(g) CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:
CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:
(1)该反应的热化学方程式可写为___ 。
(2)两种反应物的转化率之和为___ 。
(3)该条件下此反应的平衡常数为___ 。
(4)若要在相同的温度下和相同的容器中,按下列物料配比充入,建立平衡后CO的体积百分含量与题干平衡相同,下列选项中可行的是___ 。
 CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:
CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:(1)该反应的热化学方程式可写为
(2)两种反应物的转化率之和为
(3)该条件下此反应的平衡常数为
(4)若要在相同的温度下和相同的容器中,按下列物料配比充入,建立平衡后CO的体积百分含量与题干平衡相同,下列选项中可行的是
| 物质 选项 | n(CO) | n(H2O) | n(CO2) | n(H2) |
| A | 0mol | 4mol | 2mol | 2mol |
| B | 0.5mol | 2.5mol | 0.5mol | 0.5mol |
| C | 1mol | 4mol | 0.5mol | 0.5mol |
| D | 0mol | 0mol | 1mol | 3mol |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】从化石燃料中能获得许多重要的有机化工原料,请回答下列问题。
(1)在一定条件下, 甲烷气体充分燃烧生成二氧化碳气体和液态水放出
甲烷气体充分燃烧生成二氧化碳气体和液态水放出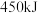 的热量,则该反应的热化学方程式为:
的热量,则该反应的热化学方程式为:___________ 。
(2)甲烷可以用来设计成燃料电池,如图是甲烷燃料电池原理示意图。请写出该电池负极的电极反应式:___________ 。

(1)在一定条件下,
 甲烷气体充分燃烧生成二氧化碳气体和液态水放出
甲烷气体充分燃烧生成二氧化碳气体和液态水放出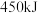 的热量,则该反应的热化学方程式为:
的热量,则该反应的热化学方程式为:(2)甲烷可以用来设计成燃料电池,如图是甲烷燃料电池原理示意图。请写出该电池负极的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
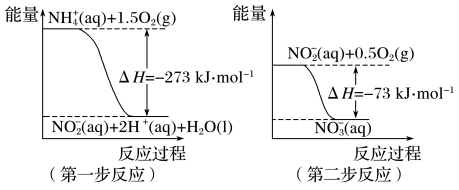
①第一步反应是______________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是___________________ 。
(2)已知红磷比白磷稳定,则反应P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1;4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;ΔH1和ΔH2的关系是ΔH1________ ΔH2(填“>”、“<”或“=”)。
(3)在298 K、101 kPa时,已知:①2H2O(g)=O2(g)+2H2(g) ΔH1;②Cl2(g)+H2(g)=2HCl(g) ΔH2;③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3,则ΔH3与ΔH1和ΔH2之间的关系正确的是________ 。
A.ΔH3=ΔH1+2ΔH2
B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2
D.ΔH3=ΔH1-ΔH2
(4)已知:
①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为
O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为_____________ 。
(5)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
则表中a=________ 。

①第一步反应是
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是
(2)已知红磷比白磷稳定,则反应P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1;4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;ΔH1和ΔH2的关系是ΔH1
(3)在298 K、101 kPa时,已知:①2H2O(g)=O2(g)+2H2(g) ΔH1;②Cl2(g)+H2(g)=2HCl(g) ΔH2;③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3,则ΔH3与ΔH1和ΔH2之间的关系正确的是
A.ΔH3=ΔH1+2ΔH2
B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2
D.ΔH3=ΔH1-ΔH2
(4)已知:
①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为
O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为(5)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
物质 | H2(g) | Br2(g) | HBr(g) |
1mol分子中的化学键断 裂时需要吸收的能量(kJ) | 436 | 200 | a |
则表中a=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH3=-221 kJ·mol-1
若某反应的平衡常数表达式为K=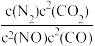 ,则此反应的热化学方程式为
,则此反应的热化学方程式为____________________ 。
(2)N2O5在一定条件下可发生分解反应:2N2O5(g) 4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
①反应开始时体系压强为p0,第2 min时体系压强为p1,则p1∶p0=________ 。2~5 min内用NO2表示的该反应的平均反应速率为________________ 。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是________________ (填字母)。
a.NO2和O2的浓度比保持不变
b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5)
d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g) NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为
NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为________________ (用k正、k逆表示)。
(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。
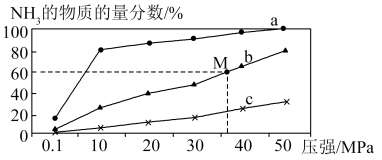
①曲线a对应的温度是________ 。
②M点对应的H2的转化率是________ 。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH3=-221 kJ·mol-1
若某反应的平衡常数表达式为K=
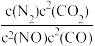 ,则此反应的热化学方程式为
,则此反应的热化学方程式为(2)N2O5在一定条件下可发生分解反应:2N2O5(g)
 4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c(N2O5)/ (mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是
a.NO2和O2的浓度比保持不变
b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5)
d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g)
 NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为
NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp为(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。

①曲线a对应的温度是
②M点对应的H2的转化率是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.氮氧化物、二氧化硫是造成大气污染的主要物质,某科研小组进行如下研究。
(1)写出SO2(g)与NO2(g)反应生成SO3(g)和NO(g)的热化学方程式_____________ 。

(2)常温下用NaOH溶液吸收SO2,当向NaOH溶液中通入足量的SO2时,得到NaHSO3溶液,利用图所示装置(电极均为惰性电极)在pH为4~7之间电解,可使NaHSO3转化为Na2S2O4,并获得较浓的硫酸,这是电化学脱硫技术之一,

①a为电源的_______ (填 “正极”或“负极”);
②阴极的电极反应式为______
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,反应为2Cu + H2O ==Cu2O + H2↑。装置如图所示:该离子交换膜为__________ 离子交换膜(填“阴”或“阳”),该电池的阳极反应式为:____________________ ,钛极附近的pH_______ (增大、减小、不变)。

Ⅲ.氢氧燃料电池是符合绿色化学理念的新型发电装置。右图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

①氢氧燃料电池的能量转化主要形式是________ ,工作时电流方向为_______ (用a→b或b→a表示)。
②负极的电极反应式为__________________ 。
(1)写出SO2(g)与NO2(g)反应生成SO3(g)和NO(g)的热化学方程式

(2)常温下用NaOH溶液吸收SO2,当向NaOH溶液中通入足量的SO2时,得到NaHSO3溶液,利用图所示装置(电极均为惰性电极)在pH为4~7之间电解,可使NaHSO3转化为Na2S2O4,并获得较浓的硫酸,这是电化学脱硫技术之一,

①a为电源的
②阴极的电极反应式为
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,反应为2Cu + H2O ==Cu2O + H2↑。装置如图所示:该离子交换膜为

Ⅲ.氢氧燃料电池是符合绿色化学理念的新型发电装置。右图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

①氢氧燃料电池的能量转化主要形式是
②负极的电极反应式为
您最近一年使用:0次



