把CoCl2溶解于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,生成[Co(NH3)6]2+。此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1molCoCl3·5NH3只生成2molAgCl。请写出表示此配合物结构的化学式:_________ ;此配合物中的Co化合价为_____________ 。
9-10高三·山西太原·阶段练习 查看更多[4]
黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高二下学期4月份月考化学试题人教版高中化学选修3第二章《分子结构与性质》测试题2人教版高中化学选修3第二章《分子结构与性质》测试题1(已下线)2010年山西省太原五中高三第一次月考化学试题
更新时间:2010-09-26 10:43:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氮元素可形成丰富多彩的物质。
(1)光化学烟雾易在PM2.5的催化作用下形成,其中含有NOx、O3、CH2=CHCHO、HCOOH等二次污染物。下列说法正确的是___________ (填字母)。
A.N2O与CO2互为等电子体,其结构式为N=N=O
B.O3的沸点高于O2的沸点
C.CH2=CHCHO分子中碳原子采取sp2和sp3杂化
D.HCOOH在水中的溶解度大,与氢键有关
(2)在配合物中,微粒NH3、NH 、NH2OH中不能作为配体的是
、NH2OH中不能作为配体的是___________ 。
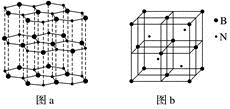
(3)图a为六方氮化硼晶体的结构示意图,该晶体中存在的作用力有___________ 。
(4)六方氮化硼在高温高压下可转化为立方氮化硼,立方氮化硼的晶胞结构如图b所示,晶胞边长为dcm,该晶胞中含有___________ 个氮原子、___________ 个硼原子,立方氮化硼晶体的密度为___________ g·cm-3(设阿伏加德罗常数的值为NA)。
(1)光化学烟雾易在PM2.5的催化作用下形成,其中含有NOx、O3、CH2=CHCHO、HCOOH等二次污染物。下列说法正确的是
A.N2O与CO2互为等电子体,其结构式为N=N=O
B.O3的沸点高于O2的沸点
C.CH2=CHCHO分子中碳原子采取sp2和sp3杂化
D.HCOOH在水中的溶解度大,与氢键有关
(2)在配合物中,微粒NH3、NH
 、NH2OH中不能作为配体的是
、NH2OH中不能作为配体的是(3)图a为六方氮化硼晶体的结构示意图,该晶体中存在的作用力有
(4)六方氮化硼在高温高压下可转化为立方氮化硼,立方氮化硼的晶胞结构如图b所示,晶胞边长为dcm,该晶胞中含有

您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】引起灰霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、含锌有机颗粒物及扬尘等。通过测定灰霾中锌等重金属的含量,可知交通污染是目前造成我国灰霾天气主要原因之一。
(1)Zn2+在基态时核外电子排布式为_________ 。
(2)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、O3、CH2=CH-CHO、HCOOH、CH3COOONO2(PAN)等二次污染物。
①N2O分子的立体构型为______ 。
②CH2=CH-CHO分子中碳原子的杂化方式为______
③1mol HCOOH 中含σ键数目为_____ 。
④NO 能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配体为______ ,Fe的化合价为_____ 。
(1)Zn2+在基态时核外电子排布式为
(2)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、O3、CH2=CH-CHO、HCOOH、CH3COOONO2(PAN)等二次污染物。
①N2O分子的立体构型为
②CH2=CH-CHO分子中碳原子的杂化方式为
③1mol HCOOH 中含σ键数目为
④NO 能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配体为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.将少量CuSO4粉末溶于盛有水的试管中得到一种天蓝色溶液,先向试管里的溶液中滴加氨水,首先形成蓝色沉淀。继续滴加氨水,沉淀溶解,得到深蓝色溶液;再加入乙醇溶剂,将析出深蓝色的晶体。
(1)溶液中呈天蓝色微粒的化学式是_______________________ 。
(2)加入乙醇的作用是_____________________________ 。
(3)写出蓝色沉淀溶解成深蓝色溶液的离子方程式______________ 。
(4)得到的深蓝色晶体是[Cu(NH3)4]SO4·H2O,晶体中Cu2+与NH3之间的化学键类型为_____________ , 该晶体中配体分子的空间构型为_______________________ 。(用文字描述)
II.含 、Fe元素的物质在生产生活中有重要的用途。回答下列问题:
、Fe元素的物质在生产生活中有重要的用途。回答下列问题:
(1) 在K3[Fe(CN)6]中中心离子是________ ,配体是_________ ,配位数是_________ 。
(2)某个 (Ⅱ)有机配合物的结构如图所示:
(Ⅱ)有机配合物的结构如图所示:
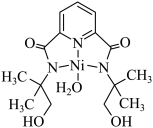
①该分子中N原子的杂化方式为________ 、________ 。
②请在图中用“ ”标出
”标出 的配位键。
的配位键。_____
(3) Ge,As,Se元素处于同一周期,三种元素原子的第一电离能由大到小的顺序为__________________ 。
(4) 的酸性强于
的酸性强于 的原因是
的原因是_________________________________________ 。
(1)溶液中呈天蓝色微粒的化学式是
(2)加入乙醇的作用是
(3)写出蓝色沉淀溶解成深蓝色溶液的离子方程式
(4)得到的深蓝色晶体是[Cu(NH3)4]SO4·H2O,晶体中Cu2+与NH3之间的化学键类型为
II.含
 、Fe元素的物质在生产生活中有重要的用途。回答下列问题:
、Fe元素的物质在生产生活中有重要的用途。回答下列问题:(1) 在K3[Fe(CN)6]中中心离子是
(2)某个
 (Ⅱ)有机配合物的结构如图所示:
(Ⅱ)有机配合物的结构如图所示:
①该分子中N原子的杂化方式为
②请在图中用“
 ”标出
”标出 的配位键。
的配位键。(3) Ge,As,Se元素处于同一周期,三种元素原子的第一电离能由大到小的顺序为
(4)
 的酸性强于
的酸性强于 的原因是
的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】过渡元素的化合物在生活中有着广泛的应用。请回答下列问题:
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是______ 。Zn位于元素周期表的______ 区。
(2)基态锰原子有______ 种空间运动状态的电子,锰有多种化合价,在+2、+3、+4、+5和+6中,最稳定的化合价是______ 。
(3)基态铁原子有______ 个未成对电子,三价铁离子的电子排布式为______ 。可用硫氰化钾检验氯化铁溶液中的铁离子,形成的血红色配合物中,主要是Fe3+与SCN-以个数比1:1形成的配离子的颜色,含该离子的配合物的化学式是______ 。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)基态锰原子有
(3)基态铁原子有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】碳、氮、氧、氟、钙、铜等元素的化合物广泛存在于自然界,回答下列问题:
(1)将乙炔(C2H2)通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。1个乙炔分子中σ键数目为___________ ,基态Cl原子的核外电子排布式为__________ ,[Cu(NH3)4] 2+中Cu 2+的配位数为___________ 。
(2)NF3是微电子工业中优良的等离子刻蚀气体。元素第一电离能N___________ F(填“>”“<”或“=”), NF3中氮原子的杂化轨道类型为____________________ ,NF3分子的空间构型___________ 。
(3)氮的氧化物中与CO2互为等电子体的分子为___________ (写化学式)。
(1)将乙炔(C2H2)通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。1个乙炔分子中σ键数目为
(2)NF3是微电子工业中优良的等离子刻蚀气体。元素第一电离能N
(3)氮的氧化物中与CO2互为等电子体的分子为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】金属钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,主要步骤如下:
Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C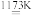 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6CO
TiO2+2Cl2+2C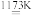 TiCl4+2CO
TiCl4+2CO
Ⅱ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg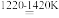 Ti+2MgCl2
Ti+2MgCl2
Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为___ 。
(2)与CO互为等电子体的离子为___ (填化学式)。
(3)在CH2Cl2、HCHO、CO2、C2H4中,碳原子采取sp2杂化的分子有___ 。
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于___ (填“原子”“分子”或“离子”)晶体。
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是___ ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为___ 。
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为___ 。

Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C
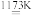 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6COTiO2+2Cl2+2C
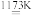 TiCl4+2CO
TiCl4+2COⅡ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg
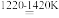 Ti+2MgCl2
Ti+2MgCl2Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为
(2)与CO互为等电子体的离子为
(3)在CH2Cl2、HCHO、CO2、C2H4中,碳原子采取sp2杂化的分子有
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为

您最近半年使用:0次



