(1)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃10kPa下,10g甲醇燃烧生成CO2和液态水时放热226.8kJ。请写出表示甲醇燃烧的热化学方程式:_____________________________________
(2) 某些化学反应可用下式表示:A + B C + D + H2O
C + D + H2O
请回答下列问题:
①若A、D均可用于消毒,且C是家家户户的厨房必备的调味品之一,写出该反应的离子方程式__________________________ 。
②若A为水垢的主要成分之一,B是日常生活常见有机物(厨房用品),写出该反应的化学方程式:_______________________ 。
③若C、D均为气体且都能使澄清石灰水变浑浊,则只用___________ 或__________ (任写两种试剂的名称)就可以鉴别C、D两种气体。
(2) 某些化学反应可用下式表示:A + B
 C + D + H2O
C + D + H2O请回答下列问题:
①若A、D均可用于消毒,且C是家家户户的厨房必备的调味品之一,写出该反应的离子方程式
②若A为水垢的主要成分之一,B是日常生活常见有机物(厨房用品),写出该反应的化学方程式:
③若C、D均为气体且都能使澄清石灰水变浑浊,则只用
10-11高三上·福建福州·期中 查看更多[1]
(已下线)2011届福建省福州市八县(市)高三上学期期中联考化学卷
更新时间:2016-12-09 01:01:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氯元素的单质及其化合物在生产、生活中均有重要用途。请结合相关知识回答下列问题:
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式___________ ,使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生 ,请用离子方程式表示其原因
,请用离子方程式表示其原因___________ 。
(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯( )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应: ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: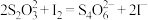 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:___________ 。
(4)实验室要配制1L 0.2 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:
①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为___________ (填序号),定容的具体操作是___________ 。
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式
 ,请用离子方程式表示其原因
,请用离子方程式表示其原因(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯(
 )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应:
 ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: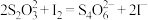 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:(4)实验室要配制1L 0.2
 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求书写化学方程式或离子方程式。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为___________ 。
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为___________ 。
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为___________ 。
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的离子 方程式为___________ 。
(5)SO2能使氯水褪色,相应的离子 方程式为___________ 。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的
(5)SO2能使氯水褪色,相应的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某实验小组用MnO2与浓盐酸加热制取Cl2,并将得的氯气与潮湿的Ca(OH)2固体反应制取少量漂白粉,实验装置如下图:
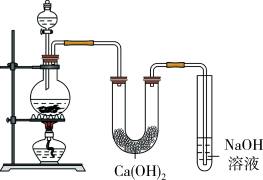
回答下列问题:
(1)漂白粉的有效成分是____________ (写化学式)。
(2)烧瓶中发生反应的化学方程式为_______________ 。
(3)温度较高时氯气与消石灰发生反应:6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O,该反应中氧化剂和还原剂的物质的量之比是________ ;若反应消耗0.3molCl2,则转移的电子数为__________ 个。

回答下列问题:
(1)漂白粉的有效成分是
(2)烧瓶中发生反应的化学方程式为
(3)温度较高时氯气与消石灰发生反应:6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O,该反应中氧化剂和还原剂的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有混有少量SO2杂质的CO2气体,请选用适当的实验装置,收集纯净干燥的CO2气体。

(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是_______ (填序号,下同)。
A.dcabh B.efabg C.feabg
(2)本实验除去SO2的原理是利用SO2的_______。
(3)SO2与酸性高锰酸钾溶液反应的离子方程式是_______ 。

(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是
A.dcabh B.efabg C.feabg
(2)本实验除去SO2的原理是利用SO2的_______。
| A.氧化性 | B.漂白性 | C.还原性 | D.酸性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是______________________ ;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 7N2+12H2O
7N2+12H2O
① 上述反应中被还原的元素是_________ (填元素符号),反应中每转移3mol电子,生成标准状况下N2的体积为____________ ;
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
上述反应中NOx所起的作用是_____________ ;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的___________ 性质(选填字母编号)。
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物
②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有______ (填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是_________________ (用离子方程式表示)。
(1)烟气脱硫、脱硝的环境意义是
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3
 7N2+12H2O
7N2+12H2O① 上述反应中被还原的元素是
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3
 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2上述反应中NOx所起的作用是
(3)下表列出了2种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的
A.漂白性 B.氧化性
 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.从以下试剂中选择合适的试剂实现转化的方程式。
试剂清单:①浓H2SO4 ②Na2S溶液 ③酸性KMnO4溶液 ④H2SO3溶液 ⑤木炭
(1)S(+4)→S(+6)离子方程式_______ 。
(2)S(+6)→S(+4)化学方程式_______ 。
II.下列溶液或用品中:
①澄清石灰水;②H2S溶液;③酸性KMnO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是________ 。
A.①⑤⑦ B.①⑤ C.①⑦ D.②③④⑤⑥
若将过量的SO2通入澄清石灰水中,写出反应的离子方程式_______
III.工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2、NO2+NO+Na2CO3=2NaNO2+CO2,现有aLNO2和bLNO的混合气体(气体体积已经换算成标准状况下)恰好被200mLNa2CO3溶液完全吸收,则a、b应满足的关系为_______ 。Na2CO3溶液的物质的量浓度为_______ mol·L-1。
试剂清单:①浓H2SO4 ②Na2S溶液 ③酸性KMnO4溶液 ④H2SO3溶液 ⑤木炭
(1)S(+4)→S(+6)离子方程式
(2)S(+6)→S(+4)化学方程式
II.下列溶液或用品中:
①澄清石灰水;②H2S溶液;③酸性KMnO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是
A.①⑤⑦ B.①⑤ C.①⑦ D.②③④⑤⑥
若将过量的SO2通入澄清石灰水中,写出反应的离子方程式
III.工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2、NO2+NO+Na2CO3=2NaNO2+CO2,现有aLNO2和bLNO的混合气体(气体体积已经换算成标准状况下)恰好被200mLNa2CO3溶液完全吸收,则a、b应满足的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察图象,然后回答问题。
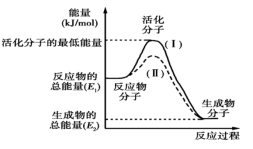
(1)图中所示反应是_______ (填“吸热”或“放热”)反应,该反应的ΔH=_______ (用含E1、E2的代数式表示)。
(2)下列4个反应中,符合示意图描述的反应的是_______ (填代号)。
a.盐酸与NaOH反应
b.Na与H2O反应生成H2
c.铝热反应
d.高温煅烧石灰石
Ⅱ.按要求完成下列问题:
(1)在1.01×105 Pa时,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则H2的燃烧热的热化学方程式为_______
(2)1.00 L 1.00 mol·L-1H2SO4溶液与2.00 L 1.00 mol·L-1NaOH溶液完全反应,放出114.6 kJ热量,该反应的中和热的热化学方程式为_______
(3)已知N2(g) + 2O2(g) = 2NO2(g);∆H=+67.7KJ/mol,
N2H4(g) + O2(g) = N2(g)+2H2O(g);∆H= -534KJ/mol,
则N2H4(g)与NO2(g)完全反应生成N2(g)和H2O(g)的热化学方程式为_______
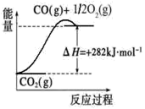
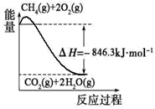
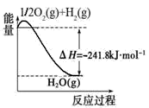
(4)可以甲烷为原料制得:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。有关化学反应的能量变化如图所示。CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为_______

(1)图中所示反应是
(2)下列4个反应中,符合示意图描述的反应的是
a.盐酸与NaOH反应
b.Na与H2O反应生成H2
c.铝热反应
d.高温煅烧石灰石
Ⅱ.按要求完成下列问题:
(1)在1.01×105 Pa时,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则H2的燃烧热的热化学方程式为
(2)1.00 L 1.00 mol·L-1H2SO4溶液与2.00 L 1.00 mol·L-1NaOH溶液完全反应,放出114.6 kJ热量,该反应的中和热的热化学方程式为
(3)已知N2(g) + 2O2(g) = 2NO2(g);∆H=+67.7KJ/mol,
N2H4(g) + O2(g) = N2(g)+2H2O(g);∆H= -534KJ/mol,
则N2H4(g)与NO2(g)完全反应生成N2(g)和H2O(g)的热化学方程式为
(4)可以甲烷为原料制得:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。有关化学反应的能量变化如图所示。CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为



您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请参考题中图表,已知E1=134kJ•mol-1、E2=368kJ•mol-1,根据要求回答问题。
(1)图I是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)的过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是_____ ,ΔH的变化是_____ 。(填“增大”“减小”或“不变”)

(2)图II表示一定条件下,在水溶液中1molCl-、ClO (x=1,2,3,4)的能量相对大小。
(x=1,2,3,4)的能量相对大小。

①D是_____ (填离子符号)。
②B→A+C反应的热化学方程式为_____ (用离子符号表示)。
(1)图I是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)的过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是

(2)图II表示一定条件下,在水溶液中1molCl-、ClO
 (x=1,2,3,4)的能量相对大小。
(x=1,2,3,4)的能量相对大小。
①D是
②B→A+C反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】乙烯、乙酸、苯是重要的有机化合物。根据题意填空:
(l)乙烯与H2反应生成乙烷,其反应类型为________ 。
(2)乙酸可用来除去热水瓶内的水垢,此过程中乙酸表现的性质为________ 。
(3)苯与液溴在溴化铁催化下发生取化反应,生成的有机物为______ (填结构简式)。
(l)乙烯与H2反应生成乙烷,其反应类型为
(2)乙酸可用来除去热水瓶内的水垢,此过程中乙酸表现的性质为
(3)苯与液溴在溴化铁催化下发生取化反应,生成的有机物为
您最近一年使用:0次
【推荐2】按照组成元素可将有机物分为烃和烃的衍生物。
Ⅰ.某些烃分子的模型如图所示,回答下列问题:

(1)丁的分子式是_______ ,写出戊的同分异构体的结构简式_______ (一种即可)。
(2)写出乙完全燃烧的化学方程式_______ 。
Ⅱ.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸(CH2=CHCOOH)、乳酸( )等。
)等。
(3)丙烯酸中含氧官能团的名称是_______ 。
(4)丙烯酸可以使溴水褪色,该反应类型为_______ ,写出反应的化学方程式_______ 。
(5)3.6 g乳酸(分子量:90)与足量钠反应,能生成标准状况下H2的体积为_______ L。
(6)丙烯酸可以和乙醇发生酯化反应,写出反应方程式:_______ 。
Ⅰ.某些烃分子的模型如图所示,回答下列问题:

(1)丁的分子式是
(2)写出乙完全燃烧的化学方程式
Ⅱ.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸(CH2=CHCOOH)、乳酸(
 )等。
)等。(3)丙烯酸中含氧官能团的名称是
(4)丙烯酸可以使溴水褪色,该反应类型为
(5)3.6 g乳酸(分子量:90)与足量钠反应,能生成标准状况下H2的体积为
(6)丙烯酸可以和乙醇发生酯化反应,写出反应方程式:
您最近一年使用:0次

 (g)反应生成CuO(s),放出157.3kJ的热量
(g)反应生成CuO(s),放出157.3kJ的热量 (g)与适量
(g)与适量 (g)和
(g)和 (l),放出1411.0kJ的热量
(l),放出1411.0kJ的热量 (g),吸收131.5kJ的热量
(g),吸收131.5kJ的热量

