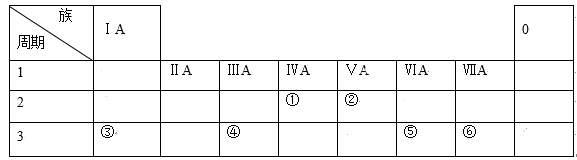
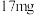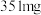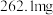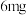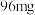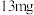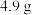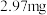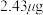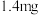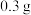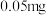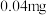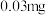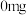下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:
(除特别注明外,其它一律用化学式表示)

(1)在这些元素中,化学性质最不活泼的是:________ (填具体元素符号,下同),其原子结构示意图为_________ 。元素K名称为_______ 在周期表中的位置______ 。
(2)最高价氧化物水化物中碱性最强的化合物的电子式是:_______ 。
(3)某元素二价阳离子的核外有10个电子,该元素是______ (填元素名称)。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序_________ 。
(5)F、H、J的最高价氧化物对应水化物的酸性由强到弱的顺序_________ 。
(6)I、J、K三种元素形成的离子,离子半径由大到小的顺序是_________ 。
(7)元素I的氢化物的结构式为________ ;该氢化物常温下和元素K的单质反应的化学方程式为__________ 。
(除特别注明外,其它一律用化学式表示)

(1)在这些元素中,化学性质最不活泼的是:
(2)最高价氧化物水化物中碱性最强的化合物的电子式是:
(3)某元素二价阳离子的核外有10个电子,该元素是
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序
(5)F、H、J的最高价氧化物对应水化物的酸性由强到弱的顺序
(6)I、J、K三种元素形成的离子,离子半径由大到小的顺序是
(7)元素I的氢化物的结构式为
更新时间:2016-12-09 15:37:27
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】下面是元素周期表的一部分,按要求回答下列问题:
(1)已知⑥号元素的一种核素的中子数为8,则其最简单的气态氢化物的摩尔质量为___________  。
。
(2)非金属性最强的单质与水反应的化学方程式为___________ 。
(3)某元素的最高价氧化物的水化物既能与强酸反应又能与强碱反应,该元素的元素符号是___________ ,向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH溶液至过量,现象为___________ 。
(4)设计实验方案;比较⑧与⑪单质氧化性的强弱,请将方案填入下表。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ⑥ | ⑦ | ⑨ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑪ |
 。
。(2)非金属性最强的单质与水反应的化学方程式为
(3)某元素的最高价氧化物的水化物既能与强酸反应又能与强碱反应,该元素的元素符号是
(4)设计实验方案;比较⑧与⑪单质氧化性的强弱,请将方案填入下表。
| 实验步骤 | 实验现象 | 实验结论 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表列出了A~G7种元素在周期表中的位置:
(1)分别写出A、D、G的元素符号:_______ 、________ 、________ ,其中化学性质最不活泼的是________ (填元素符号);
(2)F的氢化物中化学键的类型是___________ ,F的最高价氧化物对应的水化物的化学式是___________ ;
(3)C、D、E三种元素中,氢化物种类最多的是___________ ;
(4)写出B与F形成的化合物发生水解反应的离子方程式___________ ;
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | D | E | |||||
| 3 | B | F | G | |||||
| 4 | A |
(2)F的氢化物中化学键的类型是
(3)C、D、E三种元素中,氢化物种类最多的是
(4)写出B与F形成的化合物发生水解反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:(用元素符号或化学式回答下列问题)
___________ 与盐酸反应最剧烈,___________ 与盐酸反应的速度最慢;___________ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为___________ 。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律
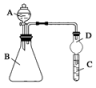
(1)仪器A的名称为___________ ,干燥管D的作用为___________ 。
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液___________ 的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用___________ 溶液吸收尾气。
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液观察到C中溶液___________ 的现象即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰试验,应在两装置间添加装有___________ 溶液的洗气瓶除去。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:(用元素符号或化学式回答下列问题)
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(1)仪器A的名称为
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液观察到C中溶液
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】现有部分元素的性质与原子 或分子
或分子 结构如表所示:
结构如表所示:
(1)画出元素T的原子结构示意图:__ 。
(2)元素Y与元素Z相比,金属性较强的是__  用元素符号表示
用元素符号表示 ,下列表述中能证明这一事实的是
,下列表述中能证明这一事实的是___  填字母
填字母 。
。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质与水反应剧烈
d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T、X、Y、Z中的两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式:__ 。
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-)__ r(Yn+)(填“>”,“<”或“=”)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式___ 。
 或分子
或分子 结构如表所示:
结构如表所示:| 元素编号 | 元素性质与原子 或分子 或分子 结构 结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的金属离子中半径最小 |
(1)画出元素T的原子结构示意图:
(2)元素Y与元素Z相比,金属性较强的是
 用元素符号表示
用元素符号表示 ,下列表述中能证明这一事实的是
,下列表述中能证明这一事实的是 填字母
填字母 。
。a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质与水反应剧烈
d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T、X、Y、Z中的两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式:
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】门捷列夫是俄国科学家,他发明的元素周期表是化学领域的重要里程碑。周期表的发明帮助人们更好地理解元素性质和变化规律,推动了化学和其他学科的发展。门捷列夫被誉为“现代化学之父”。
(1)②的元素符号是:___________ ;①的最高价氧化物对应的水合物化学式是___________ 。
(2)磷元素在周期表中的位置是:___________ 周期___________ 族。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方程式___________ 。
(3)③、④两种元素的简单离子半径大小关系:___________ (填离子符号)
(4)④、⑤和⑥中,金属性最强的元素是___________ (填元素符号);③和⑧两种元素形成的气态氢化物稳定性强的是:___________ (填化学式);④、⑤、⑥、⑦、⑧元素最高价氧化物形成的水化物中酸性最强的是___________ (填化学式)。
(5)Cl元素比S元素的非金属性强,是因为从结构层面看来,Cl原子和S原子___________ 相同,而Cl原子的核电荷数比S原子___________ ,所以,原子核对电子的吸引作用更___________ 。能证明这一事实的化学反应为___________ (请写出化学方程式)。
| 族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)磷元素在周期表中的位置是:
(3)③、④两种元素的简单离子半径大小关系:
(4)④、⑤和⑥中,金属性最强的元素是
(5)Cl元素比S元素的非金属性强,是因为从结构层面看来,Cl原子和S原子
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】元素周期表与元素周期律在化学学习研究中有很重要的作用。下表是元素周期表的一部分
(1)④和②组成的一种化合物颜色为淡黄色,请写出该化合物的电子式_______ ,该化合物含有的化学键类型有_______ 。
(2)请写出元素①的简单氢化物的结构式_______ 。
(3)元素①、②、⑦简单氢化物的稳定性最强的是_______ (用化学式表示) 。
(4)元素①、②、⑧简单氢化物的沸点最高的是_______ (用化学式表示) 。
(5)元素③、⑤、⑨的简单离子半径由大到小的顺序(用离子符号表示)_______ 。
(6)写出元素①最高价氧化物对应水化物稀溶液与铜应的化学方程式_______ 。
(7)元素非金属性强弱比较有很多方法,其中比较⑧和⑨的非金属性强弱的研究方案中不可行的是:_______(填序号)。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | |||||||
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)请写出元素①的简单氢化物的结构式
(3)元素①、②、⑦简单氢化物的稳定性最强的是
(4)元素①、②、⑧简单氢化物的沸点最高的是
(5)元素③、⑤、⑨的简单离子半径由大到小的顺序(用离子符号表示)
(6)写出元素①最高价氧化物对应水化物稀溶液与铜应的化学方程式
(7)元素非金属性强弱比较有很多方法,其中比较⑧和⑨的非金属性强弱的研究方案中不可行的是:_______(填序号)。
| A.比较两种单质的颜色 | B.比较两种单质与 化合的难易程度 化合的难易程度 |
| C.依据两元素在周期表中的位置 | D.比较氧化物对应水化物的酸性 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】①~⑨九种元素在元素周期表中的位置如图所示:
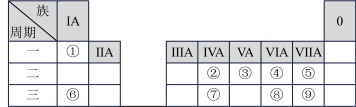
请按要求回答下列问题:
(1)②的元素名称为___________ ;⑧的原子结构示意图为___________ 。
(2)上述九种元素中,属于碱金属元素的为___________ (填元素符号,下同),非金属性最强的为___________ ;其最高价氧化物对应的水化物中,酸性最强的为___________ (填化学式)。
(3)③形成的常见的气体单质的结构式为___________ ;用电子式表示⑥和⑨组成的化合物的形成过程:___________ 。
(4)④⑥形成的一种化合物常用作供氧剂,该物质与④的最简单氢化物反应的化学方程式为___________ ,该反应中的还原剂为___________ (填化学式)。

请按要求回答下列问题:
(1)②的元素名称为
(2)上述九种元素中,属于碱金属元素的为
(3)③形成的常见的气体单质的结构式为
(4)④⑥形成的一种化合物常用作供氧剂,该物质与④的最简单氢化物反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】醋是一种低升糖指数的食物,适合肥胖症、单纯性肥胖、高血糖人群食用。每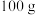 醋中常见营养元素和其他营养元素如下表:
醋中常见营养元素和其他营养元素如下表:
常见营养元素 | 其他营养元素 | ||||
|
|
|
|
|
|
|
|
|
|
|
|
碳水化合物 |
|
|
|
|
|
蛋白质 |
| 烟酸 |
|
|
|
脂肪 |
| 核黄素 |
|
|
|
—— | 硫胺素 |
| 维生素 |
| |
回答下列问题:
(1)上述表格中的
 是
是 元素在元素周期表中的位置是
元素在元素周期表中的位置是(2)“其他营养元素”中,位于同主族的金属元素是
(3)硫胺素中含有
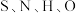 等元素,利用元素周期律知识比较(用“
等元素,利用元素周期律知识比较(用“ ”或“
”或“ ”表示):
”表示):①金属性:
 ;
;
②酸性:
 ;
;
③还原性:
 ;
;
④稳定性:
 。
。
(4)
 元素在元素周期表中的相关信息如图:
元素在元素周期表中的相关信息如图:25 锰
54.94 |
①锰元素所有核素的质子数为
②“54.94”表示锰元素的
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是_______ 。根据对角线规则,B的一些化学性质与元素_______ 的相似。
(2)NH3BH3分子中,N—B化学键称为_______ 键,其电子对由_______ 提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为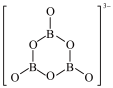 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是_______ 。
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
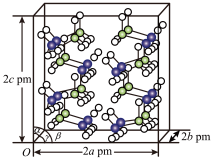
氨硼烷晶体的密度ρ=_______ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)H、B、N中,原子半径最大的是
(2)NH3BH3分子中,N—B化学键称为
 +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。

氨硼烷晶体的密度ρ=
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知A、B、C、D、E、F是分属三个短周期的六种主族元素,且原子序数依次增大,D元素焰色试验时火焰呈黄色。①B是植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染。②C和D能形成电子总数为30和38的两种化合物。③E与C同主族。请回答下列问题:
(1)元素F在元素周期表中的位置是___________ 。
(2)C、D、E三种元素形成的简单离子的离子半径由小到大的顺序是___________ (用离子符号表示)。
(3)C和D形成电子总数为38的化合物中化学键类型有___________ (填“离子键”“极性共价键”或“非极性共价键”)。
(4)写出D的最高价氧化物对应的水化物的电子式:___________ 。
(5)E、F两种元素形成的氢化物中还原性较强的是___________ (填化学式);用电子式表示该化合物的形成过程:___________ 。
(1)元素F在元素周期表中的位置是
(2)C、D、E三种元素形成的简单离子的离子半径由小到大的顺序是
(3)C和D形成电子总数为38的化合物中化学键类型有
(4)写出D的最高价氧化物对应的水化物的电子式:
(5)E、F两种元素形成的氢化物中还原性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题。
(1)在这10种元素中,化学性质最不活泼的元素是___________ (写序号),得电子能力最强的原子是___________ (用元素符号表示);元素⑦的最高价氧化物对应的水化物是___________ (写化学式)。
(2)元素④的离子结构示意图为___________ 。
(3)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示)___________ 。
(4)请写出:
(i)③的单质置换出⑥的单质的化学方程式:___________ 。
(ii)①和⑤两种元素最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑧ | ⑩ | |||||
| 三 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
| 四 | ② | ④ |
(2)元素④的离子结构示意图为
(3)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示)
(4)请写出:
(i)③的单质置换出⑥的单质的化学方程式:
(ii)①和⑤两种元素最高价氧化物对应的水化物相互反应的化学方程式为
您最近一年使用:0次