利用氧化还原反应原理配平
(1)__ NH3+___ O2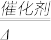
____ NO +____ H2O
(2)____ FeSO4+____ KNO3+____ H2SO4=____ K2SO4+____ Fe2(SO4)3+____ NO↑+____ H2O
(1)
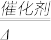
(2)
10-11高一下·福建福州·阶段练习 查看更多[2]
更新时间:2011-03-25 10:22:05
|
【知识点】 氧化还原反应方程式的配平解读
相似题推荐
【推荐1】三氧化砷,俗称砒霜,分子式As2O3,是最具商业价值的砷化合物及主要的砷化学开始物料。它也是最古老的毒物之一,无臭无味,外观为白色霜状粉末,故称砒霜。
(1)完成并配平下列化学方程式:___ As2O3+___ Zn+___ H2SO4→___ AsH3+___ ZnSO4+___
(2)As2O3在上述反应中显示出来的性质是___ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.2molAsH3,则转移电子的物质的量为___ mol。
(4)砷化氢AsH3是一种很强的还原性,在室温下它能在空气中自然,其氧化产物是砒霜,写出该反应的化学方程式___ 。
(1)完成并配平下列化学方程式:
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.2molAsH3,则转移电子的物质的量为
(4)砷化氢AsH3是一种很强的还原性,在室温下它能在空气中自然,其氧化产物是砒霜,写出该反应的化学方程式
您最近一年使用:0次
【推荐2】Ⅰ.(1)以下是日常生活中常见的一些物质:①液氯、②酒精、③CO2、④熟石灰、⑤碳酸钠、⑥稀盐酸、⑦CaO、③Na2O2、⑨Cu,请你指出(填写序号):
属于碱性氧化物的是___ ;能导电的是___ 。
(2)胶体粒子直径在___ nm之间
Ⅱ.化学计量在化学中占有重要地位。根据计算填空:
(1)实验室某浓盐酸的质量分数为36.5%,密度为1.20g·cm-3,此浓盐酸的物质的量浓度是___ mol·L-1;
(2)6.8gH2O2与标准状况下___ LCO2所含氧原子数相同;
Ⅲ.除去Mg粉中的Al粉,指明应加入的试剂,写出有关的离子反应方程式。
Mg粉(Al粉):试剂___ ,离子方程式____ 。
IV.配平如下方程式
___ NaClO+___ NH3·H2O=___ N2H4+___ NaCl+___ H2O
属于碱性氧化物的是
(2)胶体粒子直径在
Ⅱ.化学计量在化学中占有重要地位。根据计算填空:
(1)实验室某浓盐酸的质量分数为36.5%,密度为1.20g·cm-3,此浓盐酸的物质的量浓度是
(2)6.8gH2O2与标准状况下
Ⅲ.除去Mg粉中的Al粉,指明应加入的试剂,写出有关的离子反应方程式。
Mg粉(Al粉):试剂
IV.配平如下方程式
您最近一年使用:0次
【推荐3】亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。
(1)已知亚硝酸钠能发生如下反应,请将化学方程式配平:_____ 。
_______NaNO2 + _______HI =_______NO↑+_______NaI + _______I2 + _______H2O
(2)①用单线桥法标出该反应中电子转移的方向及数目:_______ 。
②被氧化的原子与被还原的原子数目之比为_______ 。
③若反应中转移0.1 mol电子,则被消耗的NaNO2为_______ g。
(3)HI在反应中表现的性质是_______ (填序号)
① 还原性 ② 氧化性 ③ 酸性
(4)自来水中的NO 对人类健康会产生危害,碱性条件下用Mg还原NO
对人类健康会产生危害,碱性条件下用Mg还原NO ,主要产物是Mg(OH)2 、N2等,写出该反应过程的离子方程式
,主要产物是Mg(OH)2 、N2等,写出该反应过程的离子方程式_______ 。
(1)已知亚硝酸钠能发生如下反应,请将化学方程式配平:
_______NaNO2 + _______HI =_______NO↑+_______NaI + _______I2 + _______H2O
(2)①用单线桥法标出该反应中电子转移的方向及数目:
②被氧化的原子与被还原的原子数目之比为
③若反应中转移0.1 mol电子,则被消耗的NaNO2为
(3)HI在反应中表现的性质是
① 还原性 ② 氧化性 ③ 酸性
(4)自来水中的NO
 对人类健康会产生危害,碱性条件下用Mg还原NO
对人类健康会产生危害,碱性条件下用Mg还原NO ,主要产物是Mg(OH)2 、N2等,写出该反应过程的离子方程式
,主要产物是Mg(OH)2 、N2等,写出该反应过程的离子方程式
您最近一年使用:0次



